Un team di scienziati della UC San Francisco e del National Institutes of Health ha realizzato un altro tipo di CRISPR che potrebbe cambiare radicalmente il modo in cui gli scienziati studiano le malattie del cervello.
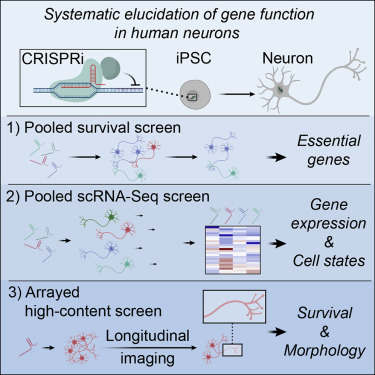
In un articolo pubblicato il 15 agosto sulla rivista Neuron, i ricercatori descrivono una tecnica che utilizza una versione speciale di CRISPR sviluppata presso l’UCSF per alterare sistematicamente l’attività dei geni nei neuroni umani generati dalle cellule staminali, la prima fusione riuscita di cellule staminali derivate e tecnologie di screening CRISPR.
Sebbene sia noto che mutazioni e altre varianti genetiche siano associate ad un aumentato rischio di molte malattie neurologiche, gli scienziati lavorano ancora per capire esattamente come questi geni causano la malattia.
“Prima di questo studio, c’erano limitazioni significative a ciò che gli scienziati potevano fare con i neuroni umani in laboratorio”, ha affermato Martin Kampmann, Professore associato presso l’Istituto per le malattie neurodegenerative dell’UCSF, ricercatore della Repubblica Ceca e co- autore senior del nuovo studio.
“Per prima cosa, fino a poco tempo fa, gli scienziati non avevano modo di ottenere in modo affidabile cellule cerebrali umane che potevano essere utilizzate in esperimenti avanzati di di laboratorio”, ha spiegato Kampmann, anche lui membro dell’UCSF Weill Institute for Neurosciences. “Abbiamo avuto la donazione di neuroni da parte di pazienti sottoposti a procedure che comportano la rimozione del tessuto cerebrale per il trattamento dell’epilessia o del cancro al cervello. Ma questi campioni possono sopravvivere solo per pochi giorni e non è possibile eseguire esperimenti per sondare la funzione genica in breve tempo”.
Gli scienziati hanno generalmente fatto affidamento su modelli animali di malattie cerebrali che tuttavia, non possono cogliere molte sfumature della neurobiologia umana.
Una svolta è arrivata nel 2006 quando Shinya Yamanaka, dell’Università di Kyoto e Gladstone Institutes, affiliati all’UCSF, hanno scoperto un modo per riavvolgere l’orologio evolutivo e trasformare le cellule adulte in cellule staminali che potrebbero essere trasformate in qualsiasi tipo di cellula del corpo, compresi i neuroni. Queste “cellule staminali pluripotenti indotte” (iPSC) hanno reso le cellule cerebrali umane ampiamente disponibili per le ricerche di laboratorio.
Quando il sistema di editing genetico CRISPR è arrivato sei anni dopo, gli scienziati hanno pensato di avere finalmente tutti gli strumenti necessari per manipolare i geni nei neuroni umani e determinare come contribuiscono alle malattie neurologiche.
Ma gli scienziati hanno rapidamente scoperto che il macchinario per il taglio del DNA del sistema CRISPR, un enzima noto come Cas9, non si mescolavano bene con le iPSC. “Le cellule staminali hanno una risposta al danno del DNA molto attiva. Quando Cas9 produce anche solo uno o due tagli di DNA, può portare alla tossicità che provoca la morte delle cellule“, ha spiegato Kampmann.
Quindi Kampmann ha deciso di affrontare il problema della tossicità.
Come postdoc nel laboratorio dell’UCSF, con il Professor Jonathan Weissman, Kampmann ha co-inventato uno strumento noto come CRISPRi (per “interferenza”), una forma modificata della tecnologia CRISPR in cui l’enzima Cas9 è stato disattivato. Quando CRISPRi trova il gene che sta cercando, sopprime la sua attività senza effettuare tagli. Di conseguenza, a differenza dello standard CRISPR-Cas9, secondo Kampmann, CRISPRi non dovrebbe essere tossico per le iPSC o neuroni derivati dalle cellule staminali.
Nel nuovo articolo, Kampmann e i suoi collaboratori descrivono come hanno adattato CRISPRi per l’uso nelle iPSC umane e neuroni derivati da iPSC e hanno scoperto che poteva colpire e interferire con i geni senza uccidere la cellula, un’impresa che a lungo gli scienziati avevano eluso.
I ricercatori hanno dimostrato come la loro tecnica può essere utilizzata per trovare geni che possono causare o contribuire alle malattie del cervello. Ad esempio, hanno identificato geni che prolungano in modo specifico la durata dei neuroni, ma non hanno effetti comparabili sulle iPSC o cellule tumorali. Hanno anche scoperto geni che aumentavano il numero di neuriti – proiezioni che crescono dai neuroni e trasmettono segnali nervosi – e hanno determinato la frequenza con cui si ramificavano.
Vedi anche,Una nuova ricerca potrebbe perfezionare le forbici genetiche CRISPR.
Ma una delle scoperte più sorprendenti è stata la scoperta che i geni che si occupano di “pulizia“, noti per essere essenziali per la sopravvivenza, ma che si ritiene svolgano la stessa funzione in tutte le cellule, si comportano in modo diverso nei neuroni e nelle cellule staminali. Quando i ricercatori hanno interferito con gli stessi geni di pulizia in questi due tipi di cellule, le cellule hanno risposto attivando (o inattivando) un insieme di geni molto diverso. Questo risultato suggerisce che, contrariamente alla saggezza precedente, i geni delle pulizie potrebbero non funzionare allo stesso modo in diversi tipi di cellule , un’idea che Kampmann e il suo laboratorio sono desiderosi di esplorare ulteriormente, poiché queste differenze possono svolgere ruoli importanti nella malattia.
Kampmann sta ora usando la tecnologia per studiare diversi tipi di neuroni nel tentativo di determinare perché alcune malattie colpiscono selettivamente solo un sottoinsieme di neuroni o il modo in cui i neuroni motori sono selettivamente danneggiati nella SLA. Sta inoltre espandendo le sue ricerche ad altri tipi di cellule cerebrali, comprese le cellule note come astrociti e microglia.
Alla fine, l’obiettivo è trasformare questa tecnologia che combina CRISPRi e iPSC in uno strumento che scopre nuovi approcci terapeutici tanto necessari per il trattamento delle malattie del cervello.
“Una delle grandi sfide che il campo deve affrontare è che, per la maggior parte di questi disturbi, i precisi percorsi molecolari che dovremmo prendere di mira per lo sviluppo di farmaci rimangono poco chiari”, ha affermato Michael Ward, co-autore senior autore del nuovo studio e medico-scienziato presso il National Institutes of Health.
“Con questa tecnologia, possiamo prendere le cellule della pelle o le cellule del sangue da un paziente con una malattia neurodegenerativa come l’Alzheimer, trasformarle in neuroni o altre cellule cerebrali e capire quali geni controllano i difetti cellulari associati alla malattia”, ha affermato Kampmann. “Queste informazioni possono permetterci di identificare obiettivi terapeutici efficaci“.
Fonte, Neuron