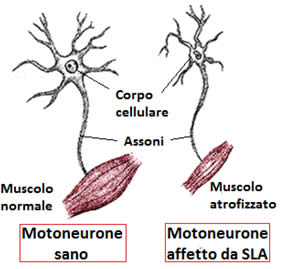
L‘integrazione di una singola proteina trovata nel midollo spinale potrebbe aiutare a prevenire i sintomi della SLA, secondo un nuovo studio della Scuola di Medicina della Case Western Reserve University. I ricercatori hanno trovato che alti livelli della proteina – chiamata mitofusione 2 o Mfn2 – prevengono la degenerazione dei nervi, l’atrofia muscolare e la paralisi in un modello murino della malattia, poichè Mfn2 è spesso esaurita nella malattia. Il nuovo studio potrebbe portare ad un nuovo approccio terapeutico per la malattia.
La malattia di Lou Gehrig o sclerosi laterale amiloide (SLA), è un disturbo progressivo che devasta le cellule nervose del motoneurone. Le persone con SLA perdono lentamente la capacità di controllare i movimenti dei muscoli e alla fine non sono in grado di parlare, mangiare, muoversi o respirare. I meccanismi cellulari alla base della SLA si trovano anche in alcuni tipi di demenza. Per i circa 15.000 americani che vivono con la SLA, i risultati di questo studio offrono nuove speranze per ritardare i sintomi della malattia.
“Abbiamo trovato un modo per alleviare l’atrofia muscolare legata alla SLA e all’età, nei nostri modelli murini”, ha detto Xinglong Wang, Professore associato di patologia presso la Case Western Reserve University School of Medicine. “Sorprendentemente, potremmo ritardare l’insorgenza dei sintomi della SLA di 67 giorni”.
Nello studio, condotto da Wang e pubblicato oggi su Cell Metabolism, i ricercatori hanno superato con successo l’atrofia muscolare e la paralisi semplicemente aumentando i livelli di Mfn2 nel midollo spinale.
( Vedi anche:Nuova tecnica aiuta a scoprire i cambiamenti nei neuroni della SLA).
Wang e colleghi hanno testato il modello di topo SLA più utilizzato. Hanno ingegnerizzato geneticamente i topi malati per aumentare i livelli di Mfn2 – ma solo nelle cellule nervose che si estendono dal midollo spinale e si collegano alle fibre muscolari. Negli stadi avanzati della malattia, i topi con alti livelli di Mfn2 in questi nervi, erano di peso sano e non presentavano alcuna atrofia muscolare, anomalie dell’andatura o ridotta forza di presa sviluppata da topi nel gruppi di controllo. Persino i topi sottoposti a pesanti danni al nervo sciatico hanno beneficiato di elevati livelli di Mfn2.
Ha detto Wang, “L’upregulation di Mfn2 specificamente nelle cellule nervose è sufficiente per abolire la perdita di muscolo scheletrico nella SLA e nei topi anziani, nonostante la proteina che causa la SLA sia stata trovata in tutti gli organi e tessuti“.
Studiando le cellule nervose raccolte dai topi, la squadra di Wang ha scoperto come Mfn2 offre i suoi effetti protettivi. I ricercatori hanno scoperto che Mfn2 coesiste con sostanze nutritive nelle strutture cellulari chiamate mitocondri. I loro esperimenti hanno mostrato che i mitocondri viaggiano lungo le estensioni delle cellule nervose – gli assoni – e forniscono i nutrienti al punto in cui le cellule nervose e le fibre muscolari si incontrano. Ciò preserva le connessioni sensibili – sinapsi – tra le cellule nervose e muscolari e previene l’atrofia muscolare. ” I mitocondri sono come” camion in miniatura” che trasportano proteine lungo gli assoni per prevenire la degenerazione sinaptica”, ha spiegato Wang.
Il trasporto cellulare non è in genere nella descrizione del lavoro dei mitocondri. Le antiche strutture cellulari sono ben note per essere “centrali elettriche della cellula” , producendo energia che mantiene in funzione le cellule. Secondo Wang, “questo è un ruolo nuovo precedentemente non riconosciuto, dei mitocondri”.
In particolare, il team di Wang ha scoperto che i mitocondri utilizzano Mfn2 sulle loro superfici per trasportare un nutriente chiamato calpstatina. La calpstatina inibisce gli enzimi dannosi che distruggono i nervi e le fibre muscolari. Con l’aiuto di Mfn2, i mitocondri trasportano la calpstatina lungo gli assoni delle cellule nervose per incontrare le cellule muscolari. Lì, calpstatina impedisce agli enzimi di distruggere le delicate connessioni sinaptiche. Ma senza Mfn2, i mitocondri non possono trasportare la sostanza nutritiva.
Secondo Wang, i risultati di questo studio hanno ampie implicazioni. “La deficienza o le mutazioni di Mfn2 sono comunemente osservate in pazienti con SLA, neuropatia periferica, morbo di Alzheimer e altre malattie neurodegenerative in cui la perdita sinaptica è stata a lungo riconosciuta come una caratteristica preminente”, dice il ricercatore “L’integrazione di Mfn2 può essere un approccio terapeutico comune ed efficace per il trattamento di una vasta gamma di patologie, inclusi i disturbi muscolari, i pazienti con danno nervoso e le varie principali malattie neurodegenerative associate alla perdita sinaptica”.
Fonte: Case Western Reserve