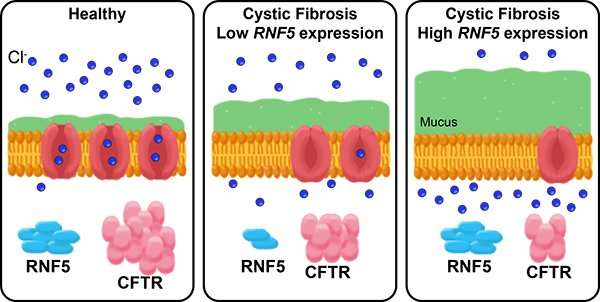
Immagine, Nelle persone sane, la proteina CFTR è incorporata nella membrana della maggior parte delle cellule, dove forma un canale per gli ioni cloro. Nelle persone con fibrosi cistica, una mutazione ereditaria nel gene CFTR significa che i loro canali non funzionano altrettanto bene e le cellule producono più muco. La proteina RNF5 inibisce la CFTR, quindi le persone con fibrosi cistica che hanno variazioni genetiche che riducono l’espressione di RNF5 hanno canali CFTR che funzionano un po’ meglio e per questo non sono inclini alle infezioni come le persone con alta espressione di RNF5. Credito: UC San Diego Health Sciences.
La fibrosi cistica è causata da una mutazione ereditaria nel gene CFTR. A causa di questa mutazione, la proteina CFTR non si incorpora nelle membrane cellulari per formare un canale per gli ioni cloro come dovrebbe. Di conseguenza, le cellule che producono muco secernono un muco più spesso del normale che può creare blocchi nei polmoni e nel sistema digestivo. Nei polmoni, questo muco spesso può aiutare i batteri a prosperare, rendendo le infezioni polmonari un problema grave e cronico per molte persone che vivono con fibrosi cistica.
Eppure alcune persone con fibrosi cistica non sviluppano infezioni polmonari frequentemente quanto le altre. I ricercatori della School of Medicine dell’Università di California di San Diego hanno recentemente scoperto che le variazioni genetiche che smorzano l’espressione di un altro gene, chiamato RNF5, offrono una probabile spiegazione.
Nello studio, pubblicato il 10 dicembre 2019 su eLife, il team ha scoperto che le persone con fibrosi cistica che presentano varianti genetiche specifiche che abbassano l’espressione di RNF5, hanno più proteine CFTR mutanti sulla loro superficie cellulare. “Anche se la proteina CFTR non è totalmente funzionale, è probabilmente meglio che non averne affatto”, hanno detto i ricercatori.
I sintomi della fibrosi cistica possono essere significativamente migliorati con farmaci relativamente nuovi che aumentano la funzione di CTFR, ma ci sono due avvertimenti: i farmaci sono estremamente costosi e non funzionano per tutti.
“La ricerca sulla fibrosi cistica sta cercando di capire quali sono i geni modificatori che attraverso il genoma geni aumentano o diminuiscono la probabilità che un singolo paziente risponderà a questi farmaci costosi”, ha affermato l’autore senior Kelly A. Frazer, Ph.D., Professore di pediatria e Direttore dell’Institute for Genomic Medicine della UC San Diego School of Medicine. “RNF5 può essere uno di questi geni modificatori”.
Vedi anche, Approvato nuovo farmaco per la fibrosi cistica.
Il gene RNF5 si trova nel complesso maggiore di istocompatibilità (MHC, un gruppo di geni polimorfici costituito da 30 unità, localizzato sul braccio corto del cromosoma 6. I geni in questa regione codificano molecole che vengono visualizzate sulla superficie della maggior parte delle cellule del corpo. Giocano un ruolo importante nel modo in cui il corpo risponde alle infezioni. Gli scienziati sanno da tempo che ognuno ha il proprio set di variazioni geniche MHC e che rende le persone più o meno sensibili alle infezioni o alle malattie autoimmuni. Ma poiché i geni presenti nella regione MHC sono così densi di variazioni, non sono stati ben studiati per il loro legame diretto con le malattie.
Frazer e colleghi hanno adottato un nuovo approccio per analizzare le varianti del gene MHC raggruppandole. Ciò ha permesso al team di identificare più facilmente le associazioni tra variazione genetica, livelli di espressione genica e i loro effetti su malattie complesse. I ricercatori hanno applicato questo approccio al sequenziamento dell’intero genoma delle cellule staminali pluripotenti indotte derivate da 419 persone. Ciò si è tradotto nell’indagine su oltre 4.000 tratti, dai quali i ricercatori hanno identificato 180 varianti nella regione MHC.
“Abbiamo scoperto che esiste un’associazione tra geni MHC e colonizzazione batterica nei pazienti con fibrosi cistica, ma nessuno sapeva perché”, ha detto Frazer. “Abbiamo supposto che questo fosse dovuto al coinvolgimento di MHC nel sistema immunitario. Ma ora sappiamo che probabilmente non è l’unico meccanismo: anche diversi livelli di espressione di RNF5 possono svolgere un ruolo importante”.
“Questo studio ha rivelato un nuovo aspetto della fibrosi cistica, un aspetto che potrebbe portare alla progettazione e allo sviluppo di nuovi farmaci e consentire ai clinici di migliorare i trattamenti su misura per questa condizione”, ha affermato il primo autore Matteo D’Antonio, Ph.D., scienziato nel laboratorio di Frazer . “Ma questo è solo un esempio di come potremmo impiegare questa nuova tecnica di analisi genetica. Ora abbiamo una road map e possiamo applicarla ad altre malattie e tipi di cellule”.
Fonte, eLife