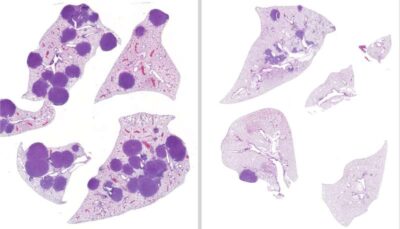
Tumore polmonare-Immagine: a sinistra: tessuto polmonare di topi con carcinoma polmonare non a piccole cellule con mutazione LKB1. A destra: tessuto polmonare dopo essere stato trattato sia con Trametinib che con Entinostat che mostra tumori più piccoli e meno numerosi. Credito: Salk Institute
I trattamenti contro il cancro si stanno da tempo muovendo verso la personalizzazione, trovando i farmaci giusti che funzionano per il tumore unico di un paziente, sulla base di specifici modelli genetici e molecolari. Molte di queste terapie mirate sono altamente efficaci, ma non sono disponibili per tutti i tumori, compresi i tumori polmonari non a piccole cellule (NSCLC) che hanno una mutazione genetica LKB1.
Un nuovo studio condotto dal Professor Reuben Shaw del Salk Institute e dall’ex borsista postdottorato Lillian Eichner, ora assistente Professore alla Northwestern University, ha rivelato che Trametinib ed Entinostat approvati dalla FDA (che è attualmente in sperimentazione clinica) possono essere somministrati in tandem per produrre meno e più piccoli tumori nei topi con NSCLC LKB1-mutato.
I risultati dello studio sono stati pubblicati su Science Advances il 17 marzo 2023.
“Per i casi di carcinoma polmonare non a piccole cellule con la mutazione LKB1, i trattamenti standard di chemioterapia e immunoterapia non sono efficaci”, afferma Shaw, autore senior e co-corrispondente dello studio e Direttore del Salk’s Cancer Center. “I nostri risultati dimostrano che esiste un modo per colpire questi casi utilizzando farmaci approvati dalla FDA o già in sperimentazione clinica, quindi questo lavoro potrebbe essere facilmente utilizzato per una sperimentazione clinica sugli esseri umani“.
Circa il 20% di tutti i tumori NSCLC ha la mutazione genetica LKB1, il che significa che attualmente non esistono terapie mirate efficaci sul mercato per i pazienti con questo tipo di cancro. Per creare una terapia che potesse mirare alla mutazione LKB1, i ricercatori si sono rivolti all’istone deacetilasi (HDAC). Gli HDAC sono proteine associate alla crescita del tumore e alla metastasi del cancro, con caratteristica sovraespressione nei tumori solidi.
Diversi farmaci inibitori dell’HDAC sono già approvati dalla FDA (sicuri per uso umano) per forme specifiche di linfoma, ma mancano dati sulla loro efficacia nei tumori solidi o se i tumori portatori di specifiche alterazioni genetiche possano mostrare un potenziale terapeutico accresciuto.
Sulla base di precedenti scoperte che collegano il gene LKB1 ad altri tre HDAC che si basano tutti su HDAC3, il team ha iniziato conducendo un’analisi genetica di HDAC3 in modelli murini di NSCLC, scoprendo un ruolo inaspettatamente critico per HDAC3 in più modelli. Dopo aver stabilito che l’HDAC3 era fondamentale per la crescita dei tumori mutanti LKB1 difficili da trattare, i ricercatori hanno successivamente esaminato se il blocco farmacologico dell’HDAC3 potesse avere un effetto altrettanto potente.
Il team era curioso di testare due farmaci, Entinostat (un inibitore HDAC negli studi clinici noto per colpire HDAC1 e HDAC3) e Trametinib approvato dalla FDA (un inibitore per una diversa classe di enzimi correlati al cancro). I tumori spesso diventano rapidamente resistenti al Trametinib, ma il co-trattamento con un farmaco che inibisce una proteina a valle dell’HDAC3 aiuta a ridurre questa resistenza.
Poiché quella proteina si basa sull’HDAC3, i ricercatori ritenevano che un farmaco che prende di mira l’HDAC3, come Entinostat, avrebbe aiutato anche a gestire la resistenza al Trametinib.
Dopo aver trattato i topi con carcinoma polmonare LKB1-mutato con regimi di trattamento variabili per 42 giorni, il team ha scoperto che i topi trattati sia con Entinostat che con Trametinib avevano il 79% in meno di volume tumorale e il 63% in meno di tumori nei polmoni rispetto ai topi non trattati. Inoltre, il team ha confermato che Entinostat era un’opzione terapeutica praticabile nei casi in cui un tumore era resistente a Trametinib.
“Pensavamo che l’intera classe di enzimi HDAC fosse direttamente collegata alla causa del carcinoma polmonare mutante LKB1. Ma non conoscevamo il ruolo specifico dell’HDAC3 nella crescita del tumore polmonare”, afferma il primo autore e co-corrispondente Eichner. “Ora abbiamo dimostrato che l’HDAC3 è essenziale nel cancro del polmone e che è una vulnerabilità farmacologica nella resistenza terapeutica“.
Vedi anche:Il blocco del metabolismo dello zucchero rallenta la crescita del tumore polmonare
I risultati potrebbero portare a studi clinici per testare il nuovo regime negli esseri umani, poiché Entinostat è già in sperimentazione clinica e Trametinib è approvato dalla FDA. È importante sottolineare che Shaw vede questa scoperta come trasformativa per i tumori oltre il NSCLC, con potenziali applicazioni nel linfoma, nel melanoma e nel cancro del pancreas .
“Il nostro laboratorio ha dedicato anni a questo progetto, compiendo piccoli e significativi passi verso questi risultati”, afferma Shaw, titolare della William R. Brody Chair. “Questa è davvero una storia di successo per come la scienza di base può portare a soluzioni terapeutiche in un futuro non così lontano“.
“Il mio laboratorio indipendente ha la fortuna di far parte del Lurie Cancer Center presso la Feinberg School of Medicine della Northwestern University, che sostiene molto la ricerca traslazionale. Ci auguriamo che questo ambiente faciliti l’avvio di una sperimentazione clinica basata su questi risultati”, dice Eichner.
Fonte:Science Advances