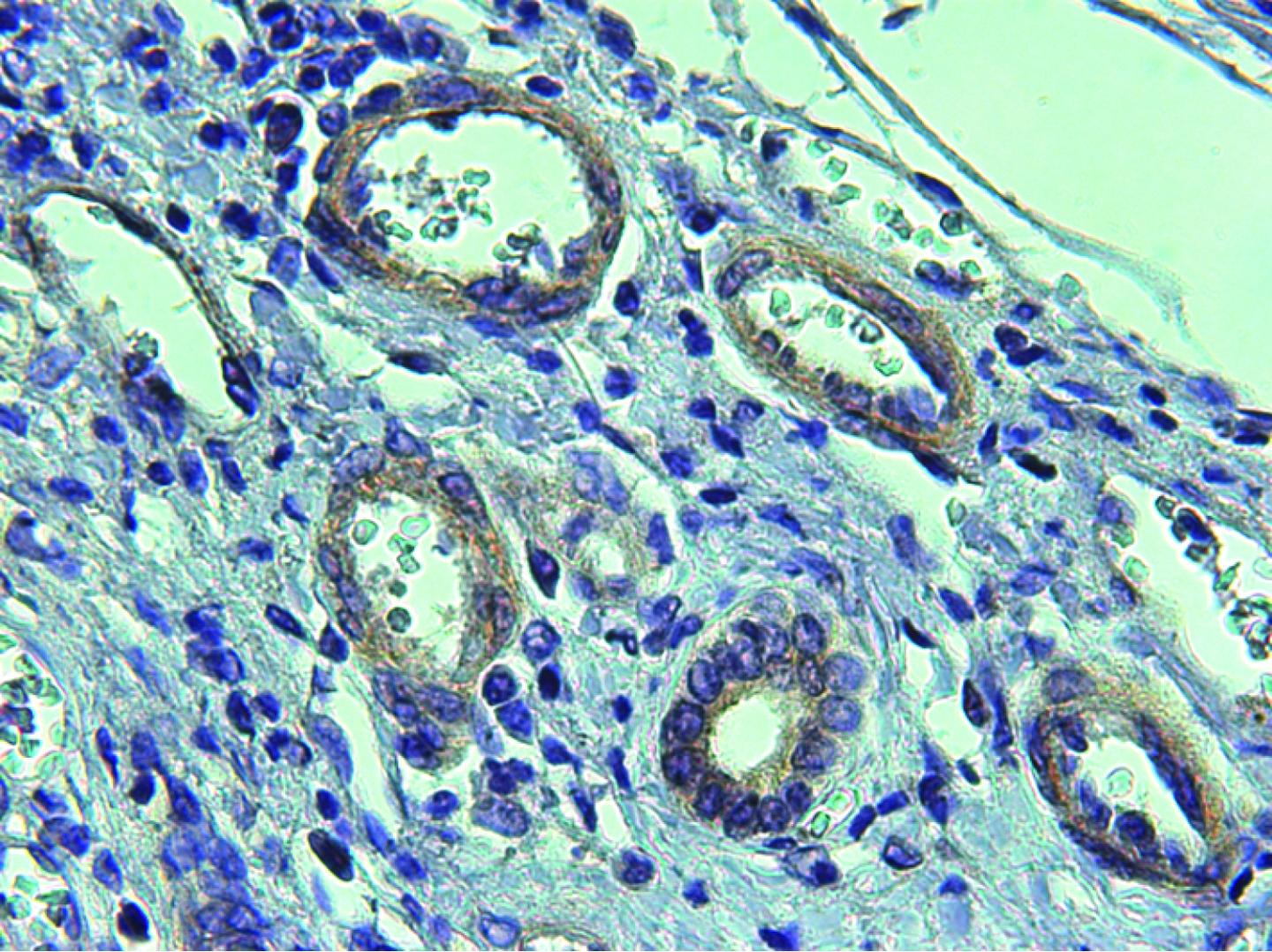
Immagine: i vasi sanguigni patologici (cerchi bianchi) hanno abbondante espressione CPEB4 nel tessuto cirrotico. Credit:(IRBBARCELONA / IDIBAPS)
Gli scienziati, guidati da Raúl Méndez, Professore di ricerca presso l’Istituto di ricerca in biomedicina (IRB Barcellona) e da Mercedes Fernández della IDIBAPS a Barcellona, hanno rivelato che l’inibizione della proteina CPEB4 può impedire lo sviluppo dei vasi sanguigni anomali associati alla cirrosi.
L’angiogenesi patologica è una delle più gravi complicazioni nei pazienti con cirrosi e un fattore chiave per lo sviluppo e peggioramento della malattia. Di conseguenza, molti sforzi di ricerca si concentrano sull’identificazione di trattamenti per questa condizione.
I risultati dello studio sono stati pubblicati nel numero più recente di Gastroenterology.
Nei paesi occidentali, la cirrosi è tra le 10 principali cause di morte tra gli adulti. Si tratta di una malattia molto comune in Spagna e la principale causa di trapianto di fegato in questo paese. E’ responsabile di un alto tasso di ricoveri ospedalieri e di uso delle risorse sanitarie a causa di complicazioni che si verificano nelle fasi avanzate della malattia.
Effetto perverso della riparazione
La cirrosi è una lesione cronica caratterizzata da accumulo di tessuto cicatriziale (noduli fibrosi), che altera la normale struttura e funzione dell’organo. Lesioni epatiche croniche sono causate principalmente da alcolismo, epatite C e sempre più da obesità.
L’accumulo di tessuto cicatriziale ostacola la circolazione del sangue nel fegato, portando così a ipertensione portale (la vena porta). Per alleviare la pressione nella vena, vasi sanguigni collaterali, si sviluppano al di fuori del fegato. Il problema è quindi duplice, in primo luogo perché il fegato riceve ancor meno sangue che causa così un danno maggiore all’organo e in secondo luogo, perché i vasi sanguigni sono di scarsa qualità (angiogenesi patologica).
“Le cellule epatiche tentano di riparare le lesioni al fegato, ma il modo con cui esse lo fanno, risulta essere fatale per l’organo. Inoltre, i vasi sanguigni formano varici nell’esofago e nello stomaco dei pazienti con cirrosi; queste vene sono fragili e hanno una elevata tendenza a scoppiare, provocando forti emorragie che sono difficili da fermare “, spiega Mercedes Fernández della IDIBAPS e co-leader dello studio. “È per questo che un trattamento che regredisce e / o previene le vene patologiche – che non è attualmente disponibile – sarebbe efficace per trattare la condizione”, aggiunge.
Un obiettivo di nome CPEB4
VEGF (fattore di crescita endoteliale vascolare) è la principale proteina effettore nello sviluppo dei vasi sanguigni. “Tutti i farmaci attuali che mirano a prevenire la neovascolarizzazione hanno come obiettivo inibire recettori di VEGF, ma il problema è che l’attacco indiscriminato di questa proteina compromette il normale sviluppo dei vasi sanguigni, causando effetti avversi intollerabili”, spiega Méndez, da IRB Barcellona.
In un precedente studio pubblicato su Nature Medicine, Méndez, insieme con i ricercatori dell’Ospedale del Mar a Barcellona, aveva già scoperto che le proteine CPEB sono coinvolte nello sviluppo dei vasi sanguigni nel pancreas e cancro al cervello. Data l’urgente necessità di identificare nuovi bersagli per l’angiogenesi patologica, Méndez e Fernández hanno iniziato a collaborare per esaminare il ruolo di CPEB4 in questo processo, nel contesto della cirrosi, una malattia caratterizzata da una profonda neovascolarizzazione.
“Lo studio ha dimostrato che lo sviluppo patologico dei vasi sanguigni può essere fermato interferendo con le proteine CPEB4, mentre la vascolarizzazione positiva rimane intatta”, dice Méndez. Gli esperimenti in cellule in vitro, in modelli animali e in campioni prelevati da pazienti con cirrosi, hanno rivelato i meccanismi molecolari attraverso i quali l’aumento di CPEB4 favorisce la sovraespressione di VEGF nella cirrosi.
Dalla cirrosi al cancro del fegato
I ricercatori sostengono che il ciclo di riparazione che il fegato mette in atto, peggiora la situazione nella misura in cui i noduli di rigenerazione, che mostrano alti livelli di CPEB4, formano carcinomi epatici. In questo contesto, l’Associazione Spagnola contro il Cancro (Asociación Española Contra el cancro (AECC)) ha assegnato più di un milione di euro alla ricerca di Méndez-Fernández, che, insieme con Jordi Bruix (IDIBAPS-Hospital Clinic), lavorerà per chiarire il ruolo di questa molecola e proporre un trattamento per carcinomi del fegato che rappresentano la terza causa di morte per cancro in tutto il mondo, con un tasso di sopravvivenza a 5 anni inferiore al 10%.
Contemporaneamente, il laboratorio di Méndez a IRB Barcellona, sta lavorando ad un progetto di ricerca sugli inibitori CPEB4. L’anno scorso i ricercatori hanno risolto le strutture di queste proteine a livello atomico. Il passo seguente sarà la progettazione computazionale di inibitori, che verrà svolta in collaborazione con Modesto Orozco, nello stesso centro. Inoltre, con il supporto della Fondazione Botín, Méndez ha messo a punto un saggio per testare inibitori CPEB4, allo scopo di accelerare la rilevazione di molecole con maggiori potenzialità terapeutiche.
Fonte: http://www.alphagalileo.org/ViewItem.aspx?ItemId=159307&CultureCode=en