La decrescente efficacia dei farmaci nel tempo continua a rappresentare una grande sfida nel trattamento delle malattie, tra cui l’asma.
Nel tentativo di trovare trattamenti precisi con un minor numero di effetti collaterali, Stephen B. Liggett, MD e colleghi della University of South Florida Health (USF Health) Morsani College of Medicine hanno esaminato come le variazioni strutturali distinte di cinque farmaci (chiamati agonisti) potrebbero influenzare a lungo termine, il trattamento dell’ostruzione delle vie aeree nell’asma. I ricercatori hanno studiato come ciascuno dei cinque farmaci regolasse un recettore del gusto amaro noto come TAS2R14, un recettore accoppiato con proteina G (GPCR) espresso sulla muscolatura liscia delle vie aeree umane, in profondità all’interno dei polmoni.
Lo studio preclinico USF Health è stato pubblicato online il 20 agosto sul The FASEB Journal.
L’attuale studio si basa sul precedente lavoro dell’autore senior Dr. Liggett, che dimostra che gli agonisti del recettore del gusto amaro sembrano superiori ai beta-agonisti per inalazione attualmente prescritti per aprire le vie aeree agli asmatici. Nel documento, il team di ricerca interdisciplinare della USF Health riporta che un farmaco — Difenidramina (DPD), un agonista TAS2R14 — ha funzionato significativamente meglio di altri quattro per ridurre al minimo la perdita a lungo termine dell’espressione di TAS2R14 e mantenere la segnalazione necessaria per dilatare le vie aeree a lungo termine.
“L’obiettivo di questo studio era vedere quanto bene i farmaci mirati a TAS2R14 che abbiamo selezionato interagivano con il recettore per mantenere il segnale che rilassa la muscolatura liscia delle vie aeree, senza perdere questa funzione terapeutica nel tempo”, ha affermato il Dott. Liggett, vicePreside della ricerca presso la USF Health Morsani College of Medicine e Professore di medicina interna, farmacologia e fisiologia molecolare e ingegneria medica. “Siamo i primi a dimostrare che è possibile influenzare l’attivazione di GPCR delle vie aeree con un farmaco con risultato terapeutico molto favorevole”.
“Quel risultato – miglioramento del flusso d’aria anche con dosi ripetitive – indica la capacità di ottenere un migliore controllo continuo dell’asma da moderata a grave”, ha aggiunto il ricercatore.
” Abbiamo bisogno di farmaci in grado di aprire direttamente le vie aeree per curare un attacco acuto, chiamati farmaci di salvataggio, così come di quelli per prevenire gli attacchi, noti come farmaci controllori. Ma tutti questi farmaci sono attualmente beta-agonisti”, ha spiegato il Dr. Liggett. “Abbiamo intrapreso la ricerca di farmaci che attivano percorsi completamente diversi, in modo che possano integrare o sostituire i farmaci attuali“.
“Quando l’efficacia di un farmaco diminuisce, poche opzioni sono disponibili”, ha detto il ricercatore. “A volte può essere d’aiuto una dose più alta o una dose più frequente, ma ciò può portare a una più bassa regolazione della risposta e creare un circolo vizioso. Il dosaggio accelerato può anche causare effetti collaterali maggiori“.
I GPCR sono recettori di membrana cellulare che ricevono informazioni da altre molecole esterne alla cellula, compresi i farmaci. Questi recettori segnalano all’interno della cellula di svolgere una o più funzioni. Nel caso del recettore del gusto amaro TAS2R14, l’attivazione del recettore innesca il rilassamento delle vie aeree ristrette.
Vedi anche, I ricercatori scoprono la causa del broncospasmo negli asmatici.
Tuttavia, dopo l’esposizione prolungata a un farmaco, TAS2R14 e molti altri GPCR, riducono la loro risposta fisiologica al farmaco che si lega e li attiva. Questa “desensibilizzazione” significa che la stessa dose di farmaco che originariamente funzionava bene, non lo fa più. Il processo comporta una cascata di eventi, tra cui una riduzione del numero di recettori sulla superficie della membrana cellulare bersaglio e un’interruzione della segnalazione cellulare, il che porta a un trattamento meno efficace.
I ricercatori della USF Health hanno creato un modello cellulare di cellule muscolari lisce delle vie aeree umane vive per studiare cinque agonisti TAS2R14 strutturalmente distinti, inclusi farmaci con proprietà antisettiche, antinfiammatorie, di dilatazione dei vasi e antidolorifici. Hanno esaminato quali farmaci hanno dimostrato distorsione dalla desensibilizzazione (non promossa) di TAS2R14, ma hanno comunque attivato questo recettore del gusto amaro.
Hanno anche usato un modello al computer noto come docking molecolare per aiutare a identificare il motivo per cui il farmaco DPD interagiva con i siti di legame TAS2R14 in modo diverso rispetto alla maggior parte degli altri farmaci.
Tra alcuni dei risultati chiave dello studio:
- Il recettore del gusto amaro TAS2R14 è stato esposto a tutti e cinque i farmaci per 18 ore. Solo la DPD ha mostrato una desensibilizzazione minima dopo un trattamento a lungo termine.
- Tutti i farmaci tranne DPD hanno indotto i recettori sulla superficie delle cellule muscolari lisce delle vie aeree a spostarsi all’interno della cellula dove alla fine vengono degradati. Ciò lascia un minor numero di recettori sulla superficie cellulare per interagire con il farmaco, quindi la risposta globale al trattamento diminuisce.
- L’aggancio molecolare ha dimostrato che DPD aveva punti di contatto profondi all’interno della tasca di legame del recettore non osservati con gli altri quattro farmaci. Come ulteriore test, anche un sesto composto (Orfenadrina) strutturalmente simile a DPD è stato ancorato al TAS2R12. Come DPD, Orfenadrine si è conformato agli stessi punti di contatto sul recettore senza down-regolazione del recettore. “ Un “migliore adattamento” dell’agonista al recettore del gusto amaro può stabilizzare la forma del recettore in modo da favorire una risposta ottimale del farmaco, evitando tuttavia la down-regolazione (e accompagnando la perdita di recettori )”, suggeriscono i ricercatori.
“Nel complesso, la nuova ricerca suggerisce che la manipolazione della struttura dei farmaci esistenti o la scoperta di nuovi farmaci con caratteristiche strutturali che meglio si adattano alla forma unica del recettore mirato, possono promuovere il controllo a lungo termine dell’asma difficile da trattare”, ha affermato il Dott. Liggett.
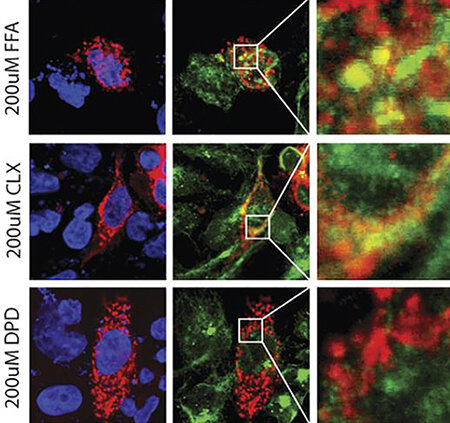
Immagine: immagini confocali fluorescenti ad alta risoluzione che mostrano cellule lisce delle vie aeree umane esposte a tre diversi farmaci nell’arco di 15 ore: il farmaco difenidramina (DPD), riga inferiore, mantiene più recettori del gusto amaro TAS2R14 (rosso) sulla superficie cellulare, subendo un minore degrado rispetto ai recettori, interagendo con i farmaci clorexidina (CLX) e flufenamic (FFA). Il giallo più pronunciato nelle cornici centrale e in alto a destra rappresenta la co-localizzazione del recettore (rosso) e un marcatore endosomiale (verde), il che significa che i recettori che si legano a CLX e FFA sono già stati presi all’interno delle cellule e sono su un percorso verso il degrado. Credito:Centro Byrd Alzheimer dell’Università della Florida meridionale.
Fonte, The FASEB Journal