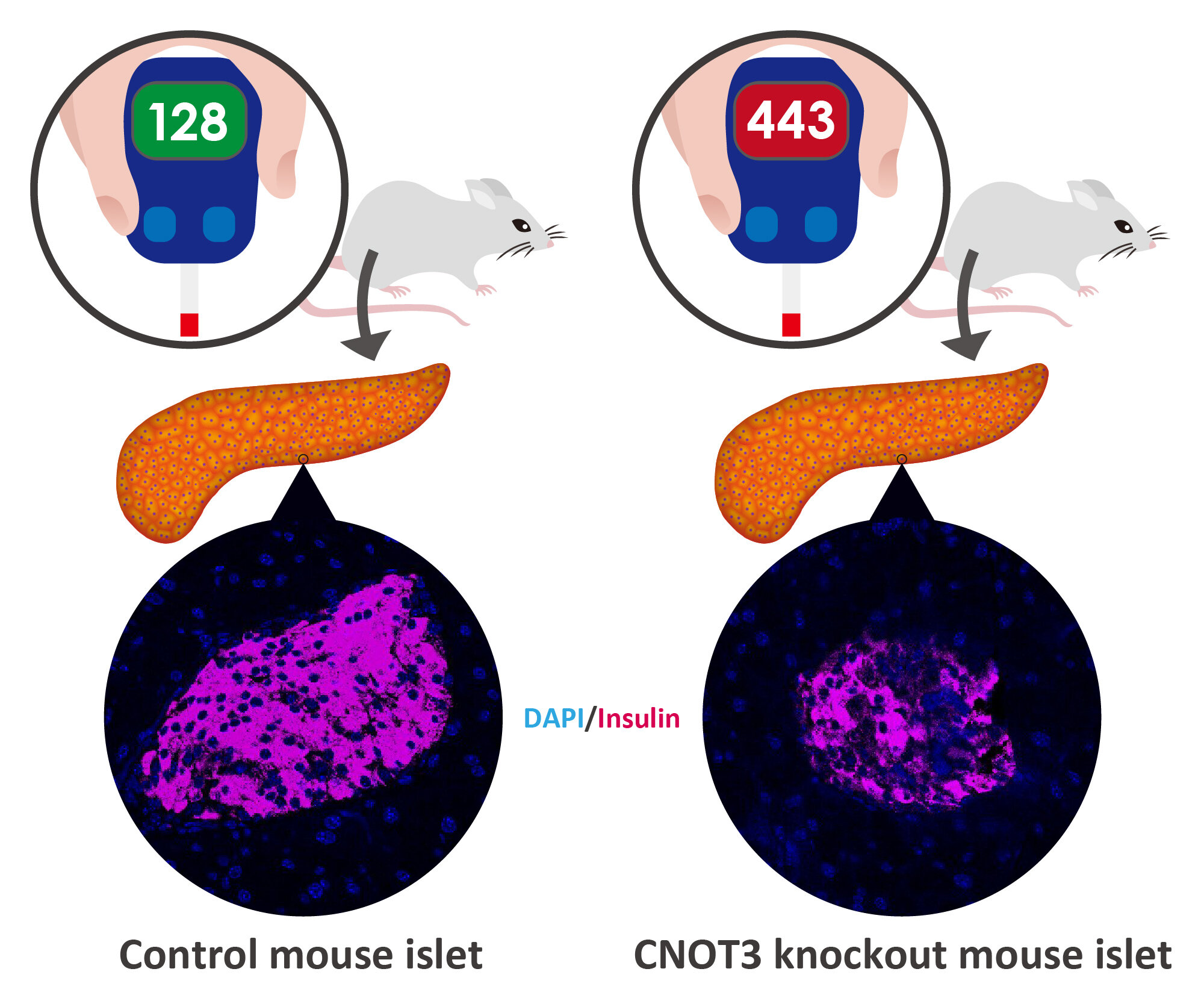
Immagine: i topi privi di CNOT3 nelle cellule beta pancreatiche hanno un minor numero di cellule produttrici di insulina che porta al diabete. Credito: OIST.
“Una proteina comune in tutto il corpo svolge un ruolo chiave nella regolazione dei livelli di glucosio e nel diabete”, afferma una nuova ricerca condotta nella Cell Signal Unit presso l’Okinawa Institute of Science and Technology Graduate University (OIST) e Riken Center of Integrative Medical Sciences. Chiamata CNOT3, questa proteina è stata trovata per silenziare un insieme di geni che altrimenti causerebbero il malfunzionamento delle cellule produttrici di insulina che è correlato allo sviluppo del diabete.
Il diabete è un disturbo comune che causa livelli di glucosio nel sangue molto alti . Se non trattata, la condizione può portare a gravi problemi di salute come insufficienza renale, malattie cardiache e perdita della vista. Questo disturbo si verifica quando non c’è abbastanza insulina nel corpo o quando le risposte indotte dall’insulina sono indebolite. L’insulina normalmente lascia il glucosio nelle cellule per uso energetico e quindi, senza di essa, il glucosio si accumula invece nel sangue. La mancanza di insulina è spesso dovuta al fatto che le cellule beta pancreatiche, che normalmente sintetizzano e secernono insulina, hanno smesso di funzionare correttamente.
“Sappiamo che i difetti nelle cellule beta possono portare ad alti livelli di glucosio nel sangue e, alla fine, al diabete”. ha detto la Dottoressa Dina Mostafa, ex Ph.D, studente dell’Unità e primo autore dell’articolo pubblicato su Communications Biology. “I nostri risultati suggeriscono che CNOT3 gioca un ruolo chiave nel mantenimento della normale funzione delle cellule beta”.
L’eliminazione di CNOT3 ha dimostrato di portare al diabete nei topi:
CNOT3 è un tuttofare. Molti organi in tutto il corpo la esprimono e regola diversi geni in diversi tessuti. Ma la sua attività ha una base comune: aiuta a mantenere le cellule vive, sane e funzionanti correttamente. Lo fa attraverso diversi meccanismi, come la produzione delle proteine giuste o la soppressione di determinati geni.
I ricercatori hanno studiato la sua funzione nelle cellule delle isole del tessuto pancreatico nei topi. Queste isole sono notoriamente difficili da studiare e occupano solo l’1-2% del pancreas.
Vedi anche: Prime cellule immunitarie create per il trattamento del diabete di tipo 1
I ricercatori hanno prima esaminato se l’espressione di CNOT3 fosse diversa nei topi diabetici rispetto ai topi non diabetici. Osservando queste isole, hanno scoperto che c’era una significativa diminuzione di CNOT3 nelle isole di Langerhans rispetto a quelle non diabetiche.
Per indagare ulteriormente sulla funzione della proteina, i ricercatori hanno bloccato la sua produzione nelle cellule beta di topi altrimenti normali. Per quattro settimane, il metabolismo degli animali ha funzionato normalmente, ma all’ottava settimana i topi avevano sviluppato un’intolleranza al glucosio e entro 12 settimane avevano il diabete in piena regola.
Senza CNOT3, i ricercatori hanno scoperto che alcuni geni, che normalmente sono disattivati nelle cellule beta, si accendono e iniziano a produrre proteine. In circostanze normali, questi geni vengono silenziati perché una volta attivati, causano tutti i tipi di problemi alle cellule beta, come impedire loro di secernere insulina in risposta al glucosio.
“Non sappiamo ancora molto su questi tipi di geni, quale sia la loro normale funzione e il meccanismo che è coinvolto nel loro silenziamento”, ha detto il Dottor Mostafa. “Quindi, è stato molto gratificante scoprire che CNOT3 è un fattore importante per tenerli spenti”.
La connessione con RNA messaggero
Ulteriori ricerche sui meccanismi cellulari hanno trovato un collegamento sorprendente tra CNOT3 e l’RNA messaggero di questi geni normalmente disattivati. Un RNA messaggero (mRNA) è una molecola a filamento singolo che corrisponde alla sequenza genetica di un gene ed è essenziale per la sintesi delle proteine.
In circostanze normali, l’mRNA di questi geni difficilmente si esprime. Ma una volta rimosso CNOT3, i ricercatori hanno scoperto che l’mRNA era molto più stabile. Infatti, la proteina è stata prodotta dall’mRNA stabilizzato, che ha effetti sfavorevoli sulla normale funzione dei tessuti. Ciò suggerisce che almeno un modo in cui questi geni vengono tenuti spenti è attraverso la destabilizzazione del loro mRNA, guidata da CNOT3.
“Questo studio è un passo verso la comprensione dei meccanismi molecolari che governano la normale funzione delle cellule beta“, ha detto il Dottor Mostafa. “In definitiva, potrebbe contribuire a nuovi modi di prevenire e curare il diabete”.
Fonte: Communications Biology