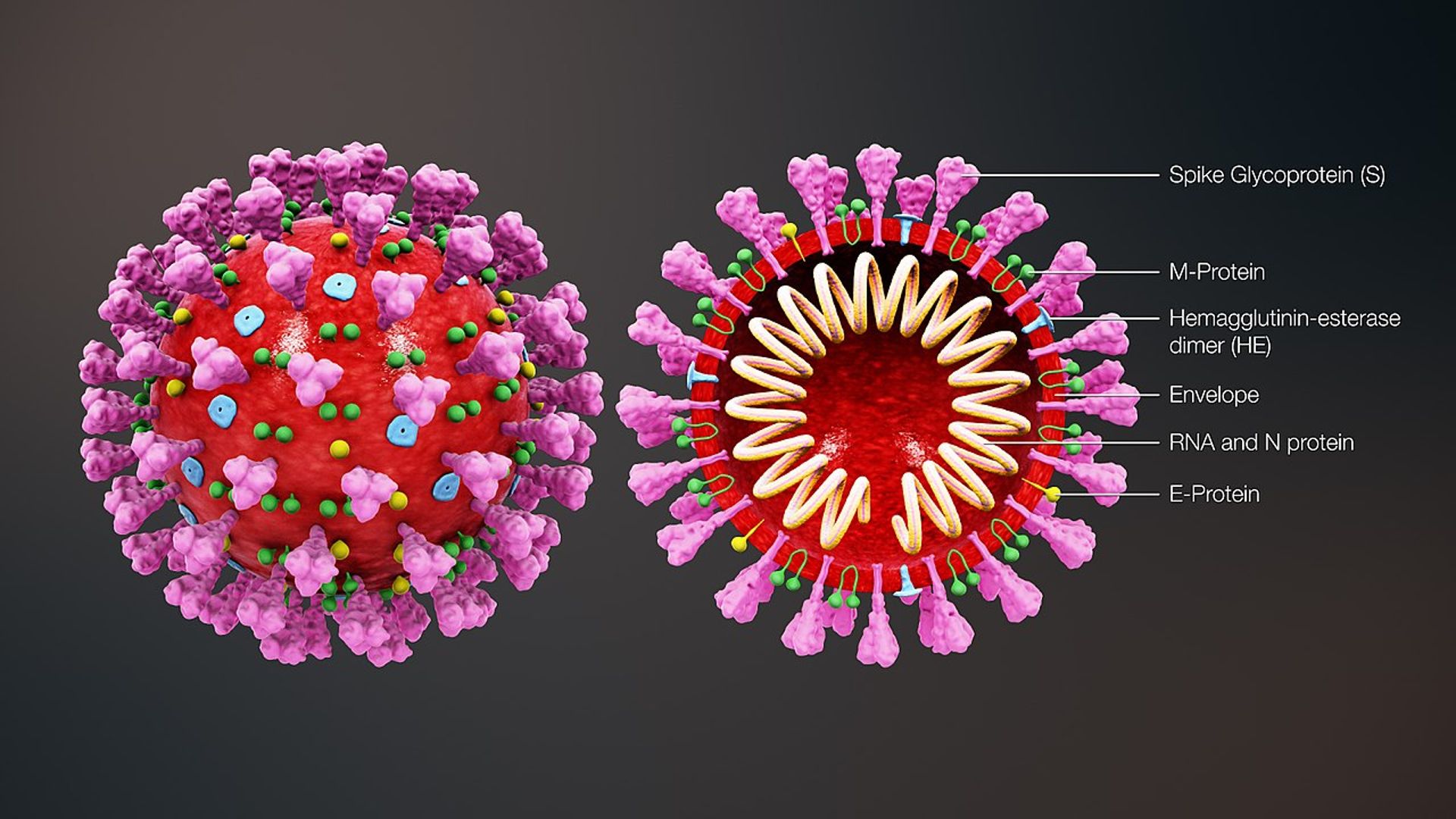
Immagine: Public Domain.
Ricercatori negli Stati Uniti e in Canada hanno progettato “trappole recettoriali” ottimizzate per l’affinità che impediscono al coronavirus SARS-CoV-2 di legarsi e infettare le cellule dell’ospite.
Affinché SARS-CoV-2 infetti le cellule umane e causi la malattia COVID-19, la proteina virale deve prima legarsi al dominio legante il recettore (RBD) dell’enzima 2 di conversione dell’angiotensina del recettore della membrana ospite (ACE2).
Ora James A. Wells (Università della California, San Francisco) e colleghi dell’Università di Alberta e della Rockefeller University hanno sviluppato varianti del dominio extracellulare ACE2 che impediscono a questa proteina spike di legare ACE2 e entrare nelle cellule ospiti.“Le trappole per recettori ACE2 ingegnerizzate offrono una strada promettente per combattere le infezioni da SARS-CoV-2 e altri coronavirus che utilizzano ACE2, con il vantaggio chiave che la resistenza virale potrebbe anche compromettere l’ingresso virale”, scrive il team.
I ricercatori affermano che le trappole possono essere progettate per virus con recettori delle cellule ospiti conosciuti per fornire risposte terapeutiche rapide, senza neutralizzare gli anticorpi che devono essere isolati dai pazienti che si sono ripresi dall’infezione.
Una versione prestampata del documento è disponibile nel server bioRxiv * , mentre l’articolo è sottoposto a revisione paritaria.
Molti team di ricerca si sono concentrati sulla neutralizzazione degli anticorpi
A seguito dell’infezione da SARS-CoV-2, la maggior parte degli anticorpi neutralizzanti generati ha impedito al virus di entrare nelle cellule legandosi all’RBD su ACE2.
Data l’urgente necessità di trattamenti efficaci durante l’attuale pandemia di COVID-19, molti ricercatori si sono concentrati sui modi per generare anticorpi ricombinanti che possono bloccare questa entrata virale.
Vedi anche: Una proteina dei fagioli Lablab blocca efficacemente le infezioni da virus influenzali e SARS-CoV-2
Sia gli anticorpi ingegnerizzati che quelli isolati dal sangue dei pazienti guariti hanno dimostrato di essere efficaci approcci terapeutici nelle precedenti pandemie.
Tuttavia, tali strategie richiedono che una percentuale significativa della popolazione abbia sviluppato anticorpi protettivi a seguito di infezione e recupero, mentre la pandemia continua a spazzare il globo.
Gli approcci di ingegneria proteica possono offrire una “rapida alternativa”
“Gli approcci di ingegneria proteica per identificare i leganti alle proteine virali di ingresso offrono una rapida alternativa, senza i prerequisiti di una popolazione infetta”, hanno affermato Wells e colleghi.
Inoltre, le mutazioni che il virus può sviluppare possono impedire l’efficacia dei trattamenti anticorpali. “Allo stesso tempo, le mutazioni che riducono l’efficacia delle trappole del recettore ACE2 probabilmente comprometterebbero anche l’invasione virale”, aggiunge il team.
Tuttavia, ad oggi, non ci sono trappole per recettori approvate dalla FDA disponibili per l’uso come biologici antivirali, sebbene alcuni siano stati testati in studi clinici come trattamento per l’HIV.

Cosa hanno fatto i ricercatori?
Ora, ricercatori di Glasgow e colleghi hanno utilizzato un approccio di ingegneria proteica graduale per sviluppare varianti solubili inattivate del dominio extracellulare ACE2 che blocca potentemente il legame della proteina spike di SARS-CoV-2.
Innanzitutto, il team ha applicato approcci computazionali per progettare un’interfaccia ACE2-RBD che migliora l’affinità per l’RBD fino a 12 volte.
Successivamente, i ricercatori hanno scoperto ulteriori mutazioni che hanno portato a un’affinità di legame 14 volte maggiore per l’RBD, rispetto alla trappola del recettore “genitore” progettata computazionalmente.
Migliorare ulteriormente l’affinità di legame delle trappole recettoriali
Glasgow e colleghi affermano che l’affinità delle trappole per recettori ingegnerizzati è spesso migliorata attraverso la fusione con il dominio costante (Fc) dell’immunoglobulina ingegnerizzata dall’uomo.
Questa trappola del recettore ha efficacemente neutralizzato sia il lentivirus pseudotipo SARS-CoV-2 sia l’autentico SARS-CoV2, con una replicazione virale ridotta a livelli quasi impercettibili.
Un “percorso promettente” per combattere SARS-CoV-2
I ricercatori affermano che le trappole del recettore ACE2 che hanno progettato offrono una “via promettente” per combattere SARS-CoV-2.
“Le trappole per recettori ACE2 ingegnerizzati presentano vantaggi chiave nel trattamento delle infezioni da SARS-CoV-2”, scrive il team. “Questo approccio ha il potenziale vantaggio che la resistenza virale a una trappola del recettore ACE2 inibirebbe anche la capacità del virus di entrare nell’ospite attraverso il legame con il recettore di ingresso ACE2”.
Inoltre, tali trappole potrebbero essere utilizzate per colpire altri ceppi di varianti emergenti che utilizzano ACE2 come punto di accesso.
Il team sottolinea che un piccolo gruppo di ricerca ha raggiunto l’approccio di ottimizzazione dell’affinità in pochi mesi, in modo simile al tempo necessario per isolare gli anticorpi dai pazienti convalescenti o attraverso la selezione utilizzando metodi in vitro.
“Pertanto, questa strategia rappresenta un approccio rapido per la generazione di candidati terapeutici per il trattamento di future pandemie virali, senza alcun prerequisito da una popolazione umana infetta”, conclude il team.
Fonte: bioRxiv *