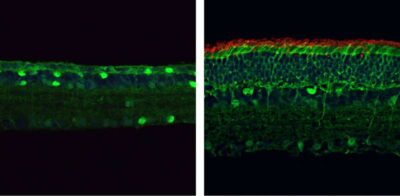
Retinite pigmentosa-Immagine: all’età di quattro mesi, le retine dei topi portatori di una mutazione nel gene che codifica per PDE6β (a sinistra) sono sottili e mancano di fotorecettori a bastoncino (rosso). Ma i topi che hanno avuto questa mutazione corretta attraverso il sistema PESpRY (a destra) hanno retine molto più spesse contenenti numerosi bastoncelli. Credito: © 2023 Qin et al. Originariamente pubblicato su Journal of Experimental Medicine . DOI: 10.1084/jem.20220776-
I ricercatori in Cina hanno ripristinato con successo la vista dei topi con retinite pigmentosa, una delle principali cause di cecità negli esseri umani. Lo studio, che è stato pubblicato il 17 marzo sul Journal of Experimental Medicine, utilizza una nuova forma altamente versatile di modifica del genoma basata su CRISPR con il potenziale per correggere un’ampia varietà di mutazioni genetiche che causano malattie.
I ricercatori hanno precedentemente utilizzato l’editing del genoma per ripristinare la visione di topi con malattie genetiche, come l’amaurosi congenita di Leber, che colpiscono l’epitelio pigmentato retinico, uno strato di cellule non neuronali nell’occhio che supporta le cellule dei fotorecettori dei coni e dei bastoncelli sensibili alla luce. Tuttavia, la maggior parte delle forme ereditarie di cecità, inclusa la retinite pigmentosa, sono causate da difetti genetici nei fotorecettori neurali stessi.
“La capacità di modificare il genoma delle cellule retiniche neurali, in particolare i fotorecettori malsani o morenti, fornirebbe prove molto più convincenti delle potenziali applicazioni di questi strumenti di modifica del genoma nel trattamento di malattie come la retinite pigmentosa“, afferma Kai Yao, Professore presso l’Università della Scienza e della Tecnologia di Wuhan.
La retinite pigmentosa può essere causata da mutazioni in oltre 100 geni diversi e si stima che comprometta la vista di 1 persona su 4.000. Inizia con la disfunzione e la morte dei bastoncelli sensibili alla luce fioca, prima di diffondersi ai coni necessari per la visione dei colori, portando infine a una perdita della vista grave e irreversibile.
Yao e colleghi hanno tentato di salvare la visione dei topi con retinite pigmentosa causata da una mutazione nel gene che codifica per un enzima critico chiamato PDE6β. Per fare questo, il team di Yao ha sviluppato un nuovo sistema CRISPR più versatile chiamato PE SpRY, che può essere programmato per correggere molti diversi tipi di mutazioni genetiche, indipendentemente da dove si verificano all’interno del genoma.
Vedi anche:Retinite pigmentosa: nuova speranza di trattamento
Quando è stato programmato per colpire il gene mutante PDE6β, il sistema PE SpRY è stato in grado di correggere efficacemente la mutazione e ripristinare l’attività dell’enzima nelle retine dei topi. Ciò ha impedito la morte dei fotorecettori di bastoncelli e coni e ha ripristinato le loro normali risposte elettriche alla luce.
Yao e colleghi hanno eseguito una serie di test comportamentali per confermare che i topi geneticamente modificati conservassero la vista anche in età avanzata. Ad esempio, gli animali sono stati in grado di trovare la via d’uscita da un labirinto d’acqua guidato visivamente quasi come topi normali e sani e hanno mostrato i tipici movimenti della testa in risposta agli stimoli visivi.
Yao avverte che c’è ancora molto lavoro da fare per stabilire sia la sicurezza che l’efficacia del sistema PE SpRY negli esseri umani. “Tuttavia, il nostro studio fornisce prove sostanziali dell’applicabilità in vivo di questa nuova strategia di modifica del genoma e del suo potenziale in diversi contesti terapeutici e di ricerca, in particolare per le malattie retiniche ereditarie come la retinite pigmentosa“, afferma Yao.