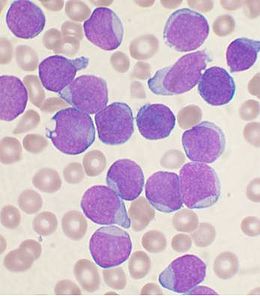
Un nuovo approccio identifica i fattori legati a scarsi risultati del trattamento nella leucemia linfoblastica acuta pediatrica.
La sopravvivenza dei pazienti con leucemia linfoblastica acuta pediatrica (ALL) è notevolmente migliorata negli ultimi decenni. Tuttavia, sono ancora necessarie nuove strategie per identificare i casi che potrebbero rispondere male al trattamento. In un nuovo studio pubblicato sulla rivista EBioMedicine, i ricercatori del Baylor College of Medicine e del Texas Children’s Cancer Center hanno riferito che la profilazione del metaboloma del midollo osseo, la costellazione di piccole molecole prodotte dal metabolismo nel midollo osseo dei pazienti al momento della diagnosi, ha permesso di identificare i pazienti che avevano maggiori probabilità di rispondere male al trattamento.
I ricercatori hanno trovato un’associazione tra metabolismo centrale del carbonio e malattia residua minima dopo il trattamento. Esperimenti in laboratorio hanno dimostrato che il trattamento di TUTTE le cellule con farmaci che interferiscono con il metabolismo del carbonio ha ridotto efficacemente la crescita del cancro, aprendo la possibilità che un approccio simile possa essere tradotto in clinica in futuro.
“In questo studio, volevamo identificare biomarcatori o fattori che prevedessero al momento della diagnosi, quali bambini non avrebbero risposto in modo ottimale alla chemioterapia standard”, ha dichiarato il primo e corrispondente autore dello studio, il Dott. Jeremy M. Schraw, associato post-dottorato nel Dan L Duncan Comprehensive Cancer Center al Baylor. Conoscere questi biomarcatori consentirebbe ai medici di identificare quei pazienti e pianificare il loro trattamento di conseguenza.
In questo studio retrospettivo, Schraw e i suoi colleghi hanno cercato quei possibili biomarcatori nel midollo osseo, dove ha origine TUTTO. Hanno ipotizzato che il metaboloma rifletta le caratteristiche biologiche del paziente, come lo stato di salute delle cellule o la loro capacità di rispondere al trattamento. La profilazione dei metaboliti prodotti nel midollo osseo non era mai stata effettuata prima per identificare TUTTI i pazienti ad alto rischio.
Vedi anche, Leucemia linfoblastica acuta pediatrica, scoperto marcatore genetico predittore della recidiva.
I ricercatori hanno analizzato i campioni di midollo osseo conservati che erano stati prelevati da 155 pazienti al momento della diagnosi. Alla fine del loro primo trattamento con la chemioterapia, questi pazienti sono stati valutati per la minima malattia residua, una misurazione considerata il più potente predittore di recidiva.
“La nostra profilazione dei metaboliti ha mostrato che i metaboliti coinvolti nelle vie del metabolismo del carbonio centrale, come quelli che producono energia cellulare e formano i mattoni del materiale genetico, erano più abbondanti nei pazienti che presentavano una malattia residua minima dopo il trattamento rispetto ai pazienti che hanno eliminato la malattia “, ha detto Schraw.
Quindi, i ricercatori hanno testato in laboratorio l’effetto che l’interruzione del metabolismo centrale del carbonio aveva su TUTTE le cellule.
“Abbiamo scoperto che i farmaci che interferiscono con il metabolismo del carbonio centrale hanno avuto un effetto anti-leucemico sia in TUTTE le linee cellulari che nei campioni di pazienti pediatrici”, ha detto Schraw. “Questo effetto è stato osservato con intervalli di dosi che in precedenza avevano dimostrato di essere realizzabili e ben tollerati in pazienti con altre forme di cancro”.
I risultati di questo studio sono importanti perché evidenziano il potenziale valore del metaboloma come mezzo per identificare TUTTI i pazienti ad alto rischio e pianificare trattamenti più efficaci. La profilazione del metabolita può rivelare potenziali talloni d’Achille anche di altre condizioni e suggerire potenziali nuove strategie di trattamento.
“Abbiamo raggiunto i limiti della chemioterapia intensiva per migliorare la sopravvivenza in TUTTI – l’aggiunta di dosi più elevate o ulteriori farmaci aumenta gli effetti collaterali e spesso non migliora la risposta“, ha affermato l’autore co-senior Dr. Karen R. Rabin, Professore associato di pediatria ematologia e oncologia e membro del Dan L Duncan Comprehensive Cancer Center di Baylor e Direttore del Programma di leucemia presso il Texas Children’s Cancer Center. “Questo studio è importante per identificare un potenziale approccio alternativo all’attacco delle cellule della leucemia nei pazienti con malattia ad alto rischio”.
Fonte, EBioMedicine