Il Premio Nobel per la Medicina 2018 è stato assegnato congiuntamente a James P. Allison e Tasuku Honjo “per la loro scoperta della terapia del cancro mediante l’inibizione della regolazione immunitaria negativa”.
SOMMARIO
Il cancro uccide milioni di persone ogni anno ed è una delle più grandi sfide per la salute dell’umanità. Stimolando la capacità intrinseca del nostro sistema immunitario di attaccare le cellule tumorali, quest’anno i Premi Nobel hanno stabilito un principio completamente nuovo per la terapia del cancro.
James P. Allison ha studiato una proteina nota che funziona da freno al sistema immunitario. Si è reso conto del potenziale di liberare questo freno e quindi di scatenare le nostre cellule immunitarie per attaccare i tumori. Il ricercatore ha poi sviluppato questo concetto in un nuovo approccio per il trattamento dei pazienti.
In parallelo, Tasuku Honjo ha scoperto una proteina sulle cellule immunitarie e, dopo un’attenta esplorazione della sua funzione, alla fine ha rivelato che anche essa funziona da freno, ma con un diverso meccanismo di azione. Le terapie basate sulla sua scoperta si sono rivelate sorprendentemente efficaci nella lotta contro il cancro.
Allison e Honjo hanno dimostrato come diverse strategie per inibire i freni sul sistema immunitario possono essere utilizzate nel trattamento del cancro. Le scoperte seminali dei due vincitori costituiscono un punto di riferimento nella nostra lotta contro il cancro.
La nostra difesa immunitaria può essere ingaggiata per il trattamento del cancro?
Il cancro comprende molte malattie diverse, tutte caratterizzate da proliferazione incontrollata di cellule anormali con capacità di diffusione a organi e tessuti sani. Sono disponibili numerosi approcci terapeutici per il trattamento del cancro, tra cui chirurgia, radioterapia e altre strategie, alcune delle quali sono state premiate con precedenti Premi Nobel. Questi includono metodi per il trattamento ormonale per il cancro alla prostata (Huggins, 1966), la chemioterapia (Elion and Hitchins, 1988) e il trapianto di midollo osseo per la leucemia (Thomas 1990). Tuttavia, il cancro avanzato rimane estremamente difficile da trattare e sono necessarie disperatamente nuove strategie terapeutiche.
Alla fine del 19 ° secolo e all’inizio del 20 ° secolo è emerso il concetto che l’attivazione del sistema immunitario potrebbe essere una strategia per attaccare le cellule tumorali. Sono stati fatti tentativi per infettare i pazienti con batteri per attivare la difesa. Questi sforzi hanno avuto solo effetti modesti, ma una variante di questa strategia è utilizzata oggi nel trattamento del cancro della vescica. Si è capito che era necessaria più conoscenza. Molti scienziati impegnati in intensa ricerca di base e meccanismi fondamentali, hanno scoperto che regolano l’immunità e hanno anche mostrato come il sistema immunitario sia in grado di riconoscere le cellule tumorali. Nonostante notevoli progressi scientifici, i tentativi di sviluppare nuove strategie generalizzabili contro il cancro si sono rivelati difficili.
Acceleratori e freni nel nostro sistema immunitario
La proprietà fondamentale del nostro sistema immunitario è la capacità di discriminare il “sé” da “non sé”, in modo che i batteri, i virus e altri pericoli che invadono possano essere attaccati ed eliminati. Le cellule T, un tipo di globuli bianchi, sono i giocatori chiave in questa difesa. Hanno mostrato di avere recettori che si legano a strutture riconosciute come non-sé e tali interazioni attivano il sistema immunitario a impegnarsi in difesa. Ma sono necessarie anche proteine addizionali che agiscono come acceleratori di cellule T per innescare una risposta immunitaria completa (vedi Figura). Molti scienziati hanno contribuito a questa importante ricerca di base e hanno identificato altre proteine che funzionano come freni sulle cellule T, inibendo l’attivazione immunitaria. Questo intricato equilibrio tra acceleratori e freni è essenziale per uno stretto controllo.
Un nuovo principio per la terapia immunitaria
Durante gli anni ’90, nel suo laboratorio dell’Università della California, a Berkeley, James P. Allison studiò la proteina T-cell CTLA-4. Era uno dei numerosi scienziati che avevano osservato che CTLA-4 funziona come un freno alle cellule T. Altri gruppi di ricerca hanno sfruttato questo meccanismo come bersaglio nel trattamento della malattia autoimmune. Allison, tuttavia, aveva un’idea completamente diversa. Aveva già sviluppato un anticorpo che poteva legarsi a CTLA-4 e bloccarne la funzione (vedi Figura). Ora ha deciso di indagare se il blocco CTLA-4 potrebbe disinnescare il freno delle cellule T e liberare il sistema immunitario per attaccare le cellule tumorali. Allison e collaboratori hanno eseguito un primo esperimento alla fine del 1994 e i risultati sono stati spettacolari. I topi con cancro erano stati curati dal trattamento con gli anticorpi che inibiscono il freno e sbloccano l’attività delle cellule T antitumorali. Nonostante lo scarso interesse dell’industria farmaceutica, Allison ha continuato i suoi intensi sforzi per sviluppare la strategia in una terapia per l’uomo. I risultati promettenti sono presto emersi da diversi gruppi e nel 2010 un importante studio clinico ha mostrato effetti sorprendenti in pazienti con melanoma avanzato, un tipo di cancro della pelle. In diversi pazienti sono scomparsi i segni di cancro rimanente. Tali risultati notevoli non erano mai stati visti prima in questo gruppo di pazienti.
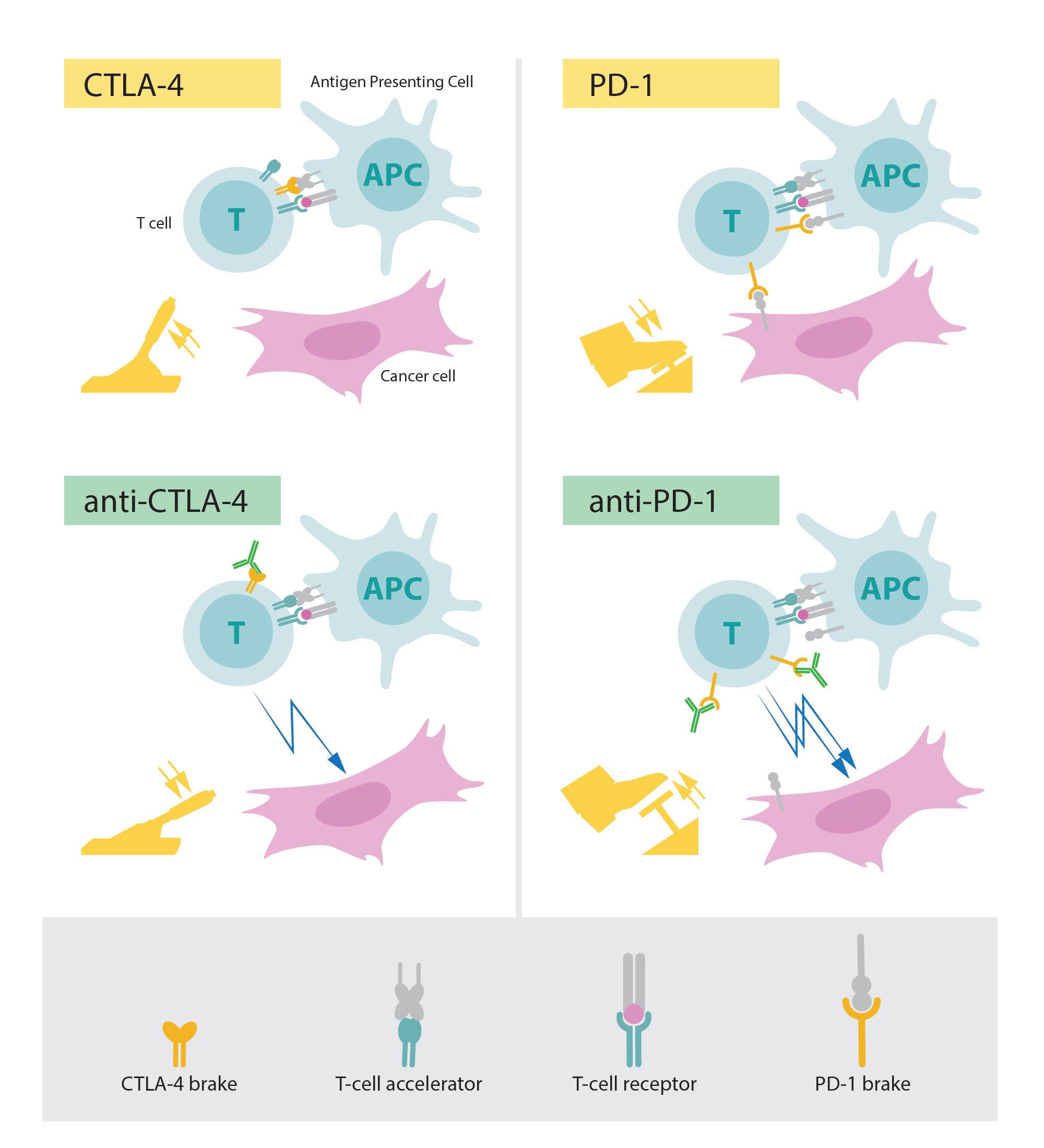
Figura: in alto a sinistra: l’ attivazione delle cellule T richiede che il recettore delle cellule T si leghi alle strutture di altre cellule immunitarie riconosciute come “non sé”. Per l’attivazione delle cellule T è necessaria anche una proteina funzionante come acceleratore di cellule T. CTLA-4 funziona come un freno sulle cellule T che inibisce la funzione dell’acceleratore. In basso a sinistra: gli anticorpi (verdi) contro CTLA-4 bloccano la funzione del freno che porta all’attivazione delle cellule T e all’attacco sulle cellule tumorali. In alto a destra: PD-1 è un altro freno a cellule T che inibisce l’attivazione delle cellule T. In basso a destra: gli anticorpi contro PD-1 inibiscono la funzione del freno che porta all’attivazione delle cellule T e un attacco altamente efficace sulle cellule tumorali.
Scoperta di PD-1 e sua importanza per la terapia del cancro
Nel 1992, alcuni anni prima della scoperta di Allison, Tasuku Honjo scoprì PD-1, un’altra proteina espressa sulla superficie dei linfociti T. Determinato a svelare il suo ruolo, il ricercatore ha esplorato meticolosamente la sua funzione in una serie di eleganti esperimenti condotti per molti anni nel suo laboratorio all’Università di Kyoto. I risultati hanno mostrato che PD-1, simile a CTLA-4, funziona come un freno sulle cellule T, ma funziona con un meccanismo diverso (vedi Figura). Negli esperimenti sugli animali, il blocco di PD-1 si è anche dimostrato una strategia promettente nella lotta contro il cancro, come dimostrato da Honjo e altri gruppi. Questo ha spianato la strada all’utilizzo di PD-1 come bersaglio nel trattamento dei pazienti. Ne è conseguito lo sviluppo clinico e nel 2012 uno studio chiave ha dimostrato una chiara efficacia nel trattamento di pazienti con diversi tipi di cancro.
Terapia immunitaria del checkpoint per il cancro oggi e in futuro
Dopo gli studi iniziali lo sviluppo clinico è stato drastico. Ora sappiamo che il trattamento, spesso definito come “terapia del checkpoint immunitario”, ha cambiato radicalmente il risultato per alcuni gruppi di pazienti con cancro avanzato. Analogamente ad altre terapie antitumorali, si osservano effetti collaterali avversi che possono essere gravi e persino potenzialmente letali. Sono causati da una risposta immunitaria iperattiva che porta a reazioni autoimmuni, ma di solito sono gestibili. Un’intensa ricerca continua è incentrata sulla delucidazione dei meccanismi di azione, con l’obiettivo di migliorare le terapie e ridurre gli effetti collaterali.
Delle due strategie di trattamento, la terapia di controllo contro PD-1 si è dimostrata più efficace e si stanno osservando risultati positivi in diversi tipi di cancro, tra cui il cancro del polmone, il cancro del rene, il linfoma e il melanoma. Nuovi studi clinici indicano che la terapia di combinazione, mirata sia a CTLA-4 che a PD-1, può essere ancora più efficace, come dimostrato nei pazienti con melanoma. Pertanto, Allison e Honjo hanno unito i loro sforzi per combinare diverse strategie per rilasciare i freni sul sistema immunitario allo scopo di eliminare le cellule tumorali in modo ancora più efficiente. Un gran numero di studi di terapia del checkpoint sono attualmente in corso contro la maggior parte dei tipi di cancro e nuove proteine di checkpoint sono state testate come obiettivi.
Per oltre 100 anni gli scienziati hanno tentato di coinvolgere il sistema immunitario nella lotta contro il cancro.
Fino alle scoperte dei due vincitori, i progressi nello sviluppo clinico erano modesti. La terapia di checkpoint ha ora rivoluzionato il trattamento del cancro e ha cambiato radicalmente il modo in cui si può gestire.
Fonte: Nobelprice

