L’Assemblea del Nobel al Karolinska Institutet, ha deciso di assegnare il Premio Nobel 2023 per la Fisiologia e la Medicina congiuntamente a Katalin Karikó e Drew Weissman per le loro scoperte riguardanti le modifiche delle basi nucleosidiche che hanno consentito lo sviluppo di efficaci vaccini a mRNA contro COVID-19.
Le scoperte dei due premi Nobel sono state fondamentali per lo sviluppo di vaccini a mRNA efficaci contro il COVID-19 durante la pandemia iniziata all’inizio del 2020. Attraverso le loro scoperte rivoluzionarie, che hanno cambiato radicalmente la nostra comprensione di come l’mRNA interagisce con il nostro sistema immunitario, i vincitori hanno contribuito al ritmo senza precedenti di sviluppo di vaccini durante una delle più grandi minacce alla salute umana dei tempi moderni.
I vaccini prima della pandemia
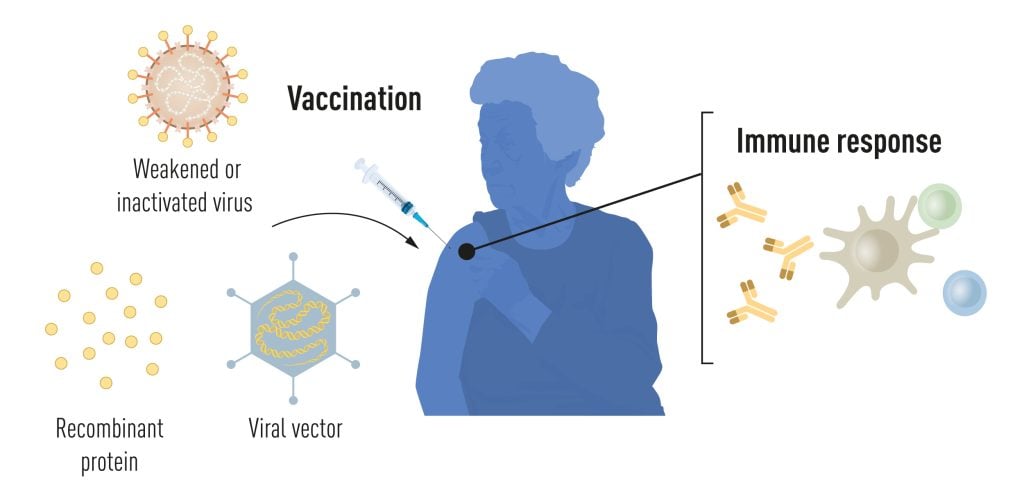
La vaccinazione stimola la formazione di una risposta immunitaria verso un particolare agente patogeno. Ciò dà al corpo un vantaggio nella lotta contro le malattie in caso di esposizione successiva. Da tempo sono disponibili vaccini basati su virus uccisi o indeboliti, come nel caso dei vaccini contro la poliomielite, il morbillo e la febbre gialla. Nel 1951, Max Theiler ricevette il Premio Nobel per la Fisiologia e la Medicina per aver sviluppato il vaccino contro la febbre gialla.
Grazie ai progressi della biologia molecolare negli ultimi decenni, sono stati sviluppati vaccini basati su singoli componenti virali, piuttosto che su virus interi. Parti del codice genetico virale, che solitamente codificano per le proteine presenti sulla superficie del virus, vengono utilizzate per produrre proteine che stimolano la formazione di anticorpi che bloccano il virus. Ne sono un esempio i vaccini contro il virus dell’epatite B e il papillomavirus umano. In alternativa, parti del codice genetico virale possono essere spostate in un virus portatore innocuo, un “vettore”. Questo metodo viene utilizzato nei vaccini contro il virus Ebola. Quando vengono iniettati i vaccini vettori, la proteina virale selezionata viene prodotta nelle nostre cellule, stimolando una risposta immunitaria contro il virus bersaglio.
La produzione di vaccini a base di virus, proteine e vettori interi richiede colture cellulari su larga scala. Questo processo ad alta intensità di risorse limita le possibilità di una rapida produzione di vaccini in risposta a epidemie e pandemie. Pertanto, i ricercatori tentano da tempo di sviluppare tecnologie vaccinali indipendenti dalla coltura cellulare, ma ciò si è rivelato impegnativo.
Vaccini a mRNA: un’idea promettente
Nelle nostre cellule, le informazioni genetiche codificate nel DNA vengono trasferite all’RNA messaggero (mRNA), che viene utilizzato come modello per la produzione di proteine. Durante gli anni ’80 furono introdotti metodi efficienti per produrre mRNA senza coltura cellulare, chiamati trascrizione in vitro. Questo passo decisivo ha accelerato lo sviluppo delle applicazioni della biologia molecolare in diversi campi. Anche l’idea di utilizzare le tecnologie dell’mRNA per vaccini e terapeutici ha preso piede, ma davanti a sé si profilavano ostacoli. L’mRNA trascritto in vitro era considerato instabile e difficile da fornire, richiedendo lo sviluppo di sofisticati sistemi lipidici trasportatori per incapsulare l’mRNA. Inoltre, in vitro l‘mRNA prodotto ha dato origine a reazioni infiammatorie. L’entusiasmo per lo sviluppo della tecnologia dell’mRNA per scopi clinici è stato quindi inizialmente limitato.
Questi ostacoli non scoraggiarono la biochimica ungherese Katalin Karikó, che si dedicò allo sviluppo di metodi per utilizzare l’mRNA a scopo terapeutico. All’inizio degli anni ’90, quando era assistente Professore presso l’Università della Pennsylvania, rimase fedele alla sua visione di realizzare l’mRNA come terapeutico, nonostante incontrasse difficoltà nel convincere i finanziatori della ricerca dell’importanza del suo progetto. Un nuovo collega di Karikó nella sua Università era l‘immunologo Drew Weissman. Il suo interesse era rivolto alle cellule dendritiche che svolgono importanti funzioni nella sorveglianza immunitaria e nell’attivazione delle risposte immunitarie indotte dai vaccini. Spronata da nuove idee, presto iniziò una fruttuosa collaborazione tra i due, concentrandosi su come i diversi tipi di RNA interagiscono con il sistema immunitario.
La svolta
Karikó e Weissman hanno notato che “le cellule dendritiche riconoscono l’mRNA trascritto in vitro come una sostanza estranea, il che porta alla loro attivazione e al rilascio di molecole di segnalazione infiammatoria”. Si chiedevano perché l’mRNA trascritto in vitro fosse riconosciuto come estraneo mentre l’mRNA proveniente da cellule di mammifero non dava luogo alla stessa reazione. Karikó e Weissman si sono resi conto che alcune proprietà critiche devono distinguere i diversi tipi di mRNA.
L’RNA contiene quattro basi, abbreviate A, U, G e C, corrispondenti ad A, T, G e C nel DNA, le lettere del codice genetico. Karikó e Weissman sapevano che “le basi nell’RNA delle cellule di mammifero sono spesso modificate chimicamente, mentre l’mRNA trascritto in vitro non lo è. Si sono chiesti se l’assenza di basi alterate in vitro dell’RNA trascritto potrebbe spiegare la reazione infiammatoria indesiderata”. Per indagare su questo, hanno prodotto diverse varianti di mRNA, ciascuna con alterazioni chimiche uniche nelle loro basi, che hanno consegnato alle cellule dendritiche. I risultati sono stati sorprendenti: la risposta infiammatoria è stata quasi abolita quando le modifiche delle basi sono state incluse nell’mRNA. Si è trattato di un cambiamento paradigmatico nella nostra comprensione di come le cellule riconoscono e rispondono a diverse forme di mRNA. Karikó e Weissman capirono immediatamente che la loro scoperta aveva un profondo significato per l’uso dell’mRNA come terapia. Questi risultati fondamentali sono stati pubblicati nel 2005, quindici anni prima della pandemia di COVID-19.
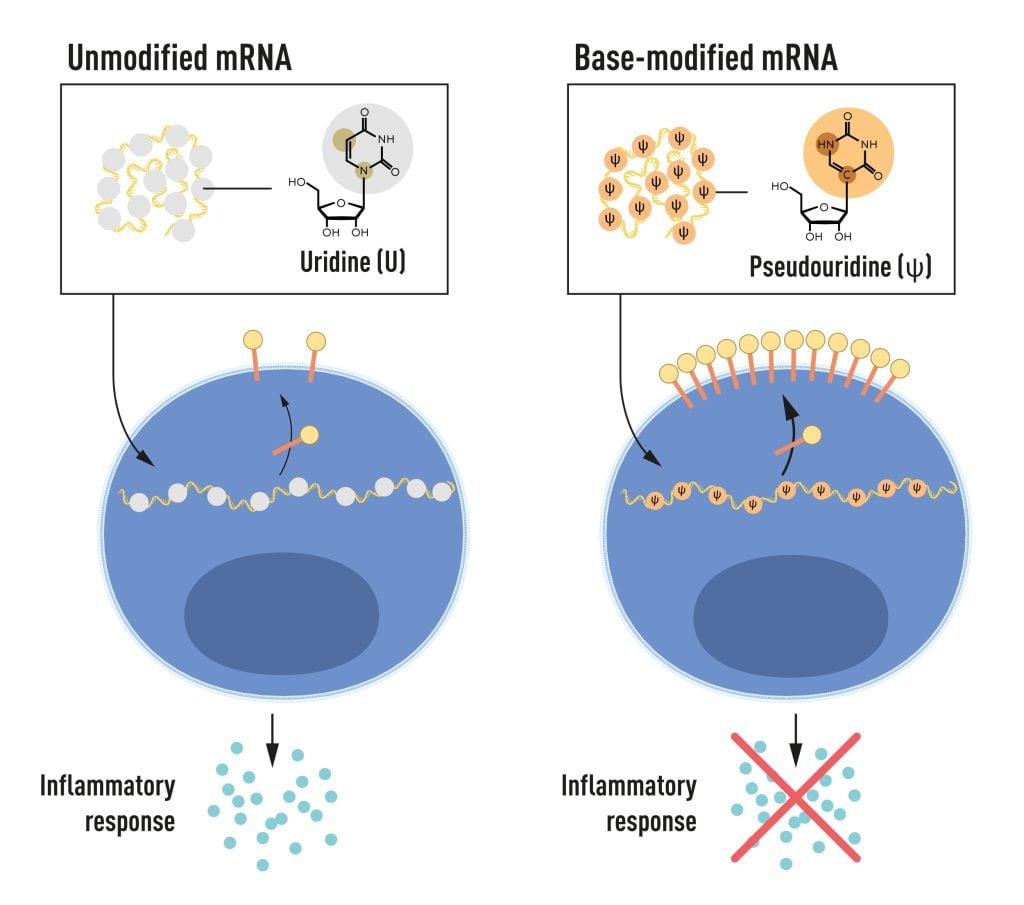
In ulteriori studi pubblicati nel 2008 e nel 2010, Karikó e Weissman hanno dimostrato che £la consegna di mRNA generato con modifiche delle basi ha aumentato notevolmente la produzione di proteine rispetto all’mRNA non modificato”. L’effetto era dovuto alla ridotta attivazione di un enzima che regola la produzione delle proteine. Attraverso la scoperta che “le modifiche delle basi riducono le risposte infiammatorie e aumentano la produzione di proteine”, Karikó e Weissman hanno eliminato gli ostacoli critici sulla strada verso le applicazioni cliniche dell’mRNA.
I vaccini a mRNA hanno realizzato il loro potenziale
L’interesse per la tecnologia dell’mRNA iniziò a crescere e nel 2010 diverse aziende stavano lavorando allo sviluppo del metodo. Sono stati perseguiti i vaccini contro il virus Zika e MERS-CoV; quest’ultimo è strettamente correlato al SARS-CoV-2. “Dopo lo scoppio della pandemia di COVID-19, due vaccini a base di mRNA modificati che codificano per la proteina di superficie SARS-CoV-2 sono stati sviluppati a velocità record“. Sono stati segnalati effetti protettivi di circa il 95% ed entrambi i vaccini sono stati approvati già a dicembre 2020.
L’impressionante flessibilità e velocità con cui i vaccini mRNA possono essere sviluppati aprono la strada all’utilizzo della nuova piattaforma anche per vaccini contro altre malattie infettive. “In futuro, la tecnologia potrebbe essere utilizzata anche per fornire proteine terapeutiche e trattare alcuni tipi di cancro”.
Sono stati rapidamente introdotti anche diversi altri vaccini contro SARS-CoV-2, basati su metodologie diverse e insieme sono state somministrate più di 13 miliardi di dosi di vaccino COVID-19 a livello globale. “I vaccini hanno salvato milioni di vite e prevenuto malattie gravi in molte altre, consentendo alle società di aprirsi e tornare a condizioni normali”. Attraverso le loro scoperte fondamentali sull’importanza delle modifiche delle basi nell’mRNA, i premi Nobel di quest’anno hanno contribuito in modo critico a questo sviluppo trasformativo durante una delle più grandi crisi sanitarie del nostro tempo.
Leggi anche:Nobel per la medicina 2022 a Svante Pääbo per le straordinarie scoperte sull’evoluzione umana
Video: Annuncio del Premio Nobel 2023 per la fisiologia e la medicina da parte del professor Thomas Perlmann, segretario generale dell’Assemblea del Nobel, il 2 ottobre 2023.
Pubblicazioni chiave
Karikó, K., Buckstein, M., Ni, H. and Weissman, D. Suppression of RNA Recognition by Toll-like Receptors: The impact of nucleoside modification and the evolutionary origin of RNA. Immunity 23, 165–175 (2005).
Karikó, K., Muramatsu, H., Welsh, F.A., Ludwig, J., Kato, H., Akira, S. and Weissman, D. Incorporation of pseudouridine into mRNA yields superior nonimmunogenic vector with increased translational capacity and biological stability. Mol Ther 16, 1833–1840 (2008).
Anderson, B.R., Muramatsu, H., Nallagatla, S.R., Bevilacqua, P.C., Sansing, L.H., Weissman, D. and Karikó, K. Incorporation of pseudouridine into mRNA enhances translation by diminishing PKR activation. Nucleic Acids Res. 38, 5884–5892 (2010).
Katalin Karikó è nata nel 1955 a Szolnok, Ungheria. Ha conseguito il dottorato di ricerca presso l’Università di Szeged nel 1982 e ha svolto ricerca post-dottorato presso l’Accademia ungherese delle scienze di Szeged fino al 1985. Ha poi condotto ricerche post-dottorato presso la Temple University, Filadelfia e l’Università di Scienze della Salute, Bethesda. Nel 1989 è stata nominata Professoressa assistente presso l’Università della Pennsylvania, dove è rimasta fino al 2013. Successivamente è diventata vice Presidente e successivamente vice Presidente senior presso BioNTech RNA Pharmaceuticals. Dal 2021 è Professoressa presso l’Università di Szeged e Professoressa a contratto presso la Perelman School of Medicine dell’Università della Pennsylvania.
Drew Weissman è nato nel 1959 a Lexington, Massachusetts, Stati Uniti. Ha conseguito la laurea in medicina e dottorato di ricerca presso l’Università di Boston nel 1987. Ha svolto la sua formazione clinica presso il Beth Israel Deaconess Medical Center della Harvard Medical School e ricerca post-dottorato presso il National Institutes of Health. Nel 1997, Weissman ha fondato il suo gruppo di ricerca presso la Perelman School of Medicine dell’Università della Pennsylvania. È il Roberts Family Professor in Vaccine Research e Direttore del Penn Institute for RNA Innovations.
Illustrazioni: © Comitato Nobel per la Fisiologia e la Medicina. Illustratore: Mattias Karlén
L’Assemblea del Nobel, composta da 50 professori del Karolinska Institutet, assegna il Premio Nobel per la Fisiologia e la Medicina. Il suo comitato per il Nobel valuta le candidature. Dal 1901 il Premio Nobel viene assegnato agli scienziati che hanno fatto le scoperte più importanti a beneficio dell’umanità.
Fonte:NobelPrize

