(Osteoporosi-Immagine Credit Public Domain).
Una proteina cellulare la cui normale funzione sembra sopprimere la formazione ossea potrebbe essere un potenziale nuovo bersaglio per il trattamento dell’osteoporosi, secondo uno studio collaborativo condotto da Weill Cornell Medicine e ricercatori del NewYork-Presbyterian.
Nello studio, pubblicato il 29 luglio su Nature Communications, i ricercatori hanno scoperto che i topi privi della proteina cellulare SLITRK5, che si trova sulla superficie delle cellule osteoblastiche che formano l’osso, costruivano più tessuto osseo rispetto ai topi che esprimono SLITRK5. Esperimenti di laboratorio sui topi hanno confermato che la differenza è dovuta principalmente all’assenza della proteina cellulare.
“Questa proteina della superficie cellulare è un nuovo regolatore negativo della formazione ossea“, ha affermato l’autore senior dello studio, Dr. Matthew Greenblatt, Professore associato di patologia e medicina di laboratorio presso la Weill Cornell Medicine e patologo presso il NewYork-Presbyterian/Weill Cornell Medical Center. “Questi sono davvero i geni più preziosi da scoprire, perché quando li inibiamo con un anticorpo o con altri metodi, potrebbero aumentare la formazione ossea ed essere potenziali bersagli terapeutici per l’osteoporosi e i disturbi correlati”.
Vedi anche:Osteoporosi: come combattere la disgregazione ossea
L’osteoporosi, una condizione sistemica in cui le ossa sono soggette a fratture a causa della densità insufficiente, è la malattia ossea più comune, che affligge circa 10 milioni di persone solo negli Stati Uniti. La malattia è particolarmente comune nelle donne, con quasi il 20% delle donne di età superiore ai 50 anni con osteoporosi e oltre la metà che mostra la condizione precursore della bassa massa ossea.
“I trattamenti disponibili per l’osteoporosi hanno importanti limitazioni nella capacità di invertire la perdita ossea”, ha detto Greenblatt. “Clinicamente, abbiamo pochissimi modi per costruire l’osso e tutti questi modi sono associati a potenziali inconvenienti, quindi avere percorsi aggiuntivi che possiamo indirizzare per costruire nuovo osso aprirebbe nuovi modelli di trattamento non solo per l’osteoporosi, ma anche per altri disturbi della fragilità scheletrica”. Il laboratorio di Greenblatt ha cercato a lungo di rispondere a questa esigenza. Nel nuovo lavoro, lui e i suoi colleghi hanno iniziato la ricerca cercando nuove proteine che sono particolarmente attive nelle cellule degli osteoblasti. Un esperimento di screening ha rivelato un lungo elenco di geni espressi negli osteoblasti, ma non in altri tipi di cellule. Greenblatt e i suoi colleghi hanno quindi filtrato l’elenco per evidenziare i prodotti genici che sarebbero stati secreti o visualizzati sulla superficie cellulare e che sarebbero le proteine più facili da colpire con i farmaci anticorpali. “Ciò che è saltato in cima alla lista è stato un gene precedentemente poco studiato, chiamato SLITRK5“, ha detto Greenblatt.
Per fortuna, uno dei pochi ricercatori ad aver pubblicato un lavoro su SLITRK5 è stato il Dr. Francis Lee, Presidente del Dipartimento di Psichiatria della Weill Cornell Medicine e psichiatra capo del NewYork-Presbyterian/Weill Cornell Medical Center e del NewYork-Presbyterian Westchester Divisione, il cui laboratorio era dall’altra parte del corridoio rispetto a quello di Greenblatt.
“È stata una scoperta sorprendente che SLITRK5 fosse coinvolto nella regolazione della formazione ossea“, ha detto Lee. “Tuttavia, il lavoro del mio laboratorio su questo gene è stato avviato da una precedente discussione fortuita che ho avuto con il Dottor Shahin Rafii (’82), Direttore dell’Ansary Stem Cell Institute presso Weill Cornell Medicine, il cui laboratorio inizialmente ha identificato SLITRK5 in cellule staminali ematopoietiche. Quella discussione ha portato al nostro lavoro collaborativo su questo gene nel corso degli anni”. Gli scienziati dei laboratori Lee e Greenblatt si sono rapidamente uniti e hanno iniziato a sezionare le funzioni specifiche SLITRK5 negli osteoblasti, scoprendo la sua funzione di soppressione ossea. Ulteriori lavori hanno rivelato che SLITRK5 agisce in modo specifico inibendo l’azione della ben studiata proteina di segnale Hh, nota come “riccio”. Tuttavia, i precedenti sforzi per promuovere la formazione ossea aumentando l’attività di Hh sono falliti. “Parte della ragione per la mancanza di progressi nello sfruttare il percorso di Hh è che la proteina fa così tante cose importanti che aumentare la sua attività può essere molto pericoloso”, ha detto Greenblatt.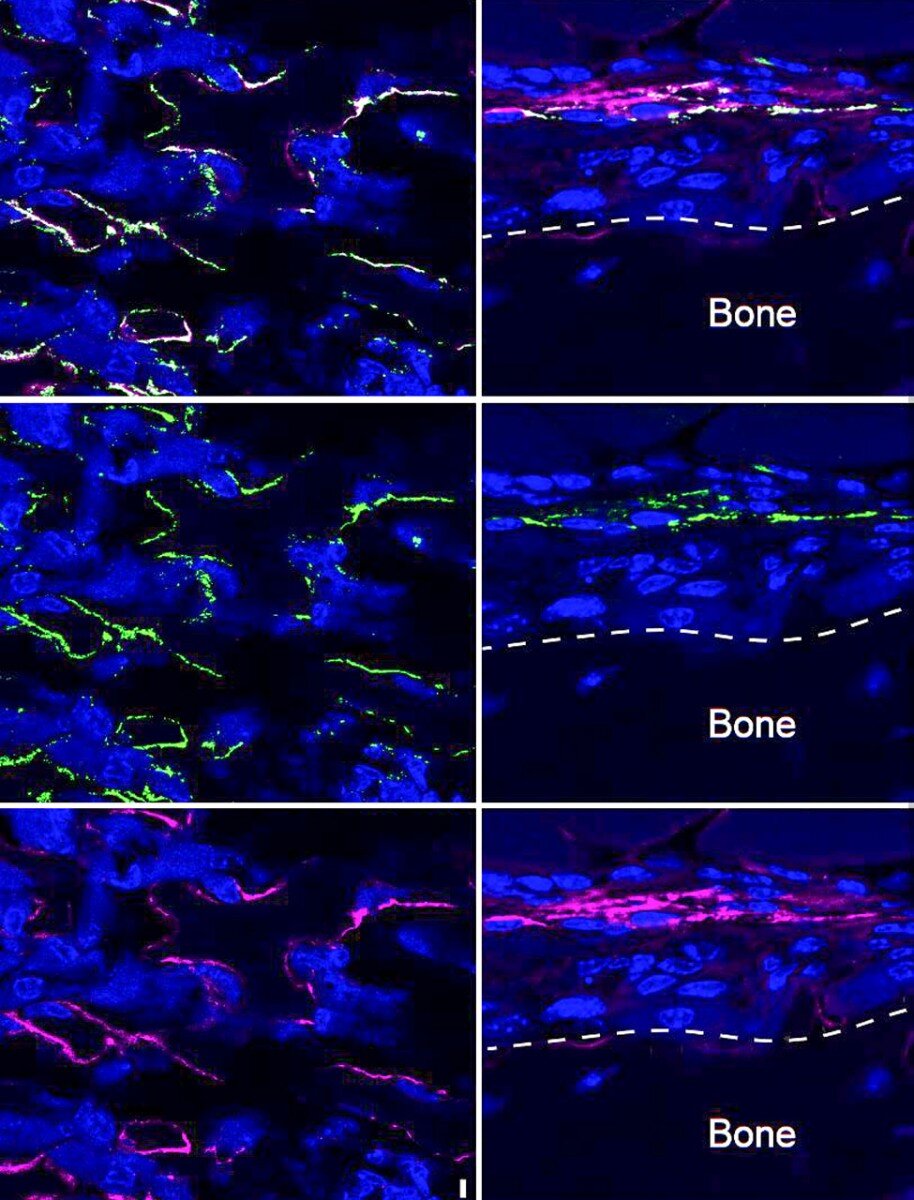
Immagine:le cellule che esprimono la proteina SLITRK5 sono contrassegnate con il magenta (a sinistra) e un marker di osteoblasti che formano l’osso in verde (al centro). Questi marcatori sono stati osservati nell’osso spugnoso nello spazio del midollo (in alto) o sullo strato esterno che copre l’osso (in basso). La sovrapposizione tra questi due marcatori (a destra) mostra che SLITRK5 si trova negli osteoblasti che formano l’osso, ma non in altri tipi di cellule, contribuendo a rendere SLITRK5 un bersaglio per il trattamento delle malattie scheletriche. Credito: Dr. Matthew Greenblatt e Dr. Jun Sun
Il gene SLITRK5 sembra essere molto più specifico. Sebbene l’eliminazione del gene dai topi aumenti i loro tassi di formazione ossea, non provoca difetti scheletrici evidenti. “Senza il gene, i topi costruiscono più ossa”, ha detto Greenblatt, “la forma delle loro ossa è normale e lo sviluppo dello scheletro è normale, quindi è tutto rassicurante”. La mancanza di importanti effetti collaterali suggerisce che i farmaci mirati a SLITRK5 non possono causare problemi, almeno nella crescita scheletrica.
Insieme a Lee e ai collaboratori della Xiamen University, della University of Massachusetts Medical School, di LegoChem BioSciences, dell’Hospital for Special Surgery e del Tri-Institutional Therapeutics Discovery Institute, il team di Greenblatt sta ora cercando di trasformare i risultati in una terapia per l’osteoporosi.