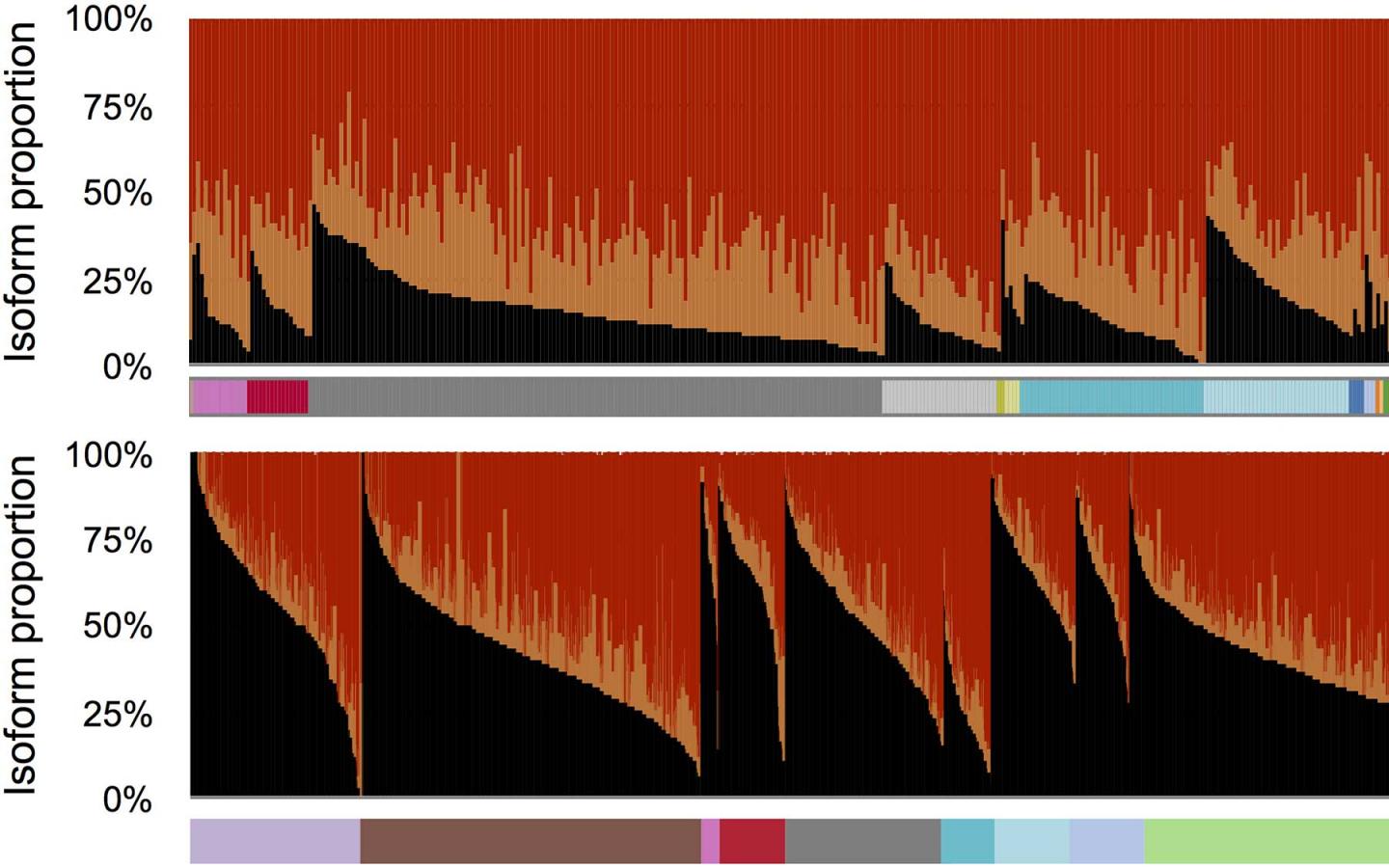
Immagine: nell’immagine sono rappresentate diverse versionio isoforme di RNA Messaggeri generati dal gene AFMID umano che mostrano la loro prevalenza relativa nel tessuto canceroso ( in alto) e non canceroso ( in basso).
Poiché il cancro del fegato è particolarmente vario geneticamente e soggetto a recidiva, identificare i biomarcatori che possono prevedere la progressione della malattia è un obiettivo fondamentale nella lotta contro di esso.
I ricercatori del Cold Spring Harbor Laboratory (CSHL), guidati dal Professor Adrian Krainer del CSHL, ora riferiscono di aver sviluppato un metodo per identificare i biomarcatori basati sullo splicing per la forma più comune di cancro del fegato, il carcinoma epatocellulare (HCC). I ricercatori ritengono che il metodo sarà utile anche per altri tipi di cancro.
“Questo studio sottolinea il potenziale di imparare come le varianti di splicing dell’RNA (Splicing: processo di trasformazione (maturazione) di una molecola di RNA mediato dalla rimozione dialcune sequenze (introni) e dall’unione di quelle rimanenti con formazione di un RNA maturo per le successive funzioni (in partic., per la traduzione, nel caso dell’mRNA), possono contribuire al cancro e punta a queste varianti come potenziali biomarcatori per la progressione del cancro”, dice Krainer.
( Vedi anche: Individuata una strategia migliore per curare il cancro del fegato).
Lo splicing si riferisce a un processo in cui un messaggio RNA copiato da informazioni codificate in un gene viene modificato prima di essere in grado di fungere da modello per la produzione di una specifica proteina. Un gene può dare origine a più messaggi RNA, ciascuno risultante in una diversa variante proteica o “isoforma”. Molte malattie sono state associate ad errori o variazioni nel modo in cui l’RNA è giuntato. Errori o variazioni nello splicing possono portare a proteine non funzionali o con funzioni distinte o aberranti.
Recenti studi hanno identificato irregolarità di splicing nelle cellule di cancro del fegato. Guidato dal ricercatore postdottorato del CSHL Kuan-Ting Lin, il team di Krainer ha sviluppato un metodo che analizza in modo esauriente tutti i messaggi RNA realizzati da un determinato gene. Il team ha testato il loro metodo di rilevazione della splicing-variant in HCC, analizzando i messaggi di RNA nelle cellule HCC campionate da centinaia di pazienti.
I ricercatori hanno scoperto che le particolari isoforme di splicing del gene AFMID erano correlate ad una sopravvivenza del paziente molto scarsa. Queste varianti portano le cellule a produrre versioni troncate della proteina AFMID. Queste versioni insolite della proteina sono associate nelle cellule del cancro del fegato degli adulti con mutazioni nei geni soppressori del tumore denominati TP53 e ARID1A.
Queste mutazioni, ipotizzano i ricercatori, sono associate a bassi livelli di una molecola chiamata NAD + che è coinvolta nella riparazione del DNA danneggiato. Il ripristino delle porzioni mancanti, chiamate esoni, nel normale messaggio RNA di AFMID, potrebbe portare a livelli normali di NAD + evitando mutazioni in TP53 e ARID1A. Il team spera di utilizzare piccole molecole chiamate ASO (oligonucleotidi antisenso) che possono legarsi all’RNA, per cambiare il modo in cui i messaggi RNA di AFMID sono uniti. La squadra di Krainer in precedenza ha usato questa tecnica per correggere gli errori nello splicing del gene SMN2 come un modo per trattare l’atrofia muscolare spinale (SMA).
La fissazione dello splicing AFMID potrebbe portare ad una maggiore produzione di NAD + e ad un aumento della riparazione del DNA.
“Lo splicing AFMID può diventare un bersaglio terapeutico e la fonte di un nuovo farmaco per il cancro del fegato“, dice Lin. Gli esperimenti preliminari suggeriscono che la squadra è sulla strada giusta. Hanno dimostrato che il coassamento delle cellule per sovra esprimere AFMID giuntato nel modo normale ha portato a livelli più alti di NAD + e crescita più lenta delle cellule del cancro del fegato.
Fonte: EurekAlert