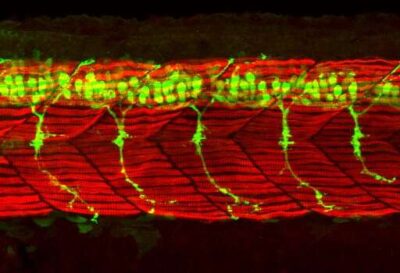
(Malattie neurodegenerative-Immagine: un segmento del tronco di zebrafish. I motoneuroni (in verde) inviano assoni che innervano le fibre muscolari (in rosso). Credito: Nikolas Nikolaou).
Una scoperta che potrebbe migliorare le opzioni terapeutiche per i pazienti con malattie neurodegenerative è stata fatta dagli scienziati del King’s College di Londra e dell’Università di Bath.
- Questa scoperta è incentrata su una molecola che svolge un ruolo profondo nello sviluppo delle cellule nervose e che è nota per contribuire alla malattia quando non funziona correttamente. In precedenza si pensava che questa molecola fosse limitata al nucleo della cellula (l’organello contenente il DNA di una cellula e separato dal resto della cellula da una membrana), ma questo nuovo studio conferma una precedente scoperta della stessa squadra che può anche essere trovata nel citoplasma (l’interno acquoso di una cellula).
Lo studio dimostra anche per la prima volta che il pool citoplasmatico di questa proteina è funzionalmente attivo.
Questa scoperta ha importanti implicazioni per la ricerca sui disturbi neurodegenerativi come l’Alzheimer e la malattia dei motoneuroni.
La scoperta, descritta in Current Biology, è stata fatta dalla Prof.ssa Corinne Houart del King’s College di Londra in collaborazione con il Dottor Nikolas Nikolaou del Dipartimento di scienze della vita di Bath.
Perdita della funzione nervosa
Gli scienziati sanno da tempo che lo splicing delle proteine, le molecole studiate in questa ricerca, a volte può aggregarsi e formare complessi insolubili nel citoplasma della cellula e che questi complessi possono interferire con la funzione di un neurone (cellula nervosa), causando alla fine la perdita di funzione e la degenerazione del neurone. Tuttavia, questo studio è il primo a dimostrare che un’importante proteina di splicing può essere trovata all’interno dei complessi proteina/RNA messaggero (noti come granuli di RNA), all’interno degli assoni delle cellule nervose.
Gli assoni sono le lunghe proiezioni che conducono gli impulsi elettrici lontano dal corpo delle cellule nervose, collegando i neuroni con i neuroni vicini o trasmettendo informazioni dai neuroni ai tessuti del corpo (diciamo, muscoli o pelle). È noto che la disfunzione degli assoni è la causa di molti disturbi neurologici progressivi, quindi la scoperta di proteine di giunzione in questa parte della cellula nervosa suggerisce il meccanismo che potrebbe dare origine alla malattia.
Modellare la molecola di RNA messaggero
I ricercatori hanno scoperto che la proteina di splicing SNRNP70 si lega a, e successivamente modella, filamenti di RNA messaggero (mRNA). Questi filamenti trasportano informazioni genetiche dal DNA nel nucleo di una cellula al citoplasma della cellula. Le informazioni trasportate dall’mRNA vengono utilizzate per creare ulteriori proteine, i mattoni della vita. Il team ha anche scoperto che la proteina di splicing è necessaria affinché l’mRNA si sposti dal corpo della cellula nervosa lungo gli assoni verso parti più periferiche di un neurone.
Vedi anche:Malattie neurodegenerative: dal colesterolo nuovo approccio terapeutico
Commentando questa ricerca, che utilizza il pesce zebra come sistema modello genetico, il Dottor Nikolaou ha detto: “Quando abbiamo interferito con la funzione della proteina di splicing, abbiamo visto che i motoneuroni non si formavano bene. Non sono riusciti a stabilire connessioni dove avrebbero dovuto e hanno perso altre importanti connessioni. Questo tipo di comportamento si osserva anche nella neurodegenerazione umana. Tuttavia, quando SNRNP70 è stato reintrodotto solo nel citoplasma e negli assoni di questi neuroni, è stato sufficiente ripristinare la connettività motoria e la funzione neuronale ancora una volta”.
Nonostante sia un piccolo pesce d’acqua dolce, il pesce zebra è una specie con un sistema nervoso molto simile a quello che si trova negli esseri umani.
Nella fase successiva di questa ricerca, il Dottor Nikolaou prevede di esplorare la precisa funzione di questa proteina negli assoni. “Sappiamo che le proteine interagiscono con altre proteine, quindi con quali proteine interagisce questa molecola? E cosa succede quando rimuoviamo questi complessi dal citoplasma: in che modo questo influisce sulla funzione dei neuroni?”
Ha aggiunto: “Ora che sappiamo che questi tipi di molecole hanno una funzione al di fuori del nucleo, dovremo affrontare la neurodegenerazione da un’angolazione diversa, chiedendoci come questi aggregati che causano malattie interferiscono con la funzione di queste proteine non solo nel nucleo ma anche nel citoplasma e quale ruolo svolgono nella rottura dei neuroni. Questo è qualcosa a cui non si era pensato prima”.
Fonte:Current Biology