Malattie neurodegnerative-Immagine Credit Public Domain-
Malattie neurodegenerative come il morbo di Parkinson, l’Alzheimer e la malattia di Huntington non hanno cure o opzioni terapeutiche per rallentarne la progressione. Sono state proposte opzioni terapeutiche potenzialmente promettenti, ma limitate dall’incapacità di attraversare la barriera emato-encefalica.
La terapia genica è una delle potenziali terapie che i ricercatori vorrebbero studiare, con la speranza di correggere i meccanismi patogenetici, rafforzare la neuroprotezione e avviare la neurorigenerazione e il ripristino del tessuto cerebrale danneggiato.
In un documento intitolato “Targeted AAV vector delivery and PET imaging”, pubblicato su Science Advances, i ricercatori guidati dall’Università CEU-San Pablo in Spagna riferiscono su un metodo di attraversamento sicuro la barriera emato-encefalica.
I vettori di virus adeno-associati (AAV) sono un veicolo attraente per il trasferimento di geni nei tessuti. Gli AAV sono piccoli DNA a filamento singolo non avvolti su cui gli scienziati hanno lavorato per creare una piattaforma per la consegna genica. Esistono AAV ingegnerizzati con la maggior parte dei genomi virali sostituiti con “cassette di espressione” contenenti un promotore, un carico utile genico e un terminatore. Questi AAV di ricerca non possono replicarsi come un virus selvaggio, ma il carico genico che trasportano può essere espresso (spesso con un secondo virus helper), fornendo un’espressione genica terapeuticamente vantaggiosa a lungo termine.
Un vantaggio della terapia genica è che la consegna del vettore AAV sarebbe necessaria solo occasionalmente poiché studi precedenti hanno dimostrato trattamenti che durano diversi anni o più. Le terapie con molecole farmacologiche richiedono interventi molto più frequenti, il che di solito non costituisce un ostacolo al trattamento a meno che il trattamento non sia nel cervello.
Un fattore limitante nell’utilizzo di AAV (o molecole di farmaci) nel cervello è la barriera emato-encefalica, una fitta rete di cellule endoteliali protettive, periciti, astrociti e microglia che lavorano tutti per tenere fuori batteri e molecole indesiderate.
Per superare la barriera, gli AAV devono rimanere molto piccoli, limitando le opzioni di carico utile della cassetta. Una volta che gli AAV sono passati, sorge un altro problema, la posizione. Se gli AAV sono necessari per trattare tessuti specifici in posizioni specifiche del cervello, il solo superamento del sangue nel cervello potrebbe non essere sufficiente per generare l’effetto terapeutico.
Nei modelli di ricerca sugli animali, l’atto di inserire AAV con iniezioni intracerebrali, il modo più diretto di condurre una sperimentazione genetica terapeutica, a volte può provocare un danno tissutale abbastanza traumatico da causare la morte. Ragionevolmente, questo è un fattore limitante quando si considerano le sperimentazioni umane. Come sottolineano gli autori dello studio, i trattamenti per le malattie neurodegenerative possono richiedere la somministrazione simultanea in diverse regioni del cervello e un approccio ideale di consegna genica alle malattie del cervello dovrebbe essere sicuro, non invasivo e specifico per regione.
Nello studio attuale, i ricercatori riferiscono di aver creato un’apertura efficace della barriera emato-encefalica e di fornire vettori AAV in specifiche regioni del cervello coinvolte nella malattia di Parkinson utilizzando ultrasuoni focalizzati a bassa intensità guidati dalla risonanza magnetica.
L’espressione della proteina fluorescente verde neuronale è stata osservata specificamente nelle regioni con l’apertura della barriera emato-encefalica, confermando che il metodo di consegna ha avuto successo. La permeabilità della barriera emato-encefalica è stata ripristinata entro 24 ore e non sono stati segnalati effetti avversi.
Vedi anche:La disregolazione del ferro potrebbe contribuire alle malattie neurodegenerative
La sperimentazione iniziale è stata condotta su scimmie macaco adulte e un follow-up è stato condotto su tre pazienti umani con malattia di Parkinson. La natura meno invasiva di questa metodologia potrebbe facilitare la consegna del vettore virale per la terapia genica, rendendo gli interventi teorici per il trattamento dei disturbi neurodegenerativi, una realtà.
Astratto grafico:
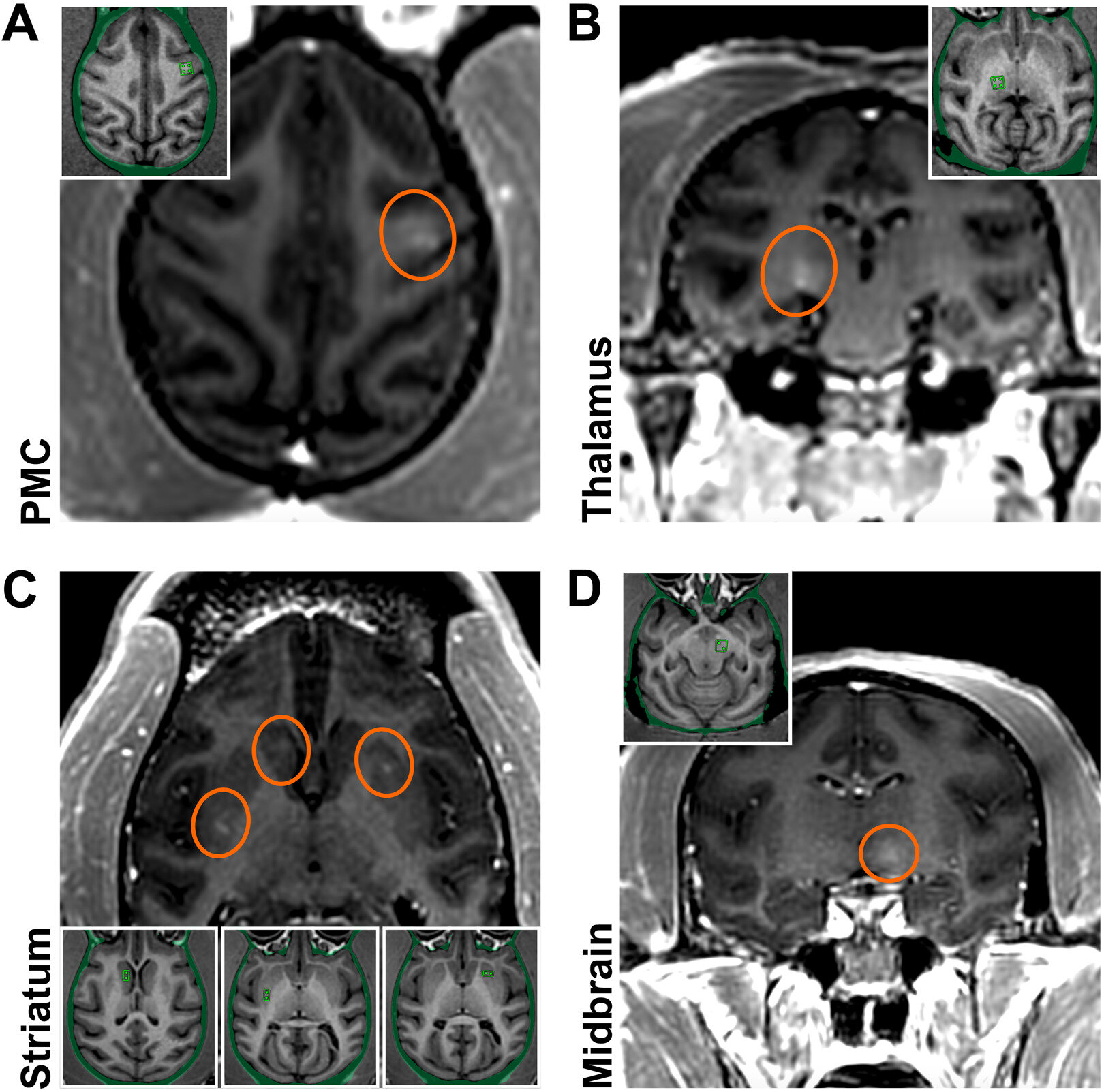
Immagine: aperture ematoencefaliche iniziali negli NHP mirate alle regioni cerebrali rilevanti per il PD. Le aperture BEE riuscite sono state dimostrate in due scimmie (M1/M2) mediante la consegna di un agente di contrasto MR (Gd) che normalmente non stravasa nel cervello. Le aperture sono state raggiunte nelle regioni target con relativa precisione. (A) L’immagine MRI pesata in T1 con contrasto assiale mostra l’interruzione della BEE nel PMC (indicata dal cerchio rosso; M1). (B) La risonanza magnetica con contrasto coronale mostra l’interruzione del BBB nella regione talamica ventrolaterale posteriore (M1). (C) La risonanza magnetica assiale con mezzo di contrasto mostra l’interruzione della BEE nello striato (sia la testa del nucleo caudato che il putamen posteriore su un lato e il putamen anteriore sull’altro; M2). (D) La risonanza magnetica con contrasto coronale mostra l’interruzione della BEE nel mesencefalo (M2). Tutti i miglioramenti sono stati in gran parte limitati alle regioni target. Sebbene sia stato utilizzato lo stesso approccio per ogni sonicazione, le dimensioni e l’entità dell’interruzione del BBB variavano a seconda della regione target. Credito:I progressi della scienza (2023). DOI: 10.1126/sciadv.adf4888-
Mentre l’attuale studio si è concentrato sui disturbi neurodegenerativi, una miriade di altri disturbi sono sfuggiti al trattamento perché si verificano dietro la barriera emato-encefalica e sono al di là della portata delle terapie convenzionali. Meningite, sifilide e toxoplasmosi, solo per citarne alcuni, potrebbero vedere tutte nuove opzioni terapeutiche con un passaggio sicuro attraverso il labirinto del sistema vascolare cerebrale protettivo.
Fonte:Science Advances