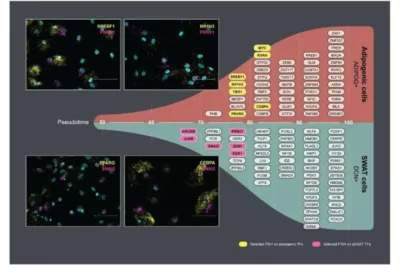
Malattie cardiometaboliche-Immagine: i fattori di trascrizione identificati come aumento dell’espressione in un ramo rispetto a un altro sono indicati sui rispettivi rami, nel punto pseudotemporale allungato in cui si osserva che l’espressione genica levigata diverge. Le immagini dell’inserto provengono dall’etichettatura dell’RNA FISH negli adipociti marroni di combinazioni, selezionate di fattori di trascrizione specifici del ramo. Barra della scala, 75 µm. Credito: Università di Copenaghen-
Gli scienziati hanno scoperto un nuovo tipo di cellula, SWAT, che può trasformarsi in cellule adipose a seconda del microambiente. Una migliore comprensione dei processi che bilanciano i tipi cellulari potrebbe ispirare approcci innovativi per affrontare le malattie cardiometaboliche.
Il grasso immagazzinato nel corpo, il tessuto adiposo, contiene molti tipi di cellule diverse, comprese le cellule di grasso bianco (WAT), che immagazzinano i lipidi e le cellule di grasso bruno (BAT), che bruciano i lipidi per produrre calore ed energia. Ora, gli scienziati dell’Università di Copenaghen e del Rigshospitalet hanno scoperto un nuovo tipo di cellula nel grasso chiamata SWAT, che conferisce al tessuto adiposo la sua integrità strutturale.
In un articolo pubblicato su Nature Metabolism, gli scienziati spiegano come la scoperta delle cellule SWAT potrebbe rimodellare la nostra conoscenza del funzionamento dei tessuti adiposi e del loro ruolo cruciale nello sviluppo di malattie cardiometaboliche.
Le cellule residenti nel tessuto adiposo regolate da Wnt strutturale, o cellule SWAT in breve, rilasciano proteine che aiutano a dare al tessuto adiposo la sua struttura. Tuttavia, i ricercatori sono rimasti sorpresi nello scoprire che le cellule SWAT si sviluppano dalle stesse cellule madri (progenitrici) delle cellule adipose. Hanno anche scoperto che le cellule SWAT sono flessibili e possono passare a diversi tipi di cellule, comprese le cellule adipose o addirittura tornare alle cellule progenitrici.
“Le cellule SWAT hanno la straordinaria capacità di tornare a uno stato simile a un progenitore o di differenziarsi in nuove cellule adipogeniche, a seconda del microambiente“, afferma la Prof.ssa associata Camilla Schéele del Novo Nordisk Foundation Center for Basic Metabolic Research dell’Università di Copenhagen e uno degli autori co-senior del documento.
L’ambiente potrebbe dettare il destino della cellula
La flessibilità delle cellule SWAT di ritornare in cellule progenitrici o di svilupparsi ulteriormente in cellule WAT o cellule BAT suggerisce che le cellule SWAT svolgono un ruolo essenziale nel consentire al tessuto adiposo di adattarsi a diverse condizioni metaboliche.
Leggi anche:Mangiare patate aumenta il rischio di malattie cardiometaboliche?
“Ipotizziamo che il crosstalk intercellulare mantenga un delicato equilibrio tra i diversi tipi di cellule. Questo equilibrio può essere interrotto in un microambiente obesogenico, contribuendo potenzialmente allo sviluppo di malattie cardiometaboliche“, ha spiegato il ricercatore senior Søren Nielsen del Rigshospitalet, un altro co-autore senior dell’articolo.
Spiegano gli autori:
“La distribuzione del grasso corporeo e la funzionalità degli adipociti sono determinanti della salute metabolica in modo dipendente dal deposito. Diversi studi hanno descritto che l’obesità addominale è fortemente associata a malattie cardiovascolari e all’insulino-resistenza, mentre l’accumulo di grasso nelle regioni ginoidi inferiori ha un ricambio lipidico inferiore ed è associato alla salute metabolica. Anche l’attività del tessuto adiposo bruno (BAT) è associata alla salute metabolica. Gli adipociti originano da cellule staminali mesenchimali che risiedono in più tessuti tra cui il tessuto adiposo, il muscolo scheletrico e il midollo osseo. Altri studi hanno mostrato una stretta relazione tra osteociti e adipociti, con opposte traiettorie di differenziazione mediate attraverso una comune rete trascrizionale. Le tecnologie unicellulari hanno permesso di comprendere l’eterogeneità degli adipociti, rivelando diversi sottotipi con funzioni specializzate. Questi studi suggeriscono che i tipi di cellule separate forniscono la termogenesi, la sensibilità all’insulina, l’accumulo di lipidi e la secrezione di adipochine o agiscono come regolatori negativi dell’accumulo di lipidi. Tuttavia, l’eterogeneità gerarchica dello sviluppo degli eventi adipogenici umani marroni e bianchi rimane sfuggente. La funzione degli adipociti è un importante determinante della malattia metabolica e questo giustifica le indagini sui meccanismi di regolazione. Mostriamo alla risoluzione di una singola cellula che le cellule progenitrici di quattro depositi adiposi marroni e bianchi umani si separano in due destini cellulari principali, un adipogenico e un ramo strutturale, che si sviluppano da un progenitore comune. La firma del gene adipogenico contiene geni dell’attività mitocondriale e si associa a tratti di studio di associazione su tutto il genoma per la distribuzione del grasso. In conclusione, forniamo una mappa di differenziazione degli adipociti umani e definiamo la cellula multipotente SWAT, fornendo una nuova prospettiva sulla regolazione del tessuto adiposo“.
Gli scienziati devono ancora comprendere appieno quali segnali controllano lo sviluppo dei diversi tipi di cellule. Tuttavia, sono ottimisti sul fatto che lo studio possa ispirare approcci innovativi per affrontare le sfide per la salute legate all’obesità, svelando gli intricati meccanismi che regolano il modo in cui gli adipociti si differenziano.
I ricercatori dell’Università del Massachusetts, negli Stati Uniti, hanno anche pubblicato uno studio su Nature Metabolism sulla scoperta della SWAT, con risultati complementari.
Fonte:Nature Metabolism