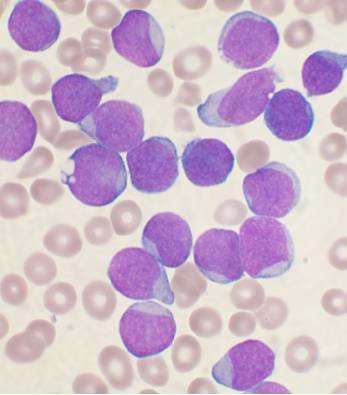
(Leucemia linfoblastica acuta-Immagine: aspirato di midollo osseo colorato di Wright di un paziente con leucemia linfoblastica acuta a cellule B precursore. Credito: VashiDonsk/Wikimedia/CC BY-SA 3.0).
Le varianti genetiche ereditarie (della linea germinale) sono state associate alla suscettibilità alla leucemia linfoblastica acuta (ALL).
Gli scienziati del St. Jude Children’s Research Hospital hanno rivelato un meccanismo biologico che aumenta le probabilità di sviluppare un tipo di leucemia pediatrica ad alto rischio. I meccanismi molecolari che collegano i cambiamenti genomici ereditari e cancerosi (somatici) in questo contesto sono poco conosciuti. I risultati mostrano come una variante ereditaria del gene GATA3 influenzi il processo mediante il quale un bambino sviluppa LLA simile al cromosoma Philadelphia (così chiamato perché scoperto appunto a Philadelphia (USA), è il cromosoma 22 modificato per l’inserzione di un frammento terminale proveniente dal cromosoma 9).
Lo studio è stato pubblicato oggi su Nature Genetics.
LLA Ph-like è un sottotipo ad alto rischio di ALL a cellule B (B-ALL) che ha una scarsa sopravvivenza e un profilo di espressione genica simile alla LLA Ph-positiva. Gli scienziati del St. Jude hanno precedentemente condotto uno studio di associazione sull’intero genoma (GWAS) su ALL Ph-like. Sulla base di ciò, ora hanno sequenziato il gene GATA3 in più di 5.000 pazienti e identificato la variante specifica che guida l’associazione.
Vedi anche:Leucemia linfoblastica acuta: i farmaci chemioterapici posso indurre la recidiva
GATA3 è ben noto per il suo ruolo come fattore di trascrizione nello sviluppo delle cellule T ed è quindi più spesso associato alle leucemie a cellule T. Questi ricercatori volevano capire il meccanismo che fa sì che questa variante ereditaria di GATA3 interagisca con altre caratteristiche genomiche della leucemia a cellule B.
“Questo studio funge da modello di ciò che dovrebbe seguire dopo il GWAS”, ha affermato il co-autore Jun J. Yang, Ph.D., dipartimenti di oncologia e scienze farmaceutiche di St. Jude. “È un allontanamento da molti altri progetti genomici sul cancro perché il loro focus è più spesso sul DNA somatico o sul cancro”.
“L’aggiunta della componente della linea germinale ci offre un’angolazione e un’opportunità uniche per comprendere la biologia del cancro”, ha affermato Yang. “Se non avessimo fatto un GWAS, non avremmo mai pensato al ruolo così importante di GATA3 in B-ALL”.
Rivelato un meccanismo di attivazione
Utilizzando l’editing del genoma CRISPR-Cas9 e campioni di pazienti tutti simili a Ph, i ricercatori hanno dimostrato che la variante ereditata attivava un forte potenziatore che si attivava e aumentava la trascrizione di GATA3. Hanno scoperto che se l’espressione di GATA3 è più alta, si traduce in una maggiore propensione al riarrangiamento genetico che colpisce un gene chiamato CRLF2, un noto oncogene per la leucemia. Questo riarrangiamento si verifica perché GATA3 regola direttamente l’espressione di CRLF2.
Questo studio fornisce prove di un meccanismo distinto che fa sì che una variante ereditaria non codificante aiuti ad attivare un oncogene attraverso la regolazione epigenetica e la riprogrammazione del genoma 3D.
Spiegano gli autori:
“Le varianti genetiche ereditarie non codificanti conferiscono una significativa suscettibilità alla leucemia linfoblastica acuta (ALL) infantile, ma i processi molecolari che collegano i polimorfismi germinali alle lesioni somatiche in questo tumore sono poco conosciuti. Attraverso il sequenziamento mirato in 5.008 pazienti, abbiamo identificato una variante fondamentale della linea germinale regolatoria in GATA3 associata a ALL simil-cromosoma Philadelphia (ALL Ph-like). Utilizzando l’editing CRISPR-Cas9 e campioni di pazienti con ALL Ph-like, abbiamo dimostrato che questa variante attivava un forte potenziatore che sovraregolava la trascrizione GATA3. Questo, a sua volta, ha rimodellato l’accessibilità globale della cromatina e l’organizzazione tridimensionale del genoma, comprese le regioni prossimali all’oncogene ALL CRLF2. Alla fine, abbiamo dimostrato che GATA3 regolava direttamente CRLF2 e potenziava gli effetti oncogenici JAK-STAT durante la leucemogenesi. Presi insieme, questi dati forniscono prove di un meccanismo distinto mediante il quale una variante non codificante della linea germinale contribuisce all’attivazione dell’oncogene, alla regolazione epigenetica e alla riprogrammazione tridimensionale del genoma”.
“Abbiamo capito come una variante di rischio ereditaria per LLA regola un’anomalia genomica specifica del cancro che alla fine porta alla leucemia con queste caratteristiche specifiche”, ha affermato il co-autore Feng Yue, Ph.D., Northwestern University e Robert H. Lurie Comprehensive Centro del cancro. “Abbiamo ritenuto importante fornire un meccanismo per il modo in cui la variante ereditaria ha effettivamente influenzato il panorama genomico in questo particolare sottotipo di leucemia linfoblastica acuta“.
Fonte:Nature Genetics