(Lesioni midollo spinale-Immagine Credit Public Domain).
I ricercatori della Northwestern University hanno sviluppato una nuova terapia iniettabile che sfrutta “molecole danzanti” per invertire la paralisi e riparare i tessuti dopo gravi lesioni del midollo spinale.
In un nuovo studio, i ricercatori hanno somministrato una singola iniezione ai tessuti che circondano il midollo spinale di topi paralizzati. Solo quattro settimane dopo, gli animali hanno riacquistato la capacità di camminare.
La ricerca sarà pubblicata nel numero del 12 novembre 2021 della rivista Science.
Inviando segnali bioattivi per indurre le cellule a ripararsi e rigenerarsi, la terapia rivoluzionaria ha notevolmente migliorato il midollo spinale gravemente ferito in cinque modi chiave: (1) le estensioni recise dei neuroni, chiamate assoni, si sono rigenerate; (2) tessuto cicatriziale, che può creare una barriera fisica alla rigenerazione e alla riparazione, notevolmente diminuito; (3) la mielina, lo strato isolante degli assoni che è importante per trasmettere i segnali elettrici in modo efficiente, riformata intorno alle cellule; (4) vasi sanguigni funzionali formati per fornire nutrienti alle cellule nel sito della lesione e (5) più motoneuroni sono sopravvissuti.
Dopo che la terapia ha svolto la sua funzione, i materiali si biodegradano in sostanze nutritive per le cellule entro 12 settimane e poi scompaiono completamente dal corpo senza effetti collaterali evidenti. Questo è il primo studio in cui i ricercatori hanno controllato il movimento collettivo delle molecole attraverso cambiamenti nella struttura chimica per aumentare l’efficacia di una terapia.
Una semplice animazione mostra come una singola iniezione ripristina le connessioni nel sistema nervoso al di sotto del sito di una grave lesione del midollo spinale. Credito: Samuel I. Stupp Laboratory/Mark Seniw/Northwestern University
“La nostra ricerca mira a trovare una terapia che possa impedire agli individui di rimanere paralizzati dopo gravi traumi o malattie”, ha affermato Samuel I. Stupp della Northwestern University che ha guidato lo studio. “Per decenni, questa è rimasta una grande sfida per gli scienziati perché il sistema nervoso centrale del nostro corpo, che include il cervello e il midollo spinale, non ha alcuna capacità significativa di ripararsi dopo un infortunio o dopo l’insorgenza di una malattia degenerativa. Andremo direttamente alla FDA per avviare il processo per ottenere l’approvazione di questa nuova terapia per l’uso in pazienti umani che attualmente hanno pochissime opzioni di trattamento”.
Stupp è Professore di scienze e ingegneria dei materiali, chimica, medicina e ingegneria biomedica presso la Northwestern, dove è Direttore fondatore del Simpson Querrey Institute for BioNanotechnology (SQI) e del suo centro di ricerca affiliato, il Center for Regenerative Nanomedicine. Ha incarichi presso la McCormick School of Engineering, il Weinberg College of Arts and Sciences e la Feinberg School of Medicine.
Un topo paralizzato (a sinistra) trascina le zampe posteriori, rispetto a un topo paralizzato che ha riacquistato la capacità di muovere le zampe dopo aver ricevuto la terapia iniettabile della Northwestern. Credito: Samuel I. Stupp Laboratory/Northwestern University
Gravi lesioni del midollo spinale: l’aspettativa di vita non è migliorata dagli anni ’80
Secondo il National Spinal Cord Injury Statistical Center, quasi 300.000 persone vivono attualmente con una lesione del midollo spinale negli Stati Uniti. La vita per questi pazienti può essere straordinariamente difficile. Meno del 3% delle persone con lesioni complete recupera le funzioni fisiche di base. E circa il 30% viene ri-ospedalizzato almeno una volta durante un dato anno dopo l’infortunio iniziale, con un costo medio di milioni di dollari per l’assistenza sanitaria a vita per paziente. L’aspettativa di vita per le persone con lesioni del midollo spinale è significativamente inferiore rispetto alle persone senza lesioni del midollo spinale e non è migliorata dagli anni ’80. “Volevo fare la differenza sugli esiti della lesione del midollo spinale e affrontare questo problema, dato l’enorme impatto che potrebbe avere sulla vita dei pazienti”, dice Samuel Stupp.
Le “molecole danzanti” colpiscono bersagli in movimento
Il segreto dietro la nuova terapia rivoluzionaria di Stupp è sintonizzare il movimento delle molecole, in modo che possano trovare e coinvolgere correttamente i recettori cellulari in costante movimento. Iniettata come un liquido, la terapia si gelifica immediatamente in una complessa rete di nanofibre che imitano la matrice extracellulare del midollo spinale. Abbinando la struttura della matrice, imitando il movimento delle molecole biologiche e incorporando segnali per i recettori, i materiali sintetici sono in grado di comunicare con le cellule.
“I recettori nei neuroni e in altre cellule si muovono costantemente”, ha detto Stupp. “L’innovazione chiave nella nostra ricerca, che non è mai stata fatta prima, è controllare il movimento collettivo di oltre 100.000 molecole all’interno delle nostre nanofibre. Facendo muovere, “danzare” o addirittura saltare temporaneamente le molecole da queste strutture, note come polimeri supramolecolari, sono in grado di connettersi in modo più efficace con i recettori”.
Le nanofibre contenenti molecole che portano due diversi segnali bioattivi (verde e arancione) impegnano più efficacemente i recettori cellulari (giallo e blu) a causa del rapido movimento delle molecole. Credito: Samuel I. Stupp Laboratory/Mark Seniw/Northwestern University
Stupp e il suo team hanno scoperto che la messa a punto del movimento delle molecole all’interno della rete di nanofibre per renderle più agili ha portato a una maggiore efficacia terapeutica nei topi paralizzati. I ricercatori hanno anche confermato che le formulazioni della loro terapia con movimento molecolare potenziato hanno ottenuto risultati migliori durante i test in vitro con cellule umane, indicando una maggiore bioattività e segnalazione cellulare.
Vedi anche:Lesioni midollo spinale: una proteina la chiave del recupero
“Dato che le cellule stesse e i loro recettori sono in costante movimento, puoi immaginare che le molecole che si muovono più rapidamente incontreranno questi recettori più spesso”, ha detto Stupp. “Se le molecole sono lente e non così ‘sociali’, potrebbero non entrare mai in contatto con le cellule”.
Un’iniezione, due segnali
Una volta connesse ai recettori, le molecole in movimento attivano due segnali a cascata, entrambi fondamentali per la riparazione del midollo spinale. Un segnale spinge le lunghe code dei neuroni nel midollo spinale, chiamate assoni, a rigenerarsi. Simile ai cavi elettrici, gli assoni inviano segnali tra il cervello e il resto del corpo. Recidere o danneggiare gli assoni può provocare la perdita di sensibilità nel corpo o addirittura la paralisi. La riparazione degli assoni, d’altra parte, aumenta la comunicazione tra il corpo e il cervello.
Il secondo segnale aiuta i neuroni a sopravvivere dopo la lesione perché fa proliferare altri tipi di cellule, promuovendo la ricrescita dei vasi sanguigni persi che alimentano i neuroni e le cellule critiche per la riparazione dei tessuti. La terapia induce anche la mielina a ricostruirsi intorno agli assoni e riduce la cicatrizzazione gliale, che agisce come una barriera fisica che impedisce la guarigione del midollo spinale.
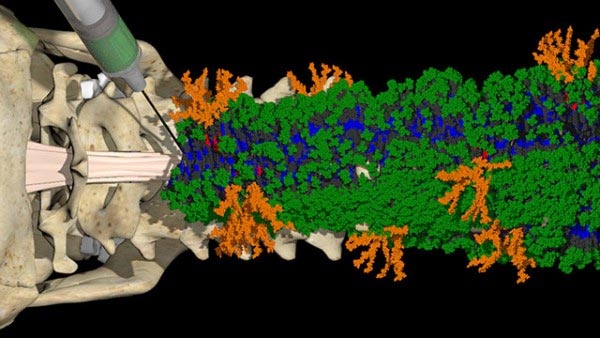
Una nuova terapia iniettabile forma nanofibre con due diversi segnali bioattivi (verde e arancione) che comunicano con le cellule per avviare la riparazione del midollo spinale danneggiato. Credito: illustrazione di Mark Seniw
“I segnali utilizzati nello studio imitano le proteine naturali necessarie per indurre le risposte biologiche desiderate. Tuttavia, le proteine hanno un’emivita estremamente breve e sono costose da produrre”, ha affermato Zaida Álvarez, la prima autrice dello studio. “I nostri segnali sintetici sono brevi peptidi modificati che, se legati insieme a migliaia, sopravviveranno per settimane per fornire bioattività. Il risultato finale è una terapia che è meno costosa da produrre e dura molto più a lungo”.
Ex Prof.ssa assistente di ricerca nel laboratorio di Stupp, Álvarez è ora visiting scholar presso SQI e ricercatore presso l’Istituto di Bioingegneria della Catalogna in Spagna.
Applicazione universale
Mentre la nuova terapia potrebbe essere utilizzata per prevenire la paralisi dopo traumi importanti (incidenti automobilistici, cadute, incidenti sportivi e ferite da arma da fuoco) e da malattie, Stupp ritiene che la scoperta sottostante – che il “movimento supramolecolare” è un fattore chiave nella bioattività – possa essere applicato ad altre terapie e bersagli.
“I tessuti del sistema nervoso centrale che abbiamo rigenerato con successo nel midollo spinale ferito sono simili a quelli del cervello colpiti da ictus e malattie neurodegenerative, come la SLA, il morbo di Parkinson e l’ Alzheimer“, ha detto Stupp. “Oltre a ciò, la nostra scoperta fondamentale sul controllo del movimento degli assemblaggi molecolari per migliorare la segnalazione cellulare potrebbe essere applicata universalmente a bersagli biomedici”.
Altri autori dello studio nordoccidentale includono Evangelos Kiskinis, assistente professore di neurologia e neuroscienze a Feinberg; tecnico di ricerca Feng Chen; i ricercatori postdottorato Ivan Sasselli, Alberto Ortega e Zois Syrgiannis e gli studenti ora laureati Alexandra Kolberg-Edelbrock, Ruomeng Qiu e Stacey Chin. Peter Mirau dell’Air Force Research Laboratories e Steven Weigand dell’Argonne National Laboratory sono anche coautori.
Fonte:Science