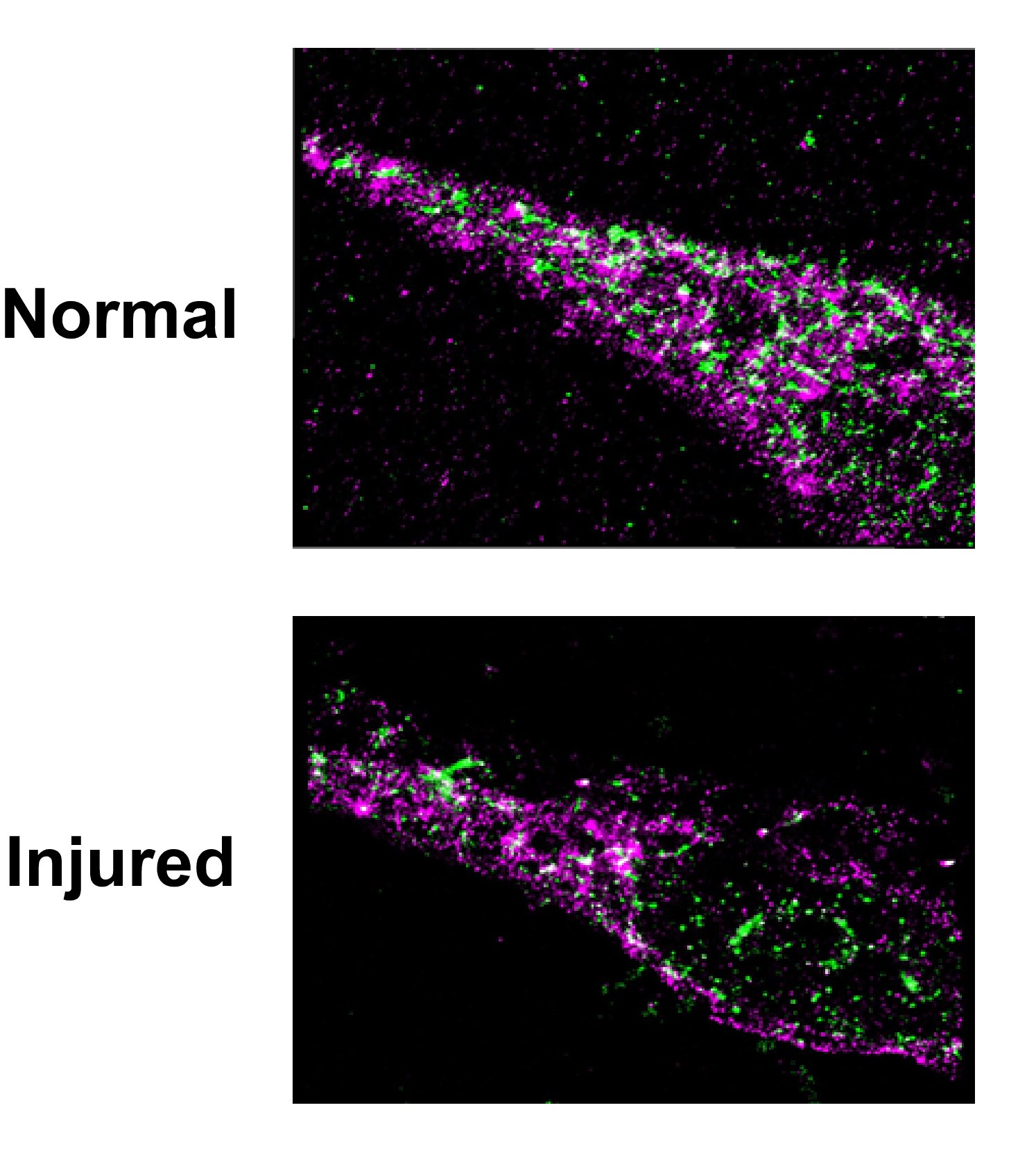
Immagine: Beta-arrestin2 (verde) si localizza con eNOS (viola) in cellule sane (pannello superiore); tuttavia, in seguito a lesioni (pannello inferiore), questa localizzazione viene persa. Credito: Dr. Don Rockey.
Il fegato filtra il sangue, disintossica i prodotti chimici e metabolizza i farmaci. L’epatite, l’alcol e le malattie epatiche primarie sono fonti comuni di danno al fegato e possono causare cicatrici, note come fibrosi. La fibrosi a lungo termine può portare a tessuto epatico più spesso che a sua volta porta ad altri problemi come l’aumento della pressione sanguigna nel fegato. Conosciuta come ipertensione portale, l’ipertensione nel fegato è spesso non riconosciuta e può essere letale.
I ricercatori della Medical University of South Carolina (MUSC) che studiano questa malattia del fegato, hanno analizzato un meccanismo che regola l’attività dell’ossido nitrico sintasi endoteliale (eNOS), un enzima che produce ossido nitrico (NO).
I loro risultati, pubblicati di recente negli Atti della National Academy of Sciences, hanno mostrato che beta-arrestin2 (beta-Arr2) agisce come una proteina di ponteggio per attivare eNOS, portando ad un aumento della sintesi di NO. In caso di danno epatico, i livelli di beta-Arr2 sono ridotti nelle cellule epiteliali causando un’interruzione della sintesi di NO e un aumento dell’ipertensione portale. Questa ricerca mostra che beta-Arr2 è un potenziale bersaglio terapeutico. “I meccanismi molecolari che regolano la funzione eNOS sono complessi e probabilmente variano nella normalità e nella malattia”, ha affermato C. Rockey, M.D., Professore e Presidente del Dipartimento di Medicina del MUSC, che studia la fibrosi epatica e l’ipertensione portale.
Vedi anche: Malattia del fegato grasso, svelato un mistero
Il Rockey Lab si concentra sulla comprensione dei meccanismi alla base dell’ipertensione portale. Le cellule endoteliali sinusoidali del fegato (SEC) svolgono un ruolo critico nell’omeostasi epatica. Le SEC controllano la pressione sanguigna e il flusso attraverso la produzione di NO, prodotta da eNOS. Come molecola di segnalazione, beta-Arr2 influenza eNOS, ma non è chiaro come queste proteine interagiscano per influenzare la produzione di NO.
L’attuale lavoro ha delineato il ruolo di beta-Arr2 nella regolazione dell’attività di eNOS. Nelle cellule endoteliali sinusoidali del fegato normali e sane, beta-Arr2 ha attivato eNOS. Al contrario, nelle cellule endoteliali sinusoidali del fegato ferite, i ricercatori hanno mostrato una riduzione significativa dei livelli di beta-Arr2 e una riduzione dell’attività eNOS. È interessante notare che la sovraespressione di beta-Arr2 ha migliorato la produzione di NO nelle cellule endoteliali sinusoidali del fegato normali e ferite. Inoltre, i topi privi di beta-Arr2 avevano una significativa riduzione dell’area sinusoide, evidenziando gli effetti fisiologici della ridotta attività eNOS. Insieme, questi dati mostrano che beta-Arr2 è un regolatore critico dell’attività eNOS.
Precedenti lavori del laboratorio Rockey hanno dimostrato che i recettori accoppiati alle proteine G (o GPCR) sono un potente attivatore di eNOS. L’esame della localizzazione di GIT-1 ha rivelato che GIT-1, beta-Arr2 ed eNOS si localizzano tutti insieme in SEC. È importante sottolineare che la perdita di beta-Arr2 ha impedito l’attivazione di GIT-1 e la successiva attivazione di eNOS. Pertanto, beta-Arr2 agisce come una proteina di ponteggio per aiutare ad attivare GIT-1 e a sua volta attivare eNOS.
In sintesi, le cellule endoteliali sinusoidali del fegato SEC sane producono NO stimolando il beta-Arr2, che quindi forma un signalosome, un complesso proteico attivo che aiuta a trasdurre i segnali cellulari, per attivare GIT-1. Il GIT-1 attivo a sua volta attiva eNOS per produrre ossido nitrico. Al contrario, durante la lesione epatica, i livelli di beta-Arr2 sono ridotti e questo percorso è perturbato.
“Il grande messaggio è che la segnalazione eNOS è complessa ed è controllata da più meccanismi ed è disregolata dopo l’infortunio delle cellule endoteliali”, ha detto Rockey.
Come componente centrale dell’asse di segnalazione eNOS, beta-Arr2 ha il potenziale per essere un nuovo obiettivo terapeutico per il ripristino della funzione SEC. Tuttavia, prima che un potenziale terapeutico arrivi in clinica, rimangono ancora alcune domande sulla biologia di beta-Arr2. Come scaffold di segnalazione che attiva eNOS, è importante determinare quali altre proteine interagiscono con beta-Arr2. Inoltre, il laboratorio Rockey sta perseguendo i meccanismi che influenzano la localizzazione e / o l’attività di beta-Arr2.