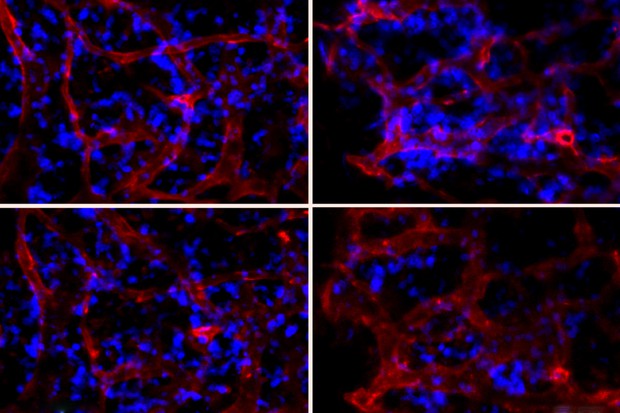
(Interferenza dell’RNA-Immagine: nella foto in alto a destra, il midollo osseo non è ancora trattato con particelle che disattivano il gene chiamato SDF1. In basso a destra, il numero di neutrofili (blu) diminuisce, indicando che sono stati rilasciati dal midollo osseo dopo il trattamento. A sinistra, il trattamento con una nanoparticella di controllo non influisce sul numero di neutrofili prima e dopo il trattamento.Credit: MIT).
L’interferenza dell’RNA o RNA interference (RNAi) è un meccanismo mediante il quale alcuni frammenti di RNA sono in grado di interferire (e spegnere) l’espressione genica.
Vedi anche:Nuovi promettenti veicoli per la consegna della terapia genica
Utilizzando nanoparticelle specializzate, gli ingegneri del MIT hanno sviluppato un modo per disattivare geni specifici nelle cellule del midollo osseo, che svolgono un ruolo importante nella produzione di cellule del sangue. “Queste nanoparticelle potrebbero essere adattate per aiutare a trattare le malattie cardiache o per aumentare la resa di cellule staminali nei pazienti che necessitano di trapianti di cellule staminali”, affermano i ricercatori.
Questo tipo di terapia genica, nota come interferenza dell’RNA, è solitamente difficile da indirizzare ad organi diversi dal fegato, dove le nanoparticelle tenderebbero ad accumularsi. I ricercatori del MIT sono stati in grado di modificare le loro particelle in modo tale che si accumulassero nelle cellule del midollo osseo.
“Se riusciamo a fare in modo che queste particelle colpiscano altri organi di interesse, potrebbe esserci una gamma più ampia di applicazioni in diverse malattie. Quello che ci interessava veramente in questo studio era il midollo osseo che è un sito per l’emopoiesi delle cellule del sangue che danno origine a un’intera linea di cellule che contribuiscono a vari tipi di malattie”, afferma Michael Mitchell, ex postdoc del MIT e uno degli autori principali dello studio.
In uno studio sui topi, i ricercatori hanno dimostrato di poter utilizzare questo approccio per migliorare il recupero dopo un attacco di cuore inibendo il rilascio di cellule del sangue del midollo osseo che promuovono l’infiammazione e contribuiscono alle malattie cardiache.
Marvin Krohn-Grimberghe, cardiologo presso il Freiburg University Heart Center in Germania, e Maximilian Schloss, ricercatore presso il Massachusetts General Hospital, sono anche gli autori principali dell’articolo, che appare su Nature Biomedical Engineering. Gli autori senior del documento sono Daniel Anderson, Professore di ingegneria chimica al MIT e membro del Koch Institute for Integrative Cancer Research e Institute for Medical Engineering and Science del MIT, e Matthias Nahrendorf, Professore di radiologia presso MGH.
Mirare al midollo osseo
L’interferenza dell’RNA è una strategia che potrebbe essere utilizzata per trattare una varietà di malattie fornendo brevi filamenti di RNA che bloccano l’attivazione di geni specifici in una cellula. Finora, il più grande ostacolo a questo tipo di terapia è stata la difficoltà di erogarla alla parte destra del corpo. Quando vengono iniettate nel flusso sanguigno, le nanoparticelle che trasportano l’RNA tendono ad accumularsi nel fegato, cosa di cui alcune aziende biotecnologiche hanno approfittato per sviluppare nuovi trattamenti sperimentali per le malattie del fegato.
Il laboratorio di Anderson, in collaborazione con il Professor Robert Langer dell’Istituto del MIT, che è anche autore del nuovo studio, ha precedentemente sviluppato un tipo di nanoparticelle polimeriche in grado di fornire RNA ad organi diversi dal fegato. Le particelle sono rivestite di lipidi che aiutano a stabilizzarle e possono colpire organi come i polmoni, il cuore e la milza, a seconda della composizione delle particelle e del peso molecolare.
“Le nanoparticelle di RNA sono attualmente approvate dalla FDA come terapia mirata al fegato, ma sono promettenti per molte malattie, che vanno dai vaccini Covid-19 ai farmaci che possono riparare in modo permanente i geni che causano diverse malattie”, dice Anderson. “Riteniamo che l’ingegneria delle nanoparticelle per fornire RNA a diversi tipi di cellule e organi del corpo sia la chiave per raggiungere il più ampio potenziale della terapia genica“.
Nel nuovo studio, i ricercatori hanno deciso di adattare le particelle in modo che potessero raggiungere il midollo osseo. Il midollo osseo contiene cellule staminali che producono molti diversi tipi di cellule del sangue, attraverso un processo chiamato emopoiesi. Stimolare questo processo potrebbe aumentare la resa di cellule staminali ematopoietiche per il trapianto di cellule staminali, mentre reprimerlo potrebbe avere effetti benefici sui pazienti con malattie cardiache o altre malattie.
“Se potessimo sviluppare tecnologie in grado di controllare l’attività cellulare nel midollo osseo e la nicchia delle cellule staminali ematopoietiche, potrebbe essere trasformativo per le applicazioni della strategia in diverse malattie”, afferma Mitchell, che ora è assistente Professore di bioingegneria presso l’Università della Pennsylvania.
I ricercatori hanno iniziato lo studio con le particelle che avevano precedentemente utilizzato per colpire i polmoni e hanno creato varianti con diverse disposizioni di un rivestimento superficiale chiamato polietilenglicole (PEG). Hanno testato 15 di queste particelle e ne hanno trovata una che era in grado di evitare di essere catturata nel fegato o nei polmoni e che poteva effettivamente accumularsi nelle cellule endoteliali del midollo osseo. Hanno anche dimostrato che l’RNA trasportato da questa particella potrebbe ridurre l’espressione di un gene bersaglio fino all’80%.
I ricercatori hanno testato questo approccio con due geni che ritenevano potesse essere utile abbattere. Il primo gene bersaglio SDF1, è una molecola che normalmente impedisce alle cellule staminali ematopoietiche di lasciare il midollo osseo. La disattivazione di questo gene potrebbe ottenere lo stesso effetto dei farmaci che i medici spesso usano per indurre il rilascio di cellule staminali ematopoietiche nei pazienti che devono sottoporsi a trattamenti con radiazioni per i tumori del sangue. Queste cellule staminali vengono successivamente trapiantate per ripopolare le cellule del sangue del paziente.
“Se hai un modo per abbattere SDF1, puoi causare il rilascio di queste cellule staminali ematopoietiche che potrebbe essere molto importante per un trapianto in modo da poterne raccogliere di più dal paziente”, dice Mitchell.
I ricercatori hanno dimostrato che quando hanno usato le loro nanoparticelle per abbattere SDF1, potrebbero aumentare di cinque volte il rilascio di cellule staminali ematopoietiche, che è paragonabile ai livelli raggiunti dai farmaci che ora vengono utilizzati per migliorare il rilascio di cellule staminali. Hanno anche dimostrato che queste cellule possono differenziarsi con successo in nuove cellule del sangue quando vengono trapiantate in un altro topo.
“Siamo molto entusiasti degli ultimi risultati”, afferma Langer, che è anche Professore al David H. Koch Institute presso il MIT. “In precedenza abbiamo sviluppato approcci di sintesi e screening ad alto rendimento per colpire le cellule del fegato e dei vasi sanguigni e ora in questo studio, il midollo osseo. Ci auguriamo che questo porti a nuovi trattamenti per malattie del midollo osseo come il mieloma multiplo e altre malattie “.
Combattere le malattie cardiache
Il secondo gene che i ricercatori hanno preso di mira per il knockdown è chiamato MCP1, una molecola che svolge un ruolo chiave nelle malattie cardiache. Quando MCP1 viene rilasciato dalle cellule del midollo osseo dopo un attacco di cuore, stimola un flusso di cellule immunitarie a lasciare il midollo osseo e viaggiare verso il cuore, dove promuovono l’infiammazione e possono portare a ulteriori danni al cuore.
In uno studio sui topi, i ricercatori hanno scoperto che fornire RNA mirato a MCP1 riduceva il numero di cellule immunitarie che andavano al cuore dopo un infarto. I topi che hanno ricevuto questo trattamento hanno anche mostrato una migliore guarigione del tessuto cardiaco dopo un infarto.
“Ora sappiamo che le cellule immunitarie svolgono un ruolo fondamentale nella progressione dell’infarto e dell’insufficienza cardiaca”, afferma Mitchell. “Se potessimo sviluppare strategie terapeutiche per impedire alle cellule immunitarie che provengono dal midollo osseo di entrare nel cuore, potrebbe essere un nuovo mezzo per curare l’attacco di cuore. Questa è una delle prime dimostrazioni di un approccio basato sull’acido nucleico per farlo”.
Nel suo laboratorio presso l’Università della Pennsylvania, Mitchell sta ora lavorando a nuove nanotecnologie che prendono di mira il midollo osseo e le cellule immunitarie per il trattamento di altre malattie, in particolare i tumori del sangue come il mieloma multiplo.
La ricerca è stata finanziata in parte dal National Institutes of Health.
I ricercatori del MIT hanno dimostrato di poter fornire nanoparticelle di RNAi al midollo osseo, influenzandone la funzione. Nella foto in alto a destra, il midollo osseo non è ancora trattato con particelle che disattivano il gene chiamato SDF1. In basso a destra, il numero di neutrofili (blu) diminuisce, indicando che sono stati rilasciati dal midollo osseo dopo il trattamento. A sinistra, il trattamento con una nanoparticella di controllo non influisce sul numero di neutrofili prima e dopo il trattamento.