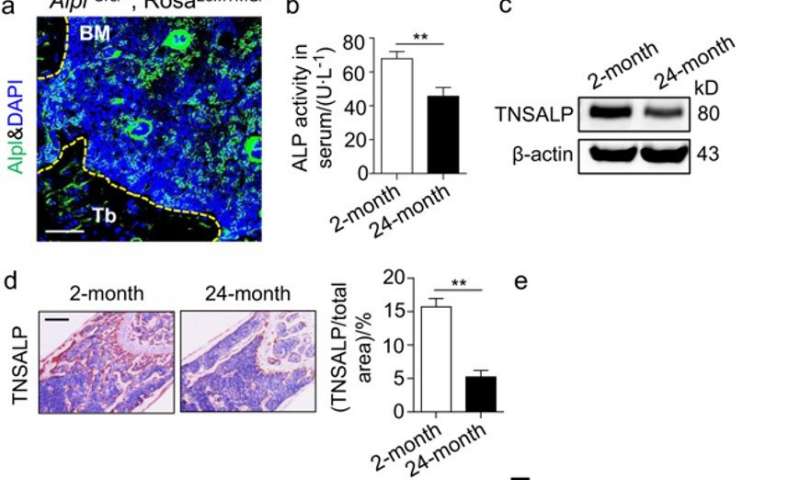
Immagini: l’espressione di Alpl è diminuita nel midollo osseo con l’età. a) Immagine rappresentativa dell’immunocolorazione che mostra Alpl (verde) nel midollo osseo (BM) dei topi 2 mesi, bc) Attività ALP nei livelli di espressione nel siero e nel TNSALP nel midollo osseo di giovani (2 mesi) e anziani (24 -month) topi analizzati con il test di attività ALP e Western blotting ha mostrato diminuita espressione proteica con l’età, d) Analisi immunoistochimica di TNSALP (marrone) della diafisi femorale, e) L’area quantificata di TNSALP + è diminuita con l’età. Credito: Bone Research.
Mutazioni del gene della fosfatasi alcalina (ALPL) nel fegato, ossa e reni possono causare l’ ipofosfatasia (HPP) e la displasia ossea a esordio precoce, affermando il suo ruolo chiave nello sviluppo osseo umano. Nonostante la sua importanza, il suo meccanismo d’azione durante l’invecchiamento osseo è in gran parte sconosciuto. In un recente studio pubblicato su Bone Research, Wenjia Liu e collaboratori presso l’Istituto Xi’an di ingegneria dei tessuti e medicina rigenerativa hanno dimostrato che il knockdown del gene ALPL ha indotto caratteristiche di invecchiamento osseo prematuro, tra cui perdita di massa ossea e guadagno di grasso nel midollo. Il fenomeno è stato accompagnato da una differenziazione delle cellule staminali mesenchimali (MSC). Gli scienziati hanno quindi riattivato il percorso utilizzando la metformina, farmaco contro il diabete, per ripristinare la capacità delle cellule staminali di crescere e differenziarsi in osteoblasti produttori di ossa e prevenire l’invecchiamento osseo.
Le MSC sono precursori degli osteoblasti produttori di ossa e la proteina codificata dal gene ALPL è arricchita nella membrana delle cellule staminali, con coinvolgimento nel metabolismo dell’ATP durante il differenziamento cellulare. Liu ha determinato il meccanismo dell’invecchiamento osseo con studi di perdita di funzione, in cui la carenza di ALPL nelle cellule staminali ha migliorato il rilascio di ATP, riducendo al contempo la sua idrolisi per causare un aumento extracellulare di ATP. L’ATP, quando internalizzato dalle MSC, ha disattivato la via di segnalazione delle cellule AMPKα (regolatore principale dell’omeostasi dell’energia cellulare), contribuendo all’interruzione del destino cellulare delle cellule MSC, compromettendone la capacità di crescere e proliferare. Il lavoro è stato condotto in vitro e in un modello di topo mutante (Alpl + / –) che mostra invecchiamento precoce, seguito dal trattamento con metformina per migliorare la funzione delle MSC endogene riattivando la via di segnalazione cellulare.
La fosfatasi alcalina (ALP) fu inizialmente identificata nel 1912 come un ectoenzima onnipresente ampiamente distribuito in natura dai batteri agli esseri umani. L’ALP è un marker osteoblastico noto come indice diagnostico per rilevare la capacità di formazione dell’osso nell’osteoporosi. Gli studi genetici che studiano ALPL nell’uomo e nei topi hanno implicato fortemente la necessità del gene nella formazione dell’osso postnatale e che le deformità ossee erano correlate al grado di deficit di ALPL. Sebbene la funzione di ALPL sia stata stabilita nello sviluppo osseo, il suo ruolo nell’invecchiamento osseo è rimasto sconosciuto.
L’invecchiamento osseo è il principale fattore di osteoporosi che determina anche una diminuzione della massa ossea e un aumento del grasso. Le cellule staminali mesenchimali del midollo osseo sono progenitori comuni di osteoblasti e adipociti, sottoposti a senescenza a livello cellulare durante l’invecchiamento osseo. Studi precedenti hanno dimostrato che il salvataggio della funzione delle MSC ha avuto un significativo impatto terapeutico sulla capacità rigenerativa e sulla massa ossea. Tuttavia, il modo in cui ALPL ha orchestrato la differenziazione e la senescenza delle MSC per influenzare l’invecchiamento osseo è rimasto elusivo.
( Vedi anche: Osteoporosi: scoperto nuovo trattamento che aumenta la formazione di tessuto osseo).
Nel presente studio, gli autori si sono concentrati sull’espressione di ALP insieme al tessuto non specifico ALP (TNSALP) che è codificato come marcatore di superficie cellulare per identificare e isolare cellule staminali che formano le ossa. L’espressione e l’attività combinate sono state rilevate utilizzando saggi di attività ALP, western blotting e immunoistochimica nei modelli di topo anziani. Gli scienziati hanno dimostrato che l’invecchiamento osseo era associato a una ridotta espressione di Alpl nel midollo osseo .
Gli autori hanno utilizzato modelli di topo knockout per studiare il ruolo di Alpl nell’invecchiamento osseo (Alpl knockout: Alpl + / – ). Rispetto al gruppo wild type, i topi knockout hanno mostrato una riduzione di quasi il 50% dell’attività ALP sierica e hanno imitato l’invecchiamento osseo prematuro, accompagnato da perdita di massa ossea correlata all’età e guadagno di grasso midollare. Lo studio ha inoltre dimostrato che nelle MSC, Alpl ha prevenuto la sensibilità all’invecchiamento osseo regolando specificamente la senescenza e il differenziamento cellulare per governare l’equilibrio osteo-adipogenico delle cellule staminali del midollo osseo.
Poiché lo studio ha dimostrato che sia il pathway di Alpl che quello di AMPKα regolavano la funzione delle MSC, è stata introdotta la metformina, un attivatore comune del pathway AMPKa. La metformina è comunemente nota come farmaco di prima linea utilizzato per il trattamento del diabete di tipo 2, recentemente usato come farmaco anti-invecchiamento poichè estendeva con successo la longevità e la durata della vita nei topi sperimentali .
Nello studio, la metformina ha dimostrato una maggiore capacità di salvare la differenziazione in MSC knockdown in vitro e in topi knockdown in vivo, rispetto al potenziale terapeutico alternativo ricercato attraverso la sovraespressione del gene Alpl. In particolare, le iniezioni di metformina nella cavità del midollo osseo hanno salvato con successo la funzione compromessa delle MSC endogene, impedendo nel contempo l’invecchiamento osseo prematuro in Alpl +/-topi mutanti.
Collettivamente, gli autori hanno rivelato un ruolo precedentemente non riconosciuto del gene Alpl nella prevenzione dell’invecchiamento osseo, con alterazioni funzionali mediate da ATP nelle MSC e il potenziale del trattamento con metformina come terapia efficace nell’invecchiamento osseo carente di Alpl. I futuri studi meccanicistici a livello cellulare esploreranno il modo in cui Alpl regola la capacità delle MSC di rilasciare ATP e l’impatto più ampio della carenza di Alpl su altri organi.
Fonte: Nature