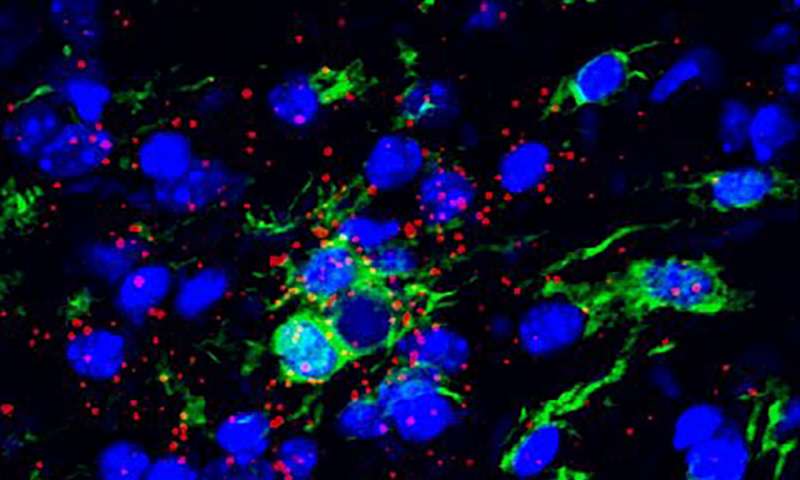
Immagine: immagine rappresentativa al microscopio confocale del corno ventrale del midollo spinale da un topo SLA. Diverse cellule microgliali (verdi) si infiltrano nel midollo spinale man mano che la malattia di SLA progredisce. FISH a singola molecola ha rilevato IRF7 (un gene inducibile dall’interferone) molecole di RNA (rosse) nella microglia e in altre cellule. Credito: Valeria Gerbino / Maniatis lab / Columbia’s Zuckerm.
Gli scienziati della Columbia hanno fornito nuove informazioni su come le mutazioni in un gene chiamato TBK1 causino la sclerosi laterale amiotrofica (SLA), una malattia neurodegenerativa progressiva che ruba il movimento ai pazienti, il linguaggio e, in definitiva, le loro vite. I ricercatori hanno scoperto che le mutazioni TBK1 associate alla SLA possono avere effetti sia positivi che negativi sulla progressione della malattia nei topi geneticamente modificati per avere sintomi simili alla SLA.
Questi risultati, riportati oggi in Neuron, forniscono intuizioni sia genetiche che meccanicistiche che potrebbero portare a nuove strategie per lo sviluppo di trattamenti per la SLA.
“Una delle maggiori sfide per trovare una cura per la SLA sta nell’ uso di dati genetici per comprendere i meccanismi alla base della malattia”, ha detto l’autore senior dello studio, Tom Maniatis, Ph.D., uno dei principali ricercatori del Mortimer B. Zuckerman Mind Brain Behaviour della Columbia Istituire. “Ad esempio, le malattie neurodegenerative come la SLA coinvolgono più tipi di cellule che cambiano costantemente man mano che la malattia progredisce, quindi un farmaco che è utile nelle prime fasi della malattia potrebbe essere dannoso in tempi successivi. Il nostro studio fornisce uno sguardo alla complessa relazione tra la genetica della SLA e i suoi meccanismi, ed evidenzia la sfida nello sviluppo di farmaci sicuri ed efficaci per il trattamento della malattia “, ha commentato il Dott. Maniatis, Isidore S. Edelman, Professore di biochimica presso il Vagelos College of Physicians and Surgeons del Columbia.
Vedi anche: Gli scienziati scoprono il legame tra i geni che causano la SLA
La SLA è una malattia che può essere innescata dall’accumulo di proteine mal ripiegate nei motoneuroni, le cellule nervose nel midollo spinale che guidano il movimento. Il gene TBK1 umano è uno degli oltre 25 geni che sono stati associati o causano la SLA quando sono portatori di una mutazione. TBK1 è un attore centrale in molteplici funzioni cellulari, tra cui l’autofagia, un processo che rimuove le proteine mal ripiegate, i frammenti di cellule danneggiati e i patogeni batterici. TBK1 è anche richiesto per la risposta antimicrobica dell’interferone, che protegge le cellule dalle infezioni batteriche e virali.
“TBK1 aiuta le cellule a eliminare i grumi di proteine mal ripiegate e difende il corpo dall’invasione di virus e batteri”, ha dichiarato Valeria Gerbino, Ph.D., ricercatrice associata nel laboratorio Maniatis e autrice principale del documento. “E poiché gli individui con determinate mutazioni in TBK1 hanno la SLA, volevamo sviluppare una profonda comprensione meccanicistica di come queste mutazioni influenzano le funzioni cellulari nel midollo spinale nel corso della malattia”.
Lavorando in collaborazione con The Jackson Laboratory, Drs. Maniatis e Gerbino, i ricercatori hanno inserito mutazioni TBK1 che causano la SLA nei topi. Questi topi non hanno mostrato segni di malattia dei motoneuroni. “Questo non è stato sorprendente, dal momento che solo alcune delle molte mutazioni di SLA umana testate finora nei topi da altri ricercatori della SLA hanno portato a malattie dei motoneuroni“, ha affermato Maniatis, che è anche Direttore della Precision Medicine Initiative della Columbia.
Nel tentativo di superare questo problema, i ricercatori hanno inserito le mutazioni TBK1 in un modello murino già consolidato di SLA: il topo SOD1. Il Dott. Gerbino e collaboratori dello Zuckerman Institute hanno quindi seguito la progressione della malattia in questi topi.
Questi nuovi topi hanno mostrato notevoli differenze nella progressione della malattia rispetto ai topi che portano solo le mutazioni SOD1. In particolare, l’insorgenza della malattia è iniziata prima. “Abbiamo scoperto che i topi portatori di mutazioni SOD1 e TBK1 presentavano anormalità nei movimenti precedenti rispetto a quelli portatori di sole mutazioni SOD1″, ha affermato il Dott. Gerbino. “Un esame più attento dei topi ha anche rivelato danni ai motoneuroni e perdita di connessioni muscolari prima del previsto”,
Per studiare ulteriormente questo fenomeno, gli scienziati hanno esaminato un altro gruppo di topi SOD1 SLA in cui il gene TBK1 è stato eliminato solo nei motoneuroni e non in altre cellule del midollo spinale. Il team ha scoperto che l’assenza di attività TBK1 nei soli neuroni motori ha portato alla perdita di autofagia in queste cellule. Questa perdita ha portato ad un aumento dell’accumulo di proteine dannose, morte precoce dei motoneuroni e perdita di connessioni neurone-muscolo. Queste osservazioni hanno dimostrato che l’insorgenza precoce della malattia era una conseguenza della perdita di TBK1 nei motoneuroni.
Il team ha quindi studiato con precisione in che modo le mutazioni di TBK1 hanno influenzato altre cellule del midollo spinale. I ricercatori hanno scoperto che la risposta dell’interferone era soppressa nelle cellule gliali, vale a dire astrociti e microglia. La risposta dell’interferone, sebbene fondamentale per la difesa dalle infezioni nelle persone sane, può essere tossica se prodotta in eccesso (come nel caso dei topi SLA) e può innescare una cascata di processi cellulari che sono tossici per i motoneuroni. “La perdita di TBK1 nella microglia e negli astrociti riduce chiaramente la risposta dell’interferone nel midollo spinale dei topi SLA”, ha dichiarato Maniatis, Direttore scientifico della famiglia Evnin e Amministratore delegato del New York Genome Center. “Questo si correla con l’estensione significativa delle loro vite”.
“Il nostro studio fornisce un esempio di come più percorsi all’interno e tra le cellule possano essere presi di mira attraverso la manipolazione di un singolo gene e come la modifica di questi percorsi nella SLA possa essere utile – o dannosa – in diverse fasi della progressione della malattia“, ha aggiunto Gerbino . Maniatis sostiene che questo tipo di ricerca fondamentale, sposterà l’ago verso trattamenti che si concentrano sui meccanismi sottostanti la SLA ed i suoi sintomi devastanti.
“Alla fine, tutte le malattie neurodegenerative iniziano con i geni”, ha dichiarato Maniatis. “Mentre continuiamo a raccogliere informazioni genetiche critiche, possiamo identificare mutazioni, come quelle di TBK1, che forniranno ulteriori approfondimenti meccanicistici. Questi geni e i percorsi che controllano saranno la chiave per lo sviluppo di farmaci che fanno la differenza nella vita dei pazienti SLA”.
L’articolo, “”The loss of TBK1 kinase activity in motor neurons or in all cell types differentially impacts ALS disease progression in SOD1 mice”, ha visto la collaborazione di Esther Kaunga, Junqiang Ye, Daniele Canzio, Sean O’Keeffe, Noam Rudnick, Paolo Guarnieri e Cathleen Lutz.
Fonte: EurekAlert