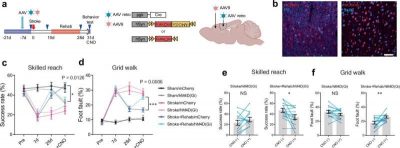
Immagine: neuroni che proiettano l’ictus sono necessari per il recupero funzionale indotto dalla riabilitazione. Credito: Nature Communications.
L’ictus è la causa principale di disabilità negli adulti, senza una terapia medica approvata che favorisca il recupero. Dal 70% all’80% delle persone che subiscono un ictus presenta una compromissione degli arti superiori e molte di loro non recuperano l’uso funzionale del braccio paretico, il che può portare a difficoltà nelle attività della vita quotidiana (ADL) e nell’impegno nella vita di comunità.
A differenza di gran parte della medicina moderna, come nel cancro, nelle malattie immunitarie o cardiache, non esiste una medicina per il recupero dall’ictus. La neuroriabilitazione ha il potenziale per migliorare il recupero dopo l’ictus, ma nella pratica clinica ha effetti limitati. La riabilitazione ha un’efficacia limitata a causa delle difficoltà di accesso, intensità, comorbilità e gravità dell’ictus. I progressi nel recupero e nella riabilitazione dall’ictus sono stati complessivamente modesti, come dimostrato dalla limitata efficacia in ampi studi clinici di riabilitazione. Per affrontare queste sfide, è fondamentale una comprensione completa dei circuiti, della fisiologia e dei sistemi molecolari alla base della riabilitazione dall’ictus.
Un nuovo studio condotto dall’UCLA Health ha scoperto quello che i ricercatori definiscono il primo farmaco in grado di riprodurre completamente gli effetti della riabilitazione fisica dopo un ictus nei modelli di topi.
I risultati, pubblicati su Nature Communications, hanno testato due farmaci candidati derivati dai loro studi sul meccanismo degli effetti cerebrali della riabilitazione, uno dei quali ha determinato un significativo recupero del controllo del movimento dopo un ictus nei topi.
L’ictus è la causa principale di disabilità negli adulti perché la maggior parte dei pazienti non si riprende completamente dagli effetti dell’ictus. Non esistono farmaci nel campo del recupero da ictus, che richiedono ai pazienti colpiti da ictus di sottoporsi a riabilitazione fisica, che ha dimostrato di essere solo modestamente efficace.
“L’obiettivo è avere un medicinale che i pazienti colpiti da ictus possano assumere e che produca gli effetti della riabilitazione“, ha affermato il Dott. S. Thomas Carmichael, autore principale dello studio, professore e Direttore del dipartimento di neurologia dell’UCLA.
“La riabilitazione dopo un ictus ha effetti limitati perché la maggior parte dei pazienti non riesce a sostenere l’intensità riabilitativa necessaria per il recupero da un ictus. Inoltre, il recupero da un ictus non è come nella maggior parte degli altri campi della medicina, in cui sono disponibili farmaci per curare la malattia, come la cardiologia, le malattie infettive o il cancro“, ha affermato Carmichael.
“La riabilitazione è un approccio di medicina fisica che esiste da decenni; dobbiamo far entrare la riabilitazione nell’era della medicina molecolare“, ha aggiunto.
Nello studio, Carmichael e il suo team hanno cercato di determinare in che modo la riabilitazione fisica migliorasse la funzionalità cerebrale dopo un ictus e se fosse possibile sviluppare un farmaco in grado di produrre gli stessi effetti.
Lavorando su modelli murini da laboratorio di ictus e con pazienti colpiti da ictus, i ricercatori dell’UCLA hanno identificato una perdita di connessioni cerebrali che l’ictus produce e che sono lontane dal sito del danno da ictus. Le cellule cerebrali situate a distanza dal sito dell’ictus si disconnettono dagli altri neuroni. Di conseguenza, le reti cerebrali non si attivano insieme per cose come il movimento e l’andatura.
Il team dell’UCLA ha scoperto che alcune delle connessioni che si perdono dopo un ictus si verificano in una cellula chiamata neurone parvalbuminico. Questo tipo di neurone aiuta a generare un ritmo cerebrale, definito oscillazione gamma, che collega i neuroni insieme in modo che formino reti coordinate per produrre un comportamento, come il movimento.
L’ictus fa sì che il cervello perda le oscillazioni gamma. La riabilitazione fisica di successo sia nei topi da laboratorio che negli esseri umani, ha riportato le oscillazioni gamma nel cervello e, nel modello murino, ha riparato le connessioni perse dei neuroni della parvalbumina.
Carmichael e il team hanno poi identificato due farmaci candidati che potrebbero produrre oscillazioni gamma dopo l’ictus. Questi farmaci agiscono specificamente per eccitare i neuroni della parvalbumina.
I ricercatori hanno scoperto che uno dei farmaci, il DDL-920, sviluppato nel laboratorio dell’UCLA da Varghese John, coautore dello studio, ha prodotto un significativo recupero nel controllo del movimento nei topi.
Leggi anche:Sotagliflozin: primo farmaco a ridurre sia attacchi cardiaci che ictus
Spiegano gli autori:
“La disabilità motoria è una compromissione critica nei pazienti colpiti da ictus. La riabilitazione ha un effetto limitato sul recupero; ma non esiste una terapia medica per il recupero post-ictus. I meccanismi biologici della riabilitazione nel cervello rimangono sconosciuti. Qui, utilizzando un modello di ictus fototrombotico nei topi maschi, dimostriamo che la riabilitazione dopo un ictus migliora selettivamente la formazione di sinapsi nei neuroni interneuroni parvalbuminici presinaptici e nei neuroni postsinaptici nell’area motoria dell’arto anteriore rostrale con proiezioni assonali all’area motoria dell’arto anteriore caudale dove è stato indotto l’ictus (neurone che proietta l’ictus). La riabilitazione migliora le prestazioni motorie e la connettività funzionale neuronale, mentre l’inibizione dei neuroni che proiettano l’ictus diminuisce il recupero motorio. I neuroni che proiettano l’ictus mostrano una densità ridotta delle spine dendritiche, input sinaptici esterni ridotti e una percentuale inferiore di sinapsi parvalbuminica nell’input GABAergico totale. Gli interneuroni parvalbuminici regolano la connettività funzionale neuronale e la loro attivazione durante l’allenamento è necessaria per il recupero. Inoltre, l’oscillazione gamma, un ritmo regolato dalla parvalbumina, aumenta con il recupero indotto dalla riabilitazione negli animali dopo un ictus e nei pazienti colpiti da ictus. Il potenziamento farmacologico della funzione delle interneuroni della parvalbumina migliora il recupero motorio dopo un ictus, riproducendo il recupero della riabilitazione. Questi risultati identificano i circuiti cerebrali che mediano la riabilitazione-recupero e la possibilità di una selezione razionale di agenti farmacologici per fornire la prima terapia di riabilitazione molecolare“.
Questo studio ha due aree principali di impatto: in primo luogo, identifica un substrato cerebrale e un circuito che sta alla base dell’effetto della riabilitazione nel cervello. In secondo luogo, il documento identifica quindi un bersaglio farmacologico unico in questo circuito cerebrale riabilitativo per promuovere il recupero imitando l’effetto principale della riabilitazione fisica.
Sono necessari ulteriori studi per comprendere la sicurezza e l’efficacia del DDL-920 prima che possa essere preso in considerazione per la sperimentazione sull’uomo.
Fonte: Nature Communications