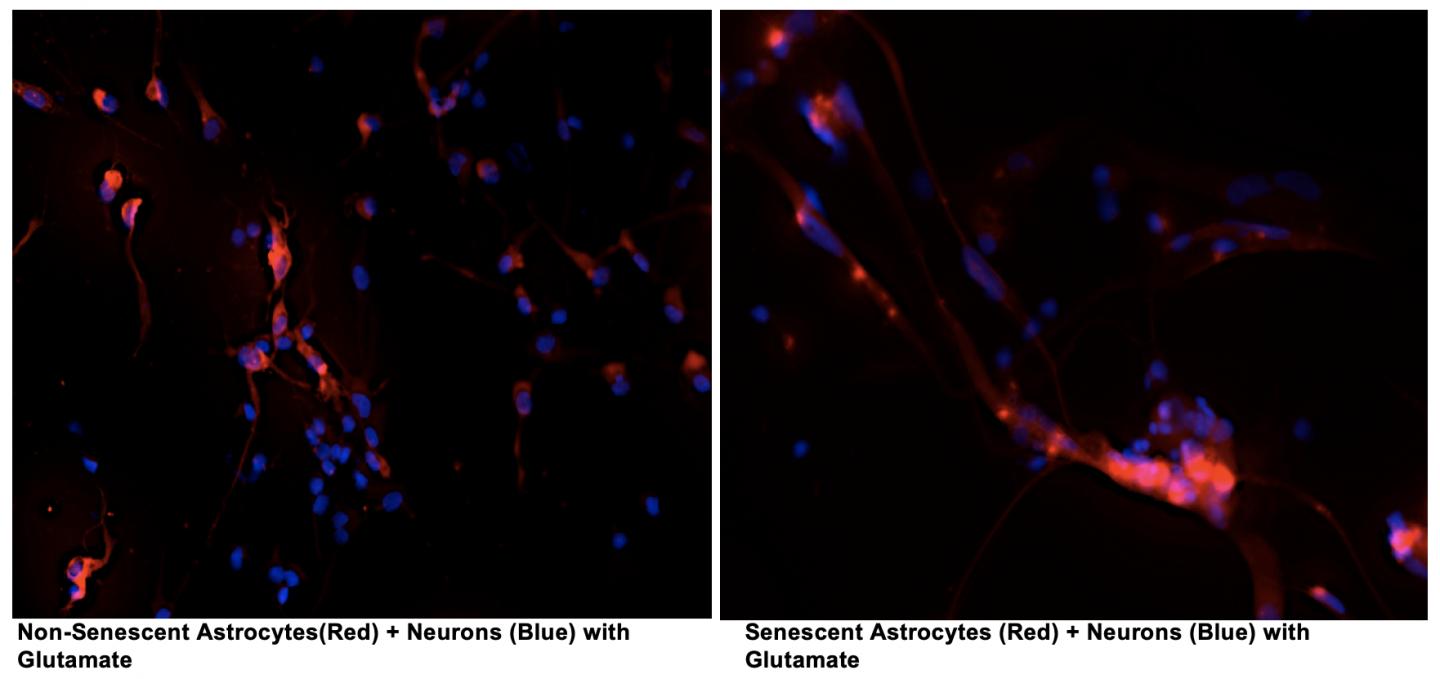
Immagine: astrociti non senescenti o senescenti (rosso) co-coltivati con neuroni (blu) in presenza di glutammato. Gli astrociti senescenti compromettono la sopravvivenza dei neuroni in presenza di glutammato. Credito Chandani Limbad, PhD
Sebbene sia stato stabilito un legame tra infiammazione cronica e malattie neurodegenerative, ci sono ancora molte domande aperte su come la senescenza cellulare, un processo in cui le cellule che smettono di dividersi sotto stress emettono un mix di proteine infiammatorie, influenza queste patologie.
In un articolo pubblicato su PLOS ONE, i ricercatori del Buck Institute riportano che la senescenza negli astrociti, il tipo di cellula più abbondante nel cervello, porta a “eccitotossicità” dannosa nei neuroni corticali coinvolti nella memoria. Questa ricerca, condotta dal ricercatore Chandani Limbad, PhD, ha scoperto che la senescenza cellulare negli astrociti sottoregola i trasportatori di glutammato, che sono vitali per l’omeostasi del glutammato nel cervello. Il glutammato è uno dei neurotrasmettitori più importanti nel cervello, ma l’eccesso di glutammato fa sì che i neuroni sparino ripetutamente segnali portando alla loro eventuale morte.
Memantina, un farmaco approvato dalla FDA per la malattia di Alzheimer, riduce la tossicità del glutammato nei pazienti che soffrono di malattia da moderata a grave per un massimo di un anno, ma l’evidenza che il farmaco potrebbe rallentare la patologia è debole. “Questo studio arriva ai meccanismi sottostanti che guidano la tossicità”, ha affermato l’autore senior dello studio Prof.ssa Judith Campisi, PhD. “Abbiamo identificato obiettivi nuovi che potrebbero essere più utili per lo sviluppo di farmaci”.
La senescenza cellulare è uno degli argomenti più importanti nella ricerca sull’invecchiamento. Il successo nel laboratorio di Campisi e in altre parti del mondo ha dato origine a società e progetti di ricerca volti a sviluppare senolitici, farmaci che eliminano le cellule senescenti o senomorfici, farmaci che sopprimono l’infiammazione associata alla senescenza. Un lavoro precedente nel laboratorio di Campisi in collaborazione con il laboratorio Andersen del Buck Institute ha mostrato che l’eliminazione delle cellule senescenti ha prevenuto il Parkinson in un modello murino della malattia.
Vedi anche, Invecchiamento: nuova comprensione del normale declino cognitivo e neurodegenerazione
Campisi rivela che la maggior parte della ricerca mirava a comprendere le caratteristiche della senescenza cellulare coinvolgendo fibroblasti umani, cellule del tessuto connettivo che producono collagene e altre fibre. Il ricercatore spiega che invece, la sua ricerca sugli astrociti dovrebbe essere un campanello d’allarme per coloro che studiano il morbo di Alzheimer, sostenendo che “Ciò che viene comunemente chiamato morbo di Alzheimer non familiare dovrebbe probabilmente essere definito con più precisione demenza correlata all’età. Se vedete cinque pazienti con Alzheimer, tutti si presentano in modo diverso. Alcuni hanno cambiamenti di personalità, altri no. La memoria è influenzata in modo diverso in ogni paziente; alcune persone perdono il controllo motorio, altri no. Questi risultati evidenziano l’invecchiamento come il più grande fattore di rischio per quasi tutta la neurodegenerazione ed è su questo che la ricerca dovrebbe essere focalizzata “.
Il co-autore dello studio Pierre-Yves Desprez, PhD, consulente scientifico nel laboratorio Campisi, che gestisce anche un laboratorio presso il California Pacific Medical Center Research Institute, afferma che questa ricerca ha anche implicazioni per coloro che studiano il glioblastoma, una forma particolarmente aggressiva di cancro al cervello che coinvolge gli astrociti. “La senescenza cellulare è un’arma a doppio taglio e l’attuale stato della ricerca associata alla senescenza è molto disordinato. Mentre la senescenza porta a un’infiammazione cronica che promuove il cancro e la neurodegenerazione, agisce anche come soppressore del tumore. Ci sono molti fattori secreti dagli astrociti senescenti, pensiamo che alcuni di essi potrebbero essere sfruttati come un modo per curare il glioblastoma “.
La ricerca, che ha coinvolto il sequenziamento dell’RNA delle trascrizioni espresse da astrociti senescenti e non senescenti, ha trovato cambiamenti nell’espressione di oltre 5.000 geni le cui funzioni sono importanti nel cancro, nelle malattie infettive e nelle malattie neurologiche.
I risultati di questo studio sono disponibili per la comunità di ricerca.
Fonte, Buck Institute