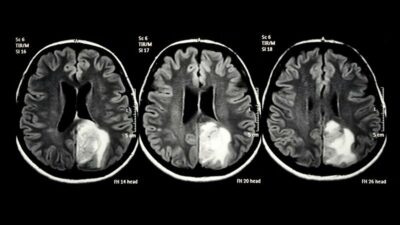
Glioblastoma-Immagine Credit Public Domain-
La riattivazione di un retrovirus dormiente, HML-2, può contribuire all’aggressività del glioblastoma, un tipo di tumore al cervello.
I ricercatori hanno scoperto che il virus influenza lo stato delle cellule staminali dei tumori, promuovendo così una forma più resistente di cancro. È stato scoperto che HML-2 influenza la programmazione delle cellule staminali tramite una proteina di regolazione genica chiamata OCT4.
Questi risultati presentano potenziali obiettivi per lo sviluppo di trattamenti più efficaci per il glioblastoma.
Fatti chiave dello studio :
- HML-2 è un antico retrovirus dormiente da 6 milioni di anni. Può contribuire alla formazione del tumore al cervello quando riattivato.
- Il virus HML-2 riattivato altera la programmazione delle cellule staminali tramite una proteina di regolazione genica chiamata OCT4. Questa attività rende il glioblastoma più aggressivo e resistente al trattamento.
- I risultati del team suggeriscono potenziali bersagli per nuove terapie. Nei loro esperimenti, un farmaco antiretrovirale ha ridotto notevolmente l’attività HML-2 e i marcatori delle cellule staminali tumorali.
La durata media della sopravvivenza dopo la diagnosi di glioblastoma è di 14 mesi, ma alcuni di questi tumori cerebrali sono più aggressivi e resistenti al trattamento rispetto ad altri, e un nuovo studio del Sylvester Comprehensive Cancer Center presso la Miller School of Medicine dell’Università di Miami suggerisce la riattivazione di un antico retrovirus potrebbe essere almeno in parte responsabile.
“Il nostro laboratorio ha scoperto che un retrovirus dormiente evolutivo di 6 milioni di anni fa – HML-2, un sottotipo di HERV-K – contribuisce alla formazione del tumore al cervello. Abbiamo dimostrato per la prima volta che questo virus, una volta riattivato, svolge un ruolo nella definizione dello stato delle cellule staminali dei gliomi di alto grado, promuovendo una forma aggressiva di cancro“, ha affermato il neurochirurgo Dr. Ashish Shah, ricercatore principale presso Sylvester’s Brain Tumor Initiative (ITV) e primo autore di un articolo pubblicato sul Journal of Clinical Investigation.
Le cellule staminali del cancro, una sottopopolazione di cellule nei tumori, guidano l’inizio e lo sviluppo del tumore e influenzano l’aggressività e la resistenza al trattamento di un cancro.
Questo studio, condotto da ricercatori della Sylvester, della Georgetown University e del National Institutes of Health, ha scoperto che l’HML-2 ha alterato la programmazione delle cellule staminali attivando una proteina di regolazione genica chiamata OCT4.
L’HML-2 era precedentemente implicato nella genesi e nello sviluppo di altri tumori, ma si ritiene che questo sia il primo studio che mostra gli effetti del virus nei gliomi e descrive i meccanismi molecolari e cellulari coinvolti.
“I nostri risultati suggeriscono che l’HML-2 contribuisce fondamentalmente alla nicchia delle cellule staminali del glioblastoma, il microambiente che supporta le cellule staminali e ne determina il destino“, ha affermato il Dott. Avindra Nath, Direttore clinico della Divisione di ricerca intramurale presso il National Institute of Neurological Disturbi e ictus presso il National Institutes of Health.
“Abbiamo condotto un’indagine traslazionale completa sull’espressione di HML-2 nel glioblastoma e sul suo ruolo nel mantenimento del fenotipo delle cellule staminali del cancro”, ha affermato Nath, autore senior dell’articolo. I risultati si basavano su analisi di cellule di glioblastoma derivate da pazienti e studi su modelli murini.
“I risultati del team forniscono ai ricercatori obiettivi per lo sviluppo di nuove terapie e nel loro lavoro, un farmaco antiretrovirale ha ridotto significativamente l’attività HML-2 e ha ridotto i marcatori delle cellule staminali tumorali”, ha affermato Shah, Direttore degli studi clinici e della ricerca traslazionale e ricercatore principale nella sezione di virologia e immunoterapia presso il Sylvester Comprehensive Cancer Center’s Brain Tumor Initiative (BTI).
“Prendere di mira la nicchia delle cellule staminali del glioblastoma è un’opzione interessante per prevenire alterazioni nelle cellule staminali e ridurre la recidiva del tumore e la resistenza al trattamento”, ha affermato il ricercatore.
Leggi anche:Glioblastoma: importanti progressi nella cura
HML-2, un sottotipo di HERV-K, è uno dei tanti retrovirus endogeni umani (HERV), reliquie ancestrali di infezioni retrovirali che si sono verificate nel corso della storia e hanno portato all’integrazione di sequenze virali nel genoma umano. Gli HERV, che costituiscono circa l’8% del genoma umano, di solito sono silenti, cioè incapaci di causare infezioni, ma gli scienziati hanno recentemente scoperto che alcuni possono essere riattivati in alcuni tipi di cancro.
Gli autori dell’Università di Miami includono il primo autore Shah, Vaidya Govindarajan, il Dottor Jay Chandar, Deepa Seetharam, PhD, Jelisah Desgraves, il Dottor Michael Ivan e il Dottor Ricardo Komotar.
Fonte:Neurosciencenews