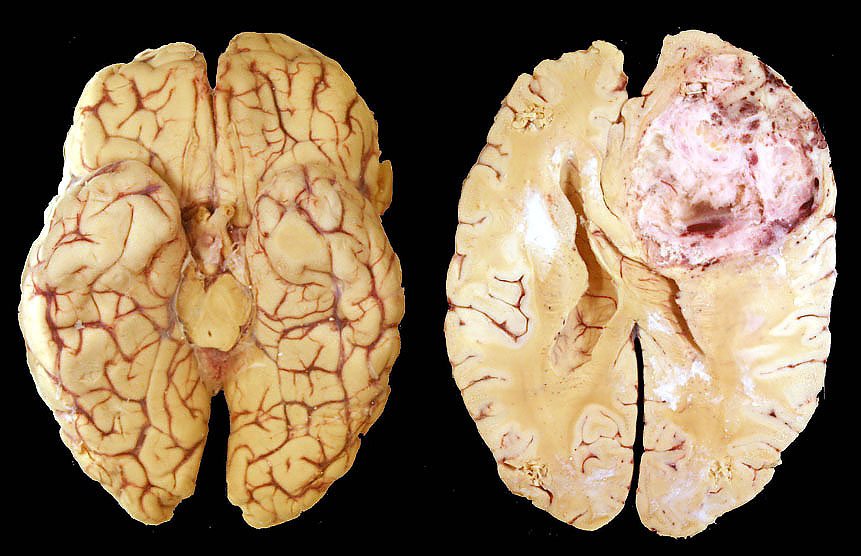
(Glioblastoma-Immagine Credit Public Domain).
Gli scienziati di Toronto hanno scoperto che il processo di guarigione che segue una lesione cerebrale potrebbe stimolare la crescita del glioblastoma quando le nuove cellule generate per sostituire quelle perse a causa della lesione vengono deragliate dalle mutazioni. Una lesione cerebrale può essere qualsiasi cosa, da un trauma a un’infezione o un ictus.
Lo studio è stato realizzato da un team interdisciplinare di ricercatori dell’Università di Toronto, del The Hospital for Sick Children (SickKids) e del Princess Margaret Cancer Center che fanno parte anche della Stand Up To Cancer Canada Dream Team che si concentra su un comune cancro al cervello noto come glioblastoma.
“I nostri dati suggeriscono che il giusto cambiamento mutazionale in particolari cellule del cervello potrebbe essere modificato da una lesione per dare origine a un tumore“, afferma il Dottor Peter Dirks, leader del Dream Team, capo della divisione di neurochirurgia e scienziato senior nel programma Developmental and Stem Cell Biology presso SickKids.
Gary Bader, Professore di genetica molecolare presso il Donnelly Center for Cellular and Biomolecular Research presso la facoltà di medicina della U of T Temerty e il Dottor Trevor Pugh, scienziato senior, hanno guidato la ricerca che è stata pubblicata sulla rivista Nature.
I risultati potrebbero portare a una nuova terapia per i pazienti con glioblastoma che attualmente hanno opzioni di trattamento limitate con una durata media della vita di 15 mesi dopo la diagnosi.
“Il glioblastoma può essere pensato come una ferita che non smette mai di guarire”, afferma Dirks. “Siamo entusiasti di ciò che questo studio ci dice su come il glioblastoma nasce e cresce e offre idee completamente nuove sul trattamento concentrandosi sulla risposta alla lesione e all’infiammazione”.
Vedi anche:Glioblastoma: la necrosi favorisce la progressione
I ricercatori hanno applicato le più recenti tecnologie di sequenziamento dell’RNA a cellula singola e apprendimento automatico per mappare la composizione molecolare delle cellule staminali del glioblastoma (GSC), che il team di Dirks aveva precedentemente dimostrato essere responsabili dell’insorgenza e della recidiva del glioblastoma dopo il trattamento.
Hanno trovato nuove sottopopolazioni di GSC che portano i segni molecolari dell’infiammazione e che si mescolano con altre cellule staminali tumorali all’interno dei tumori dei pazienti. Questo suggerisce che alcuni glioblastomi iniziano a formarsi quando inizia il normale processo di guarigione dei tessuti che genera nuove cellule per sostituire quelle perse a causa di lesioni, forse anche molti anni prima che i pazienti diventino sintomatici”, ha detto Dirks.
Una volta che una cellula mutante si impegna nella guarigione della ferita, non può smettere di moltiplicarsi perché i normali controlli sono interrotti e questo stimola la crescita del tumore, secondo lo studio.
“L’obiettivo è identificare un farmaco che ucciderà le cellule staminali del glioblastoma”, afferma Bader, il cui studente laureato Owen Whitley ha contribuito all’analisi computazionale dei dati.”Ma prima dovevamo capire la natura molecolare di queste cellule e indirizzarle in modo più efficace”.
Il team ha raccolto GSC da 26 glioblastomi di pazienti e le ha ampliate in laboratorio per ottenere un numero sufficiente di queste cellule rare per l’analisi. Quasi 70.000 cellule sono state analizzate mediante sequenziamento dell’RNA a cellula singola che rileva quali geni sono attivati nelle singole cellule, uno sforzo guidato da Laura Richards, una ricercatrice del laboratorio di Pugh.
I dati hanno confermato un’ampia eterogeneità della malattia, il che significa che ogni tumore contiene più sottopopolazioni di cellule staminali tumorali molecolarmente distinte, rendendo probabile la recidiva poiché la terapia esistente non può spazzare via tutti i diversi subcloni.
Uno sguardo più attento ha rivelato che ogni tumore ha uno dei due stati molecolari distinti, chiamati “sviluppo” e “risposta al trauma”, o qualche parte su un gradiente tra i due.
Lo stato di sviluppo è un segno distintivo delle cellule staminali del glioblastoma e assomiglia a quello delle cellule staminali in rapida divisione nel cervello in crescita prima della nascita.
Ma il secondo stato è stato una sorpresa. I ricercatori l’hanno definito “risposta alle lesioni” perché mostrava una sovraregolazione delle vie immunitarie e dei marker di infiammazione, come l’interferone e il TNFalfa, che sono indicativi dei processi di guarigione delle ferite.
Queste firme immunitarie sono state raccolte solo grazie alla nuova tecnologia a cellula singola dopo essere state ignorate dai metodi precedenti per le misurazioni delle cellule sfuse.
Nel frattempo, gli esperimenti condotti dal laboratorio di Stephane Angers presso la Facoltà di Farmacia di Leslie Dan hanno stabilito che i due stati sono vulnerabili a diversi tipi di knock out genici, rivelando una serie di bersagli terapeutici legati all’infiammazione che non erano stati precedentemente considerati per il glioblastoma.
Infine, si è scoperto che il relativo incrocio dei due stati era specifico del paziente, il che significa che ogni tumore era influenzato o verso l’estremità del gradiente dello sviluppo o della risposta alla lesione. I ricercatori stanno ora cercando di indirizzare questi pregiudizi per terapie su misura.
“Ora stiamo cercando farmaci che siano efficaci su diversi punti di questo gradiente”, afferma Pugh, che è anche il Direttore dell’Ontario Institute for Cancer Research. “C’è una reale opportunità per la medicina di precisione: sezionare i tumori dei pazienti a livello di singola cellula e progettare un cocktail di farmaci in grado di eliminare più di un subclone di cellule staminali tumorali allo stesso tempo”.
Fonte: Nature Cancer