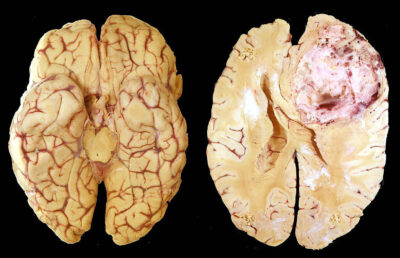
(Glioblastoma multiforme-Immagine Credit Public Domain).
La ricerca condotta da medici e scienziati dell’UCLA Jonsson Comprehensive Cancer Center e dell’UCLA Jane & Terry Semel Institute for Neuroscience & Human Behavior ha identificato un gene che potrebbe fornire un bersaglio terapeutico per il glioblastoma multiforme (GBM), un cancro al cervello resistente al trattamento e letale.
Il gene, P300, consente alle cellule del GBM che sono state danneggiate dalla radioterapia di riprendersi riorganizzando il DNA e avviando un meccanismo molecolare che fortifica le cellule tumorali per la crescita e la sopravvivenza. Il blocco di P300 ha interrotto la sua capacità di mettere in moto questo processo, secondo i ricercatori, che hanno condotto i loro studi su modelli murini e su cellule GBM umane.
I risultati dello studio appaiono online su Nature Communications.
Sebbene il glioblastoma sia considerato raro (secondo la National Brain Tumor Society), negli Stati Uniti quest’anno dovrebbero essere diagnosticati circa 13.000 nuovi casi. E’ il tumore cerebrale primario più comune negli adulti. Non esiste una cura nota e la durata media della sopravvivenza è misurata in mesi. Le cellule GBM e i loro precursori, le cellule staminali del glioma (GSC), si adattano rapidamente e si riprendono dalla lesione, quindi la chemioterapia e la radioterapia, che inizialmente possono rallentare la progressione di un tumore, possono infine contribuire alla crescita e alla recidiva.
Vedi anche:Glioblastoma multiforme:combinazione inibisce la crescita
Eseguendo il sequenziamento trascrittomico unicellulare, in grado di identificare i cambiamenti molecolari nelle cellule cancerose, il team di ricerca guidato dalla UCLA ha dimostrato che lo stress indotto dalla radioterapia promuove la conversione fenotipica delle cellule staminali del glioma per assomigliare a due tipi di cellule che si trovano normalmente nei vasi sanguigni (cellule simil-endoteliali vascolari e cellule simil-pericita). I ricercatori hanno scoperto che queste cellule convertite promuovevano la crescita del tumore e la recidiva post-trattamento. La conversione è stata determinata da cambiamenti all’interno di specifiche regioni del gene vascolare in un processo mediato dal gene P300 o P300 HAT (istone acetiltransferasi).
“I nostri risultati mostrano a livello unicellulare che lo ‘stress da radiazioni’ altera gli stati funzionali delle cellule di glioma, ma invece di ricostituire il sistema vascolare per trasportare l’afflusso di sangue, come è stato talvolta teorizzato, queste cellule convertite forniscono un supporto trofico che consente le cellule tumorali di sopravvivere e crescere nelle condizioni ostili create dalle radiazioni”, ha affermato l’autore senior Harley Kornblum, MD, Ph.D., ricercatore presso l’UCLA Jonsson Comprehensive Cancer Center e l’UCLA Brain Research Institute.
“Proprio come il P300 svolge un ruolo chiave nel cambiare il panorama molecolare delle cellule staminali del glioma, l’inibizione della funzione del gene sembra bloccare la conversione fenotipica. Ciò suggerisce che piccole molecole che inibiscono l’attività HAT del P300 possono essere utili nel prevenire la crescita del tumore e la resistenza adattativa di GBM“, ha affermato il Dottor Sree Deepthi Muthukrishnan, Assistant Project Scientist e primo autore dello studio.
Mentre gli autori sono stati in grado di identificare alcuni fattori candidati espressi dalle cellule simil-vascolari e i loro esperimenti mostrano il potenziale ruolo di questi fattori nel promuovere la proliferazione delle cellule tumorali irradiate, saranno necessari ulteriori studi per scoprire completamente i meccanismi sottostanti coinvolti. Tuttavia, è importante sottolineare che i fattori che mediano le azioni trofiche delle cellule simil-vascolari indotte dalle radiazioni nel glioblastoma multiforme sarebbero probabilmente bersagli per un potenziale intervento terapeutico per prevenire la ricaduta del GBM.
Fonte:Nature