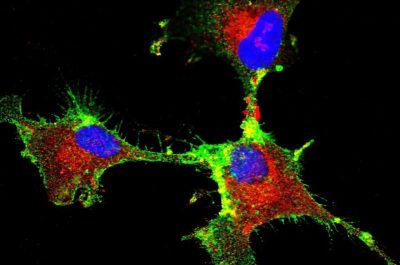
Glioblastoma/studio art. di Fernanda Bassette, FAPESP. Immagine: cellule staminali di glioblastoma con marcatura fluorescente per la proteina prionica (rosso), la proteina CD44 (verde) e il nucleo cellulare (blu). Credito: Marilene Hohmuth Lopes e Mariana Prado/ICB-USP.
Il glioblastoma (GBM), uno dei tipi più aggressivi di cancro al cervello, è una delle sfide più grandi per la medicina, sia perché è difficile da curare sia per il suo alto tasso di mortalità. In Brasile, sebbene non siano disponibili cifre esatte, si stima che ogni anno vengano diagnosticati tra 10.000 e 12.000 nuovi casi.
La malattia, che rappresenta quasi la metà (49%) di tutti i tumori cerebrali , ha un tasso di sopravvivenza estremamente basso, con la maggior parte dei pazienti che vivono solo circa 12 mesi dopo la diagnosi. Per questo motivo, gli scienziati sono alla ricerca di nuovi obiettivi terapeutici da anni per sviluppare trattamenti più efficaci che possano migliorare la sopravvivenza e la qualità della vita di questi pazienti.
Il trattamento tradizionale include un intervento chirurgico per rimuovere il tumore, chemioterapia e radioterapia. Il farmaco principale utilizzato è il Temozolomide (TMZ), un chemioterapia approvato alla fine degli anni ’90 e ancora utilizzato per controllare la malattia. Il problema è che, sebbene il paziente possa essere libero dal tumore per alcuni mesi, il glioblastoma raramente risponde completamente al trattamento e si ripresenta mesi dopo, spesso in una forma più aggressiva e invasiva.
Con questo in mente, il gruppo guidato dalla prof.ssa Marilene Hohmuth Lopes, del Laboratorio di neurobiologia e cellule staminali del Dipartimento di biologia cellulare e dello sviluppo dell’Istituto di scienze biomediche dell’Università di San Paolo (ICB-USP) in Brasile, ha deciso di esaminare più da vicino il meccanismo d’azione delle cellule tumorali che rimangono nel tessuto cerebrale anche dopo il trattamento completo.
I risultati sono stati pubblicati sulla rivista BMC Cancer.
Nello studio, il team ha scoperto che la proteina prionica svolge un ruolo chiave nella biologia del glioblastoma.
“Il trattamento del glioblastoma è stagnante da oltre 20 anni. È essenziale scoprire nuove strategie per migliorare le possibilità di recupero e sopravvivenza dei pazienti”, ha detto Lopes ad Agência FAPESP.
Cellule staminali tumorali
Per comprendere l’importanza della proteina prionica nella biologia del cancro, è innanzitutto necessario comprendere il meccanismo d’azione del glioblastoma. Come spiega Lopes, l’intervento chirurgico e il trattamento con Temozolomide uccidono le cellule che proliferano rapidamente e formano la “massa” del tumore. Tuttavia, le cosiddette cellule staminali tumorali (o cellule staminali del glioblastoma) rimangono dormienti nel tessuto cerebrale. Quando tornano attive, sono in grado di orchestrare nuovamente la crescita del tumore.
“È importante ricordare che le cellule staminali sono molto potenti e hanno la capacità di auto-rinnovarsi. Rimangono inattive per un po’, ma quando si ‘risvegliano’ generano nuove cellule che si moltiplicano rapidamente e ricostruiscono l’intera gerarchia cellulare del tumore. “Questo è ciò che ha attirato la nostra attenzione”, afferma il professore.
Proteina prionica
Tutti gli esseri umani producono una proteina chiamata prione, che ha funzioni biologiche rilevanti ed estremamente importanti per il mantenimento del sistema nervoso centrale: influenza la funzionalità e la plasticità del cervello, è coinvolta nei processi cognitivi (ad esempio la formazione e il consolidamento della memoria) e contribuisce alla comunicazione tra i neuroni.
“Stavo già studiando questa proteina prima di iniziare a esaminare il suo ruolo nello sviluppo del cancro. Quando abbiamo osservato nei campioni dei pazienti che era elevata nei tumori molto aggressivi, abbiamo deciso di comprendere meglio la sua relazione con il glioblastoma e la sua influenza sulle cellule staminali tumorali responsabili della recidiva del cancro“, afferma.
Ciò è importante perché la proteina prionica è presente sulla superficie delle cellule, il che la rende “farmaceutica” (un bersaglio che può essere modulato dai farmaci).
“Ciò significa che quando si pensa a una possibile terapia, è molto più facile attraversare la barriera ematoencefalica e colpire una proteina che si trova sulla superficie della cellula piuttosto che una che si trova al suo interno, ad esempio”, spiega il professore.
Negli esperimenti in vitro, il gruppo ha osservato che quando venivano coltivate le cellule staminali del glioblastoma, si verificava un aumento significativo nei livelli della proteina prionica, suggerendo che essa svolge un ruolo fondamentale nella regolazione di queste cellule.
Modifica genetica
Sulla base di questa scoperta, il gruppo ha utilizzato la tecnologia CRISPR-Cas9 per modificare il genoma delle cellule staminali del glioblastoma e bloccare la produzione della proteina prionica in queste cellule. Ciò ha permesso ai ricercatori di alterare il funzionamento di queste cellule staminali tumorali, riducendo la loro capacità di invadere e proliferare.
“Questo ci ha mostrato che il prione è un potenziale bersaglio terapeutico. Ma è improbabile che una singola proteina da sola sia responsabile dello sviluppo della malattia. Crediamo che agisca in diversi percorsi di segnalazione, motivo per cui continuiamo a studiare altri meccanismi e possibili partner per la proteina“, spiega Lopes.
Il gruppo ha poi studiato l’interazione del prione con la proteina CD44, un noto marcatore delle cellule staminali tumorali coinvolto nell’invasione collettiva dei tumori al seno e al colon.
“Abbiamo scoperto di recente che una molecola modula l’altra e ora stiamo cercando di comprendere meglio questa interazione. Finora, sappiamo che la proteina prionica può agire come un’impalcatura, creando piattaforme di segnalazione multiproteica nella membrana delle cellule in modo che possano sopravvivere e proliferare. Quando abbiamo alterato la produzione di questa proteina [utilizzando CRISPR-Cas9], abbiamo scoperto che la sua assenza compromette l’auto-rinnovamento, la migrazione e l’invasione delle cellule tumorali“, sottolinea.
Oggi anche:Il glioblastoma riprogramma i neutrofili infiltranti il tumore
Nonostante i risultati promettenti, non è ancora possibile prevedere quando queste nuove scoperte troveranno applicazione nella pratica clinica.
“Lavoriamo con la ricerca di base. Ci vogliono molti anni per tradurre queste scoperte in trattamenti. Ma siamo nel processo di comprensione dei meccanismi, di comprensione di come questa proteina regola altri geni importanti nella biologia cellulare e tumorale e di come potrebbe diventare un potenziale bersaglio terapeutico in futuro. Lo studio continua“, conclude il ricercatore.
Fonte: BMC Cancer