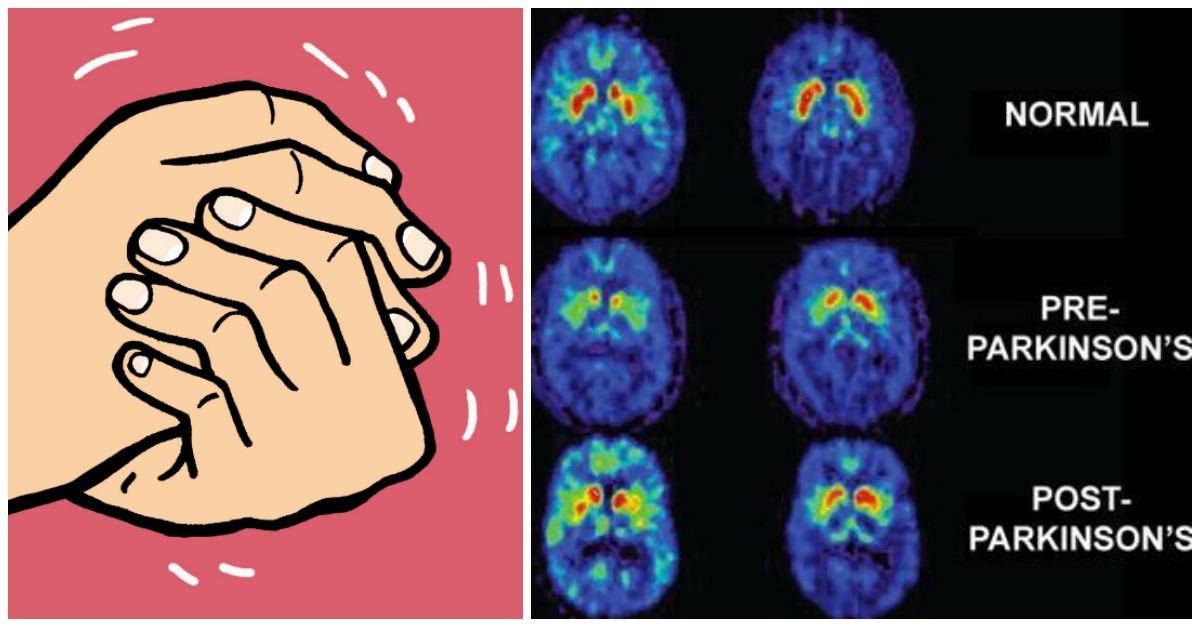
La mutazione genica più comune associata al Parkinson altera le cellule circolanti all’esterno del cervello, non all’interno, offrendo una nuova comprensione di ciò che causa la malattia.
Fino a poco tempo fa, il Parkinson era stato pensato come una malattia che inizia nel cervello, distruggendo i centri di movimento e causando tremori e perdita di movimento. Una nuova ricerca pubblicata questa settimana sulla rivista Brain, mostra che la mutazione genetica più comune del Parkinson può cambiare il modo in cui le cellule immunitarie reagiscono a infezioni generiche come il raffreddore, che a loro volta innescano la reazione infiammatoria nel cervello che causa il Parkinson. La ricerca offre una nuova comprensione della malattia di Parkinson.
“Sappiamo che le cellule del cervello chiamate microglia causano l’infiammazione che alla fine distrugge l’area del cervello responsabile del movimento nel Parkinson”, ha detto Richard Smeyne,Direttore del Jefferson Comprehensive Parkinson’s Disease and Movement Disorder Center presso l’ Istituto Vickie e Jack Farber per Neuroscienze . “Ma non era chiaro come una mutazione ereditaria comune fosse coinvolta in quel processo e se la mutazione alterasse la microglia”.
Insieme al Dr. Smeyne e alla prima autrice dell’articolo Elena Kozina, il ricercatore ha esaminato la versione mutante del gene LRRK2 (pronunciato “lark”). Le mutazioni nel gene LRRK2 sono la causa più comune di morbo di Parkinson ereditario. Tuttavia c’è stata una controversia sull’esatta funzione del gene LRRK2 nel cervello.
( Vedi anche: Parkinson: determinata la struttura della proteina associata all’ infiammazione).
“Sappiamo che la mutazione genetica non è sufficiente per causare la malattia”, ha detto il Dr. Kozina, studente post-dottorato presso la Jefferson University . “Sappiamo che i gemelli che portano entrambi la mutazione non svilupperanno necessariamente il morbo di Parkinson, ma occorrerà un secondo” colpo “o un evento iniziale“.
Sulla base del suo precedente lavoro, che dimostra che l’ influenza potrebbe aumentare il rischio di malattia di Parkinson, il Dr. Smeyne ha deciso di indagare se quel secondo colpo provenisse da un’infezione. Sospettando che le mutazioni di LRRK2 possano agire al di fuori del cervello, i ricercatori hanno usato un agente – il guscio esterno dei batteri, chiamato lippopolisaccaride (LPS) – che causa una reazione immunitaria. LPS stesso non passa nel cervello, né attiva le cellule immunitarie, il che lo rende ideale per testare se questo secondo colpo agisca direttamente nel cervello.
Quando i ricercatori hanno somministrato i frammenti batterici ai topi portatori delle due più comuni mutazioni del gene LRRK2, la reazione immunitaria è diventata una “tempesta di citochine”, con mediatori infiammatori che salivano a livelli che erano 3-5 volte superiori a una normale reazione a LPS. Questi mediatori dell’infiammazione sono stati prodotti dalle cellule immunitarie T e B che esprimono la mutazione LRRK2.
Nonostante il fatto che LPS non ha attraversato la barriera emato-encefalica, i ricercatori hanno dimostrato che le citochine elevate erano in grado di entrare nel cervello, creando un ambiente che causava l’attivazione patologica della microglia e distruggeva la regione del cervello coinvolta nel movimento.
“Questi risultati ci offrono un nuovo modo di pensare a come queste mutazioni possano causare il morbo di Parkinson”, ha detto il dott. Smeyne. “Sebbene non possiamo trattare le persone con immunosoppressori per tutta la vita per prevenire la malattia, se questo meccanismo sarà confermato, è possibile che altri interventi possano essere efficaci nel ridurre la possibilità di sviluppare la malattia”.
Fonte: Brain