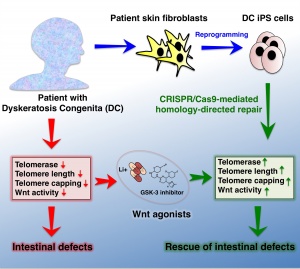
Immagine: il collegamento tra telomeri e la via di segnale Wnt può portare a una opzione di trattamento per la discheratosi congenita.
La Discheratosi congenita o sindrome di Zinsser-Cole-Engman è una forma particolare di anemia congenita, una malattia ereditaria, che si manifesta in età infantile. ” E’ caratterizzata da una triade di sintomi muco-cutanei, che comprende anomalie della pigmentazione cutanea, distrofia ungueale e leucoplachia delle mucose. Possono essere presenti anche altre anomalie. L’insufficienza del midollo osseo è la causa principale di morte precoce, unitamente alla predisposizione alle lesioni tumorali e alle complicazioni polmonari ad esito fatale. La DC presenta una notevole eterogeneità clinica e genetica. Sono note forme recessive, legate all’X, forme autosomiche dominanti e forme autosomiche recessive. I geni DKC1 e TERC, che sono mutati in due sottotipi di DC, codificano per componenti del complesso delle telomerasi; per questo, si ritiene che la DC sia soprattutto causata da un difetto delle telomerasi “. Altre anomalie associate alla discheratosi sono: stenosi esofagea, fibrosi polmonare, cirrosi epatica, anomalie ossee e anomalie immunitarie.
Una caratteristica di fondo comune della malattia è la presenza di telomeri corti. I telomeri sono le strutture che proteggono le estremità dei cromosomi, ma tendono ad accorciarsi con la divisione cellulare e l’età e possono quindi perdere le loro funzioni di protezione. Molti pazienti DC hanno una mutazione nel gene DKC1, che codifica per un componente dell’ enzima chiamato telomerasi che aiuta a mantenere la lunghezza dei telomeri. La maggior parte delle anomalie nei pazienti affetti da discheratosi si verificano nei tessuti che si dividono più spesso e nei quali la telomerasi è essenziale come i tessuti epiteliali, la pelle, intestino e polmoni.
In un nuovo studio pubblicato su Cell Stem Cell, i ricercatori della University of Pennsylvania, guidati da Christopher J. Lengner della School of Veterinary Medicine e Brad Johnson della Perelman School of Medicine, hanno trovato un legame tra i telomeri e una cascata di segnali molecolari chiamati pathway Wnt che possono essere utilizzati per una nuova opzione di trattamento.
Il collegamento è stato identificato inizialmente utilizzando topi nel laboratorio di Johnson. In seguito Lengner e Johnson hanno esteso questi risultati ai tessuti umani in coltura per dimostrare che stimolare la via segnale Wnt ha invertito i segni di disfunzione DC-correlati.
Lo studio sottolinea la presenza di un feedback positivo tra la via di segnale Wnt e la funzione dei telomeri, per cui la stimolazione della via di segnale Wnt attiva l’espressione di proteine che aumentano la dimensione dei telomeri e porta a cellule staminali più funzionali, che a loro volta stimolano ulteriormente la via di segnale Wnt.
La ricerca fornisce anche nuove intuizioni per combattere la disfunzione dei telomeri, un processo che è stato implicato anche in alcuni tipi di cancro e nell’invecchiamento naturale.
“Quello che si verifica nei topi mutanti e nei pazienti con discheratosi congenita è la conseguenza di una insufficiente attività della telomerasi nei tessuti in rapida divisione”, ha spiegato Johnson, co-autore senior dello studio e Professore associato di patologia e medicina di laboratorio della Penn Medicine.
Lengner, Professore assistente presso il Dipartimento di Scienze Biomediche alla Penn Vet, è co-autore senior dello studio.
“In questo momento la terapia principale per questi pazienti è un trapianto di midollo osseo”, ha detto Lengner. “Che può affrontare l’ insufficienza del midollo osseo, ma non risolve altri problemi associati con la malattia e soprattutto, non riduce il rischio di cancro. Questo lavoro suggerisce un modo per affrontare la causa della malattia”.
All’inizio, la ricerca condotta sui modelli murini di DC aveva suggerito che ci poteva essere un collegamento tra la via di segnale Wnt e la telomerasi. In seguito, uno studio condotto sulle cellule di pazienti affetti da discheratosi congenita aveva ‘trovato una diminuzione dell’attività nella via di segnale Wnt”. Così i ricercatori Penn hanno voluto verificare se l’attivazione di Wnt poteva invertire gli effetti della malattia.
Il team ha utilizzato tre tecniche innovative. In primo luogo, ha impiegato cellule staminali pluripotenti o iPSCs, che sono cellule adulte che sono “riprogrammate” per diventare cellule staminali embrionali che possono dar luogo a diversi tipi di cellule.
In secondo luogo, i ricercatori hanno usato il sistema Cas9 /CRISPR, un metodo semplice: portando la proteina Cas9 e gli appropriati RNA guida (gRNA) nelle cellule, il genoma dell’organismo può essere tagliato in qualsiasi punto in maniera estremamente precisa e con una tecnica semplice che richiede attrezzature relativamente economiche. Inoltre, CRISPR è stato modificato per creare fattori di trascrizione programmabili che permettono di attivare o silenziare specifici geni.
I ricercatori hanno utilizzato questo sistema gene-editing per introdurre una mutazione DKC1 nelle iPSCs umane sane e anche per correggere la mutazione che causa la malattia nelle iPSCs da campioni dei pazienti con discheratosi congenita.
Infine, i ricercatori hanno cresciuto in vitro i cosiddetti “organoidi” intestinali, simili all’intestino, attraverso un processo chiamato differenziazione diretta.
Quando la squadra di Penn ha osservato lo sviluppo dell’ organoide intestinale, ha trovato che, inizialmente, “le cellule dei pazienti DC sembravano formarsi normalmente, ma al punto in cui si suppone la formazione dell’organoide intestinale, le cose sono crollate”, ha detto Lengner.
Mentre “da campioni prelevati da pazienti sani e da pazienti DC le cui mutazioni erano state corrette attraverso CRISPR, l’organoide intestinale si è formato, da campioni di pazienti DC con la mutazione causata dalla malattia, lo sviluppo dell’organoide intestinale non è andato a buon fine e le cellule presentavano telomeri più corti”.
“Abbiamo potuto vedere a livello molecolare, che il mancato sviluppo dell’organoide intestinale è stato accompagnato da una mancata attivazione di programmi genetici delle cellule staminali intestinali specifiche”, ha spiegato Lengner, “in particolare dei geni coinvolti nella via di segnale Wnt”.
Il passo logico successivo per i ricercatori è stato quello di attivare la via di segnale Wnt per vedere se questi difetti genetici potevano essere invertiti. I ricercatori hanno trattato gli organoidi derivati da iPSCs dei paziente DC con un composto chiamato CHIR che stimola la via di segnale Wnt e hanno scoperto che è stata ripristinata la formazione della struttura intestinale-like così come l’espressione genica. Il trattamento ha anche aumentato l’attività della telomerasi e la lunghezza dei telomeri nelle cellule con DKC1 mutante.
Per valutare questo approccio terapeutico in un modello clinicamente più rilevante, i ricercatori hanno trapiantato gli organoidi intestinali umani nei topi. I topi che hanno ricevuto un trapianto contenente la mutazione DKC1 e sono stati trattati con uno stimolatore approvato dalla FDA della via di segnale Wnt, il litio, hanno mantenuto la struttura del tessuto intestinale e avevano un’alta espressione dei geni coinvolti nella via di segnale Wnt. In effetti, essi somigliavano ai topi che avevano ricevuto un trapianto di un organoide derivato da un paziente sano.
Lo studio offre la prova di principio che l’attivazione del pathway Wnt può invertire almeno i fenotipi gastrointestinali associati con la discheratosi congenita. Guardando al futuro, i ricercatori vorrebbero provare a compiere la stessa impresa in altri tipi di tessuti colpiti dalla malattia, come ad esempio i polmoni e persino il sangue.
Fonte: Penn News