Dieta chetogenica-Immagine Astratto Grafico Credito: Cell Reports Medicine (2023). DOI: 10.1016/j.xcrm.2023.101283-
Gli interventi dietetici chetogenici (KDI) sono utili nei modelli animali di malattia renale policistica autosomica dominante (ADPKD). KETO-ADPKD, uno studio esplorativo, randomizzato e controllato, ha lo scopo di fornire la traduzione clinica di questi risultati.
Il nuovo studio indaga gli interventi dietetici chetogenici nella malattia del rene policistico. Lo studio clinico sulle diete speciali presso l’Università di Colonia mostra risultati promettenti “sull’uso di una dieta chetogenica come possibile trattamento per la malattia renale policistica ereditaria (ADPKD)”. Questa malattia causa circa il 10% di tutti i casi di insufficienza renale ed è la malattia renale ereditaria più comune a livello mondiale.
Lo studio, chiamato Keto-ADPKD, è stato condotto dal Professor Dr. Roman-Ulrich Müller e dal suo team presso l’Ospedale universitario di Colonia e il Cluster di eccellenza nella ricerca sull’invecchiamento CECAD dell’Università di Colonia. L’unità di nefrologia traslazionale guidata dal Professor Müller al CECAD si concentra sugli interventi dietetici che prolungano la durata della vita e combattono le malattie.
Nello studio KETO-ADPKD, uno di questi regimi dietetici, la dieta chetogenica, è stato studiato come trattamento per la malattia del rene policistico. Lo studio, “Fattibilità e impatto degli interventi dietetici chetogenici nella malattia del rene policistico: KETO-ADPKD, uno studio randomizzato e controllato“, è stato ora pubblicato come articolo di copertina sulla rivista Cell Reports Medicine.
Müller ha presentato i risultati principali dello studio alla Kidney Week dell’American Society of Nephrology nel novembre 2022. I risultati finali dello studio di fase II, che sono ora disponibili, hanno anche mostrato che il passaggio a una dieta chetogenica può avere un effetto positivo effetto positivo sulla funzionalità renale dei pazienti con ADPKD.
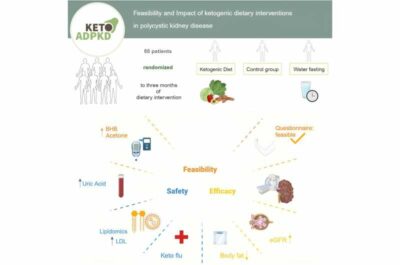
Allo studio hanno partecipato 66 pazienti in totale, divisi in tre gruppi: un gruppo ha seguito una dieta chetogenica per tre mesi, un secondo gruppo ha fatto tre giorni di digiuno idrico una volta al mese, una sorta di dieta zero che consente solo di bere acqua. e un terzo gruppo di controllo ha seguito le raccomandazioni dietetiche standard.
Uno dei risultati più importanti è stato che il 95% dei pazienti del gruppo chetogenico e l’85% del gruppo a digiuno hanno riferito che la dieta era fattibile. Molti critici inizialmente erano piuttosto scettici sulla possibilità della dieta di modificare la vita di tutti i giorni. Tuttavia, i partecipanti avevano diversi punti di vista su questa posssibilità.
Inoltre, i ricercatori sono stati in grado di utilizzare biomarcatori – corpi chetonici – misurati in campioni di sangue che hanno dimostrato che i partecipanti avevano effettivamente aderito alla dieta prescritta. A differenza di molti altri studi sulla dieta, il disegno di questo studio corrisponde a quello di un comune studio sui farmaci (controllo randomizzato) e soddisfa quindi gli standard più elevati.
La dieta chetogenica è una dieta che a prima vista sembra insolita poiché evita i carboidrati come lo zucchero o la farina mentre si consumano più grassi. Questa forma di dieta è stata studiata anche per quanto riguarda il suo effetto generale di prolungamento della vita. Afferma il leader del gruppo di ricerca Müller: “Devi evitare pane e dolci e, ad esempio, usare più olio d’oliva: anche i pesci grassi come il salmone sono un ottimo alimento in questo senso“.
Lo studio è riuscito a dimostrare che dopo soli tre mesi si sono osservati cambiamenti positivi in parametri importanti come la funzionalità renale e non si sono verificati effetti collaterali inattesi. I cambiamenti positivi nella funzione renale sono stati statisticamente significativi e hanno superato le aspettative dei ricercatori.
Spiegano gli autori:
“La malattia del rene policistico autosomico dominante (ADPKD) è la malattia monogenica più comune che porta all’insufficienza renale e mostra una prevalenza genetica di circa 1:1.000. Il decorso della malattia è caratterizzato da cisti renali bilaterali che aumentano di numero e dimensioni con l’età. Circa il 75% dei pazienti con ADPKD necessita di terapia sostitutiva renale entro i 70 anni. L’ADPKD è causata principalmente da mutazioni in due geni, PKD1 e PKD2 e, sulla base della funzione delle proteine codificate, è considerata una ciliopatia, un gruppo di malattie genetiche accomunate dall’alterazione funzionale di una struttura intracellulare chiamata ciglio primario. I cambiamenti nella biologia cellulare associati alla mutazione di questi geni sono alla base non solo del fenotipo renale, ma di un disturbo sistemico, che più frequentemente include la malattia del fegato policistico (PLD) e manifestazioni cardiovascolari. Prima del 2015 non esisteva un trattamento mirato e il cardine della terapia si basava su misure di supporto per proteggere la funzione renale ed evitare complicazioni. Tra le altre, queste misure includono il controllo ottimale della pressione sanguigna, la riduzione dell’assunzione di sale e un apporto sufficiente di acqua. L’approvazione di Tolvaptan, un antagonista del recettore della Vasopressina-2, come prima strategia terapeutica mirata ha rappresentato una pietra miliare per il settore. Tuttavia, gli eventi avversi associati alla terapia, come l’epatotossicità e la poliuria massiva, ne limitano l’uso universale. Inoltre, Tolvaptan rallenta solo la perdita della funzionalità renale e non risolve le manifestazioni extrarenali nell’ADPKD. Di conseguenza, si attendono con urgenza nuove opportunità terapeutiche. A questo proposito, le anomalie metaboliche cellulari osservate nell’ADPKD hanno guadagnato crescente attenzione. Questi cambiamenti includono un pronunciato effetto Warburg, anaplerosi della glutammina, disfunzione mitocondriale e difetti nell’acido tricarbossilico (TCA), nonché nell’ossidazione e nella sintesi degli acidi grassi. Di conseguenza, è stato dimostrato che le cellule epiteliali che rivestono le cisti sono glucosio-dipendenti e metabolicamente inflessibili. È interessante notare che una riduzione dell’assunzione di cibo con conseguente chetosi ha rallentato l’aumento del peso dei reni e la proliferazione delle cellule che rivestono le cisti in due modelli murini di malattia del rene policistico (PKD). Sulla base di questa osservazione, Torres et al. hanno fornito prove in due modelli PKD di roditori e felini che gli interventi metabolici chetogenici sono estremamente utili per ridurre la crescita delle cisti e la perdita della funzionalità renale. Ciò ha suscitato molta attenzione anche tra i pazienti, portando ai primi passi in coorti umane, tra cui una serie di casi retrospettivi tra pazienti con ADPKD, esperienze iniziali di un programma di dieta chetogenica supervisionata (KD) per pazienti con ADPKD e un piccolo studio pilota che espone i pazienti a un breve periodo di interventi dietetici chetogenici. Sebbene questi studi puntassero alla fattibilità generale delle diete e agli esiti positivi riportati dai pazienti (PRO), mancano dati provenienti da studi randomizzati su interventi a lungo termine che estendano le conoscenze sulla fattibilità e forniscano informazioni reali sulla sicurezza e sull’efficacia. Per rispondere a queste domande, KETO-ADPKD è stato concepito come uno studio clinico che esamina due interventi dietetici chetogenici in un contesto randomizzato e controllato“.
Il Professor Müller è convinto che i risultati dello studio costituiscano un passo importante per lo sviluppo di un possibile nuovo trattamento per la malattia del rene policistico. Tuttavia, sottolinea anche che questi dati di uno studio di fase II non erano ancora sufficienti per raccomandare in generale la dieta chetogenica ai pazienti con malattia del rene policistico. Sono necessari ulteriori studi più ampi in più siti per confermare i risultati e per chiarire se è possibile ottenere miglioramenti duraturi della funzionalità renale a lungo termine senza effetti collaterali.
In generale, però, il presente studio è già molto importante perché, grazie alla sua struttura analoga a una sperimentazione farmacologica, dimostra che il cibo può essere efficace quanto un farmaco. Müller è convinto che “questo potrebbe essere il punto di partenza per molte strategie di trattamento dietetico”.
Fonte:Cell Reports Medicine