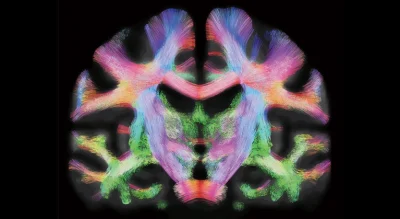
Koji Kamagata dell’Università Juntendo di Tokyo, in Giappone, ritiene che il morbo di Alzheimer possa funzionare un po’ come uno scarico intasato. La malattia è collegata a un accumulo della proteina beta amiloide nel cervello e ritiene che questo potrebbe essere un sintomo di un sistema di eliminazione dei rifiuti lento. Se ciò si rivelasse corretto, potrebbe esserci un modo per rilevare il problema molto prima che si verifichi un danno?
Nel 2022, Kamagata ha pubblicato uno studio che utilizzava i più recenti metodi di risonanza magnetica (MRI) per monitorare il movimento dei fluidi nel cervello, suggerendo un collegamento tra la debole eliminazione dei liquidi di scarto e il morbo di Alzheimer. Da allora ha pubblicato ulteriori studi che collegano i problemi relativi al sistema di eliminazione dei rifiuti del cervello a problemi di sonno, disturbi autoimmuni e altre forme di declino cognitivo.
Imaging dei fluidi cerebrali
Sebbene Kamagata esegua da molto tempo l’imaging del cervello umano vivente, osservare i fluidi non è facile. “Proprio come non è possibile vedere attraverso le pareti e all’interno di un tubo per individuare un problema idraulico, il cervello è nascosto dietro strati di pelle, ossa e liquidi”, spiega.
Un altro livello di protezione proviene dalla barriera emato-encefalica – che impedisce alle tossine di entrare nel cervello – e da altre membrane, come la barriera emato-fluido cerebrospinale e la barriera aracnoidea. Questi bloccano gli agenti di contrasto e altre sostanze utilizzate per rendere possibile l’imaging.
Ma Kamagata è riuscito a trovare riesce una via d’uscita. È uno specialista in “MRI a diffusione” presso il Dipartimento di Radiologia Diagnostica dell’Università di Juntendo. Questa tecnica può esaminare i dettagli microstrutturali del cervello attraverso la modellazione dinamica della diffusione dell’acqua. Kamagata sta anche conducendo un’indagine sul “sistema glinfatico” del cervello, una struttura scoperta nel 2013 che è simile al sistema linfatico del corpo, eliminando proteine solubili e metaboliti dal sistema nervoso centrale.
Questo progetto gli ha già fornito indizi per comprendere meglio la malattia di Alzheimer, così come il cervello in un senso più ampio.
Ad esempio, studi sui roditori avevano suggerito che l’accumulo della proteina beta amiloide nel cervello era correlato a problemi di eliminazione dei liquidi, ma trovare un collegamento simile negli esseri umani è difficile senza un intervento chirurgico invasivo.
Kamagata si rese conto che avrebbe potuto valutare la funzione del sistema glinfatico utilizzando la risonanza magnetica a diffusione.
In primo luogo, le misurazioni del “volume dello spazio perivascolare” potrebbero identificare gli ingrandimenti causati dal ristagno del liquido cerebrospinale nel sistema glinfatico e qualcosa chiamato “analisi lungo l’indice dello spazio perivascolare (ALPS)” potrebbe tracciare la dinamica dei fluidi. Lo fa analizzando il movimento tridimensionale dei fluidi utilizzando la risonanza magnetica a diffusione, un’impresa che richiede l’analisi matematica del tensore (la stessa tecnica con cui Einstein lottò nello sviluppo della sua teoria della relatività generale).
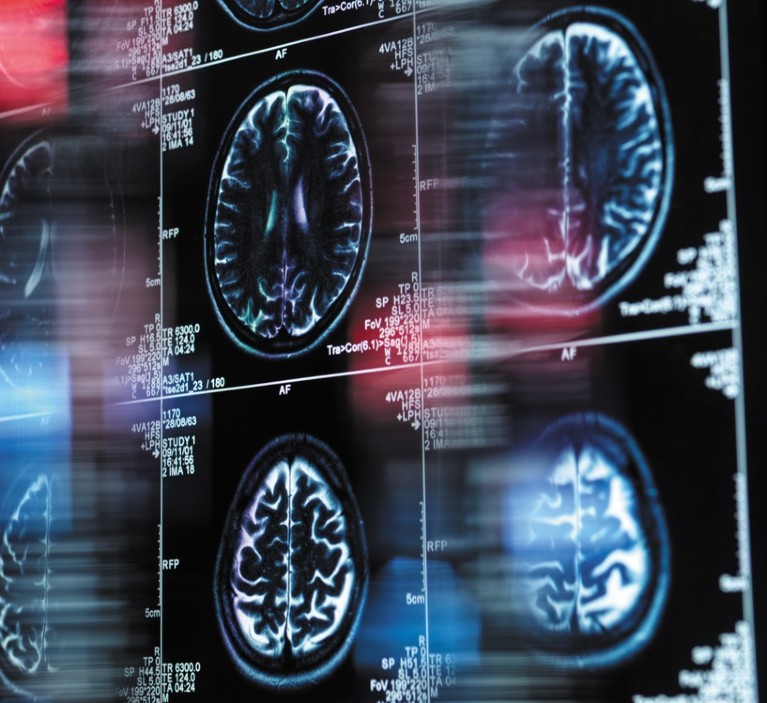
La risonanza magnetica fornisce un buon contrasto se utilizzata su aree di tessuti molli, come il cervello. Credito: IMMAGINE TEK/Libreria fotografica scientifica/Getty
Meglio ancora, Kamagata ha avuto accesso ai dati di 100 pazienti, ai quali ha potuto applicare le tecniche di analisi, dell’Alzheimer’s Disease Neuroimaging Initiative (ADNI), uno studio multicentrico longitudinale fondato negli Stati Uniti per sviluppare la diagnosi precoce e il monitoraggio della malattia di Alzheimer.
Il suo team ha confrontato i processi di eliminazione dei fluidi di soggetti sani con quelli di pazienti affetti da Alzheimer e con quelli con lieve deterioramento cognitivo e ha trovato un possibile collegamento. Meno il fluido sembra muoversi, maggiore è l’accumulo di beta-amiloide e maggiore è il deterioramento della funzione cerebrale.
Prevenzione potenziale
Kamagata spera che ciò possa portare a trattamenti preventivi. “La deposizione di beta-amiloide inizia 10 anni o più prima del deterioramento cognitivo, quindi spero che questo porti a nuovi farmaci che migliorino la disfunzione glinfatica prima dell’inizio della malattia di Alzheimer“.
Ma sviluppare farmaci per il cervello è notoriamente difficile. Per aggirare la barriera emato-encefalica è necessaria la somministrazione tramite una dolorosa iniezione nella colonna vertebrale e misurare gli effetti è complicato senza ricorrere a tecniche chirurgiche invasive.
Un potenziale modo per aggirare questo problema è in fase di sviluppo altrove nell’Università di Juntendo. Nella nuova Facoltà di Scienze dei dati sanitari (vedi riquadro sotto), il ricercatore Zhe Sun ha l’ambizioso obiettivo di creare una “simulazione dell’intero cervello umano”.
Con questo incredibile strumento di simulazione dei dati i ricercatori potrebbero essere in grado di testare i meccanismi dei farmaci prima degli studi clinici, dando loro potenzialmente un potente vantaggio.
La visione è audace: lo strumento dovrebbe simulare gli 86 miliardi di neuroni del cervello umano. Negli ultimi anni, Sun e i suoi colleghi hanno sviluppato simulazioni della corteccia cerebrale, dei gangli della base, del cervelletto e del talamo utilizzando uno dei supercomputer giapponesi. Da allora, l’avvento del nuovo supercomputer giapponese Fugaku – uno dei cinque supercomputer più veloci al mondo – ha fornito un incremento di cento volte alla velocità della simulazione.
Il team di ingegneri di Sun ha inoltre migliorato gli algoritmi al punto che ritiene che saranno in grado di far funzionare un intero cervello entro i prossimi cinque anni.
Leggi anche:Alzheimer: identificato nuovo obiettivo terapeutico
I dati per costruire il cervello provengono da una serie di database MRI sul cervello umano. Diversi tipi di risonanza magnetica forniscono dati sui componenti statici del cervello, mentre i dati della risonanza magnetica a diffusione utilizzano forti gradienti di campo magnetico per mostrare processi dinamici e possono evidenziare le connessioni tra le aree.
“Una volta che i ricercatori aggiungeranno l’apprendimento automatico, per aiutare a ricostruire i punti dati mancanti e mettere a punto i processi dinamici in modo che corrispondano ai dati strutturali misurati, disporranno di uno strumento formidabile“, afferma Sun.
Koji Kamagata ha attinto alle vaste risorse della Facoltà di scienza dei dati sanitari dell’Università di Juntendo per fare importanti scoperte sul legame tra il movimento dei fluidi nel cervello e le malattie.
Lanciata nel 2023, la facoltà è già un importante hub per la risonanza magnetica (MRI) avanzata, una tecnologia che produce immagini anatomiche tridimensionali del corpo.
“Vanta non solo specialisti clinici, ma tecnici, ingegneri, data scientist e ingegneri del software”, afferma Shigeki Aoki, un importante neuroradiologo, che si è trasferito a Juntendo per aiutare a guidare il fiorente team di Data Science della Facoltà. “Non siamo grandi rispetto ad alcuni istituti negli Stati Uniti, ma gli sviluppatori clinici e tecnici sono molto vicini: questo porta a molti progressi, in molte malattie”, afferma.
“La scienza dei dati sanitari”, afferma Aoki, “può avere un impatto enorme. Ad esempio, un ambizioso progetto a Juntendo per simulare tutti i neuroni del cervello, dovrebbe aiutare i ricercatori nella scoperta di farmaci e potrebbe anche aiutare i neurochirurghi a rimuovere i tumori”.
“I neurochirurghi vogliono prelevare quanto più tumore possibile. Ogni piccolo dettaglio che possiamo simulare è utile”, afferma. Nel frattempo, l’accelerazione della scoperta di farmaci potrebbe avere enormi implicazioni per oltre 55 milioni di persone affette da demenza a livello globale.
Attraverso le loro collaborazioni cliniche, le scoperte della facoltà si estendono già alla psichiatria, alla cardiologia e alla scienza dello sport, oltre ai loro contributi alle condizioni neurologiche, come il morbo di Alzheimer e il morbo di Parkinson.
Fonte: Newswise