CRISPR-Immagine Credit Public Domain-
Il sistema CRISPR-Cas è una tecnologia di ingegneria genomica ampiamente utilizzata grazie alla sua semplice programmabilità, scalabilità versatile ed efficienza di target. Sebbene i ricercatori stiano sviluppando rapidamente strumenti CRISPR-Cas9, la sfida più grande resta quella di superare i risultati indesiderati all’interno e all’esterno del target.
Studi precedenti hanno segnalato alterazioni genomiche indesiderate, come l’integrazione di sequenze funzionali derivate da bersagli, ampia delezione nel sito di rottura del doppio filamento (DSB), cromotripsi, perdite cromosomiche segmentali o traslocazioni che spesso si verificano contemporaneamente.
La maggior parte di questi riarrangiamenti genomici rimangono non rilevabili con i metodi di validazione convenzionali, sottolineando la necessità di valutare approfonditamente le cellule o gli organismi modificati con CRISPR-Cas9 mediante strumenti più avanzati.
Un nuovo studio del gruppo di ricerca guidato da Claudia Kutter presso il Dipartimento di microbiologia, tumori e biologia cellulare (MTC) ha identificato potenziali insidie nell’uso della tecnica di editing genetico CRISPR-Cas9, una forbice genetica utilizzata per i trattamenti contro il cancro.
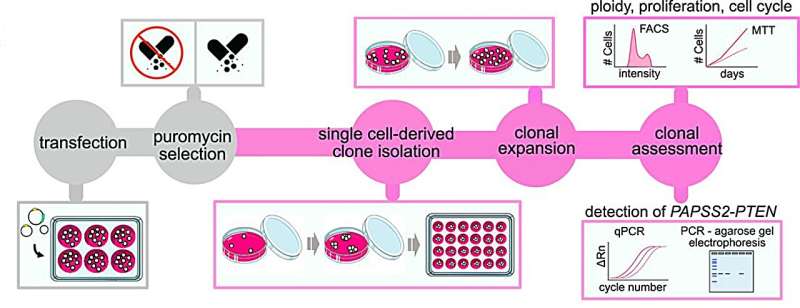
Astratto grafico:l’illustrazione schematica mostra il flusso di lavoro per determinare la frequenza della delezione genomica del locus PAPSS2-PTEN e le conseguenze cellulari associate nei cloni HAP1 derivati da singole cellule. In alcuni esperimenti, le fasi di trasfezione e selezione della puromicina (colorate in grigio) sono state omesse come parte del test. Credito: Life Science Alliance.
“Lo studio ha identificato una linea cellulare tumorale derivata dalla leucemia che rimuove una regione che codifica per un gene che sopprime il tumore e geni che controllano la crescita cellulare”.
I risultati dello studio sono stati pubblicati sulla rivista Life Science Alliance.
“Abbiamo scoperto che questa eliminazione spesso avviene quando le cellule tumorali sono esposte a stress, come quando si utilizza CRISPR, forbici genetiche o altri trattamenti come gli antibiotici. L’eliminazione modifica la regolazione genetica in un modo unico, che a sua volta influenza i processi biologici di base come la replicazione del DNA, regolazione del ciclo cellulare e riparazione del DNA“, afferma Claudia Kutter, leader del gruppo di ricerca presso l’MTC, Karolinska Institutet.
Questa conoscenza è importante affinché ricercatori, medici e biotecnologi possano interpretare e applicare correttamente i risultati dell’editing genetico. Lo studio ha anche rilevanza clinica, poiché le eliminazioni osservate riguardano geni associati al cancro, con implicazioni per la ricerca e il trattamento del cancro.
Spiegano gli autori:
“Il sistema CRISPR-Cas9 è un potente strumento per studiare le funzioni genetiche e ha un potenziale per il trattamento delle malattie. Tuttavia, un editing genomico preciso richiede valutazioni approfondite per ridurre al minimo gli effetti indesiderati sul bersaglio e fuori bersaglio. Qui, riportiamo un’inaspettata delezione di 283 kb sul cromosoma 10 (10q23.31) nelle cellule HAP1 derivate dalla leucemia mieloide cronica, che sono spesso utilizzate negli schermi CRISPR. La regione deleta codifica geni regolatori, inclusi PAPSS2 , ATAD1 , KLLN e PTEN . Abbiamo scoperto che questa eliminazione non era una conseguenza diretta dell’off-targeting di CRISPR-Cas9, ma piuttosto si verificava frequentemente durante la generazione di cellule modificate con CRISPR-Cas9. La delezione è stata associata a cambiamenti globali nell’acetilazione degli istoni e nell’espressione genica, che influenzano processi cellulari fondamentali come il ciclo cellulare e la replicazione del DNA. Abbiamo rilevato questa delezione nei genomi dei pazienti affetti da cancro. Come nelle cellule HAP1, la delezione ha contribuito a modelli di espressione genetica simili tra i pazienti affetti da cancro, nonostante le differenze interindividuali. I nostri risultati suggeriscono che la delezione involontaria di 10q23.31 può confondere gli studi CRISPR-Cas9 e sottolineano l’importanza di valutare i cambiamenti genomici non intenzionali nelle cellule modificate con CRISPR-Cas9, che potrebbero avere un impatto sulla ricerca sul cancro”.
“Sorprendentemente, questa eliminazione è stata involontariamente trascurata da molti ricercatori che modificano i geni nelle cellule tumorali mediante screening CRISPR. L’eliminazione è avvenuta più frequentemente anche nei pazienti che hanno subito cure antitumorali. Le cellule tumorali trattate avevano, grazie all’eliminazione, un vantaggio selettivo, il che è dannoso per la sopravvivenza a lungo termine del paziente poiché queste cellule rimangono dopo il trattamento”, afferma Claudia.
Leggi anche:CRISPR/Cas9: trovata alternativa più sicura per lediting genetico
“Lo studio serve principalmente come segnale di allarme, ma apre anche le porte a ulteriori ricerche volte a sfruttare il potenziale dell’editing genetico riducendo al minimo le conseguenze indesiderate”, conclude Claudia.
Fonte: Life Science Alliance