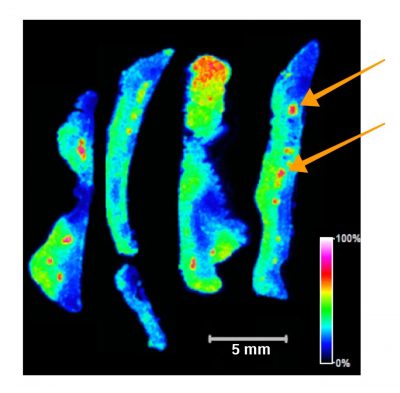
Cancro gastrico-Immagine: l’analisi mediante spettrometria di massa per immagini dei tessuti gastrici di gerbilli mongoli infettati da Helicobacter pylori ha evidenziato la presenza di peptidi triptici di interesse nei follicoli linfoidi (frecce). Crediti: Tim Cover.
Il nostro corpo è pieno di batteri e altri microrganismi che coesistono senza danneggiarci, ma occasionalmente soffriamo di infezioni che possono causare danni. Infezione batterica? Nessun problema: basta (responsabilmente) assumere qualche pillola di antibiotico (prescritta dal medico) (fino alla fine del ciclo di cura) e… via! Tutto va meglio.
Ma non sempre funziona così, e a volte i batteri possono causare danni permanenti. Un batterio in particolare, l‘Helicobacter pylori, infetta lo stomaco e può viverci per decenni, senza essere individuato, ma può causare ogni sorta di problema, persino il cancro.
Sebbene l’H. pylori infetti circa la metà degli adulti in tutto il mondo, le infezioni possono passare inosservate per decenni e rappresentano il principale fattore di rischio per il cancro gastrico. Il cancro gastrico è la quinta causa di morte per cancro più comune a livello mondiale. Dei due principali ceppi di H. pylori esistenti, uno è associato a un rischio di cancro più elevato rispetto all’altro.
Un frammento di DNA chiamato isola di patogenicità Cag è responsabile di questa differenza. L’isola di patogenicità Cag conferisce all’H. pylori componenti di una struttura chiamata sistema di secrezione Cag di tipo IV, noto come T4SS, e un’oncoproteina batterica chiamata CagA. La Cag T4SS trasporta CagA dai batteri alle cellule ospiti. In qualche modo, l’azione della Cag T4SS e della CagA può portare al cancro gastrico.
I ricercatori del Vanderbilt University Medical Center e della Vanderbilt University hanno scoperto come questi due elementi inducano alterazioni molecolari nei tessuti dell’ospite che favoriscono lo sviluppo del cancro gastrico.
I loro risultati sono stati pubblicati il mese scorso su Infection and Immunity.
“Il nostro laboratorio e altri hanno condotto studi approfonditi sulle proteine codificate dall’isola di patogenicità Cag, tra cui CagA e componenti del T4SS”, ha affermato Tim Cover. Cover è Professore di medicina e autore principale dello studio.
“In questo studio, condotto da Jennifer Shuman, ex studentessa laureata e postdoc del mio laboratorio, abbiamo valutato il contributo di Cag T4SS e CagA alle alterazioni molecolari gastriche rilevanti per la carcinogenesi“. Utilizzando un modello animale, i ricercatori hanno testato le differenze tra infezioni da H. pylori selvatico o mutanti di H. pylori con Cag T4SS difettoso o privo di CagA.
Con l’ausilio di strumenti altamente specializzati e con l’aiuto del Proteomics Core Laboratory e dell’Imaging Mass Spectrometry Core, gli autori dello studio hanno analizzato le alterazioni delle proteine e dei trascritti di RNA nei tessuti gastrici di animali infettati da diversi ceppi di H. pylori.
In totale, Cover e coautori hanno rilevato più di mille alterazioni molecolari, oltre a segni di infiammazione, nei tessuti gastrici di animali infettati da un ceppo di H. pylori selvatico – che conteneva Cag T4SS e CagA intatti – ma non nei tessuti infettati da batteri privi di Cag T4SS o CagA funzionali. Nonostante queste differenze, i ceppi mutanti di H. pylori hanno colonizzato con successo lo stomaco degli animali, sebbene senza risposte patologiche rilevabili da parte dell’ospite.
Una progressione graduale di alterazioni patologiche gastriche, nota come “Cascata Correa”, inizia con una gastrite non atrofica (infiammazione della mucosa gastrica in risposta a H. pylori ), che può progredire verso una gastrite atrofica multifocale. La gastrite atrofica può quindi progredire verso una metaplasia intestinale, seguita da displasia. Una volta che si sviluppano la gastrite atrofica e la displasia, il rischio di progressione verso l’adenocarcinoma è quasi 10 volte superiore rispetto agli individui con gastrite non atrofica. La valutazione del tessuto gastrico colorato con ematossilina ed eosina (H&E) è stata lo standard nel campo per rilevare questi esiti patologici dell’infezione.
Leggi anche:Cancro gastrico diffuso ereditario: svelato il mistero
“Questi risultati forniscono informazioni sui meccanismi attraverso i quali l’infezione da H. pylori può portare al cancro gastrico“, ha affermato Cover. “Speriamo che possano anche aiutarci, in futuro, a identificare i soggetti con un’alta probabilità di sviluppare un cancro gastrico, in modo da poterli indirizzare verso un intervento medico mirato“.
Fonte: Infection and Immunity