Sarcoma dei tessuti molli-Immagine Credito: JAMA Oncology (2023)-
La combinazione dell’immunoterapia con le radiazioni potrebbe essere un’opzione terapeutica promettente per i pazienti con sarcoma avanzato dei tessuti molli, secondo i risultati di uno studio clinico condotto da ricercatori della Northwestern Medicine e pubblicato su JAMA Oncology.
Secondo il National Institutes of Health, i sarcomi avanzati dei tessuti molli che non possono essere completamente rimossi con un intervento chirurgico sono generalmente considerati incurabili. “Sono stati fatti pochi progressi utilizzando le attuali immunoterapie e il tempo di sopravvivenza globale per i pazienti con sarcoma dei tessuti molli avanzato è di circa due anni”, hanno affermato il Dott. Seth Pollack e il Dott. Steven T. Rosen, Professore di Biologia del cancro e Professore associato di Medicina presso la Divisione di Ematologia e Oncologia e autore senior dello studio.
Dopo aver studiato numerosi campioni di tessuto dei suoi pazienti affetti da sarcoma, Pollack sperava di alterare l’ambiente immunitario dei tumori introducendo l’immunoterapia, che in ricerche precedenti aveva dimostrato di alterare le cellule T e i macrofagi, due tipi di cellule essenziali per la difesa dell’organismo e risposta immunitaria.
“Il mio laboratorio è davvero interessato ad alterare il microambiente immunitario del tumore per far funzionare meglio l’immunoterapia“, ha detto Pollack, che è anche Direttore del Sarcoma Program presso il Robert H. Lurie Comprehensive Cancer Center della Northwestern University.
“In questo contesto, siamo stati davvero interessati alle radiazioni come metodo per sensibilizzare i tumori all’immunoterapia. Quando abbiamo esaminato i pazienti che avevano appena ricevuto radiazioni standard, abbiamo visto che c’erano molte più cellule immunitarie che vogliamo veramente avere, tuttavia abbiamo anche visto alcune cellule che potrebbero bloccare la risposta immunitaria“, ha spiegato Pollack.
“In particolare, era presente un sottoinsieme di macrofagi che inibivano la risposta immunitaria del corpo”, ha aggiunto il ricercatore. Pollack e i suoi ricercatori hanno teorizzato che l’immunoterapia con glicopiranosil lipide A (GLA) potrebbe attivare i macrofagi affinché agiscano contro il tumore.
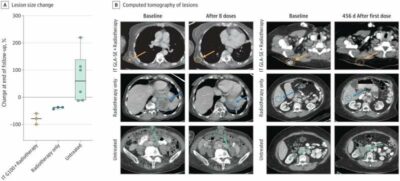
Nello studio, i ricercatori hanno somministrato radioterapia standard insieme a un’iniezione di GLA a 12 pazienti con sarcoma dei tessuti molli avanzato. Dopo otto dosi, tutti i pazienti hanno ottenuto il controllo locale del tumore e in un paziente è stata riscontrata una regressione totale del tumore. Inoltre, il sequenziamento ha rivelato che i pazienti presentavano un numero maggiore di sospette cellule T antitumorali in seguito al trattamento .
Nel complesso, il trattamento è stato ben tollerato e solo un paziente ha manifestato effetti collaterali significativi.
“Quello che abbiamo scoperto è che il GLA sembrava davvero approfondire la risposta alle radiazioni“, ha detto Pollack.
Poiché lo studio era un piccolo studio pilota, sarà necessario un altro studio randomizzato per comprendere appieno l’efficacia del trattamento con GLA.
Leggi anche:Sarcoma di Ewing: scoperto nuovo bersaglio farmacologico
Spiegano gli autori:
“I sarcomi dei tessuti molli (STS) sono un gruppo eterogeneo di oltre 50 distinte neoplasie mesenchimali che insieme costituiscono l’1% di tutti i tumori. Nonostante i progressi incrementali, la sopravvivenza globale mediana per i pazienti con STS metastatico rimane di circa 24 mesi. Sebbene gli inibitori dei checkpoint abbiano attività in alcuni sottotipi di STS, il ruolo dell’immunoterapia nell’STS è ancora in fase di definizione. Il glicopiranosil lipide A in formulazione in emulsione stabile (GLA-SE) è un agonista del recettore toll-like 4 (TLR4) che è un adiuvante affermato per i vaccini contro l’epatite B e contro il papillomavirus umano (sierotipi 16 e 18) ed è stato testato a livello intratumorale in diversi tipi di tumore. Il glicopiranosil lipide A nella formulazione in emulsione stabile è un potente attivatore delle cellule dendritiche e induce una maggiore risposta cellulare TH 1 CD4 + rispetto ad altri agonisti TLR. I ricercatori si sono interessati alla potenziale sinergia tra radioterapia e agonisti TLR4. Poiché i pazienti che si presentano con sarcoma metastatico occasionalmente presentano tumori superficiali sintomatici che richiedono radioterapia, abbiamo cercato di valutare la fattibilità e la sicurezza del GLA-SE intratumorale (IT) e della radioterapia nell’STS metastatico in questo studio pilota di fase 1“.
Conclusione
La radioterapia è uno strumento efficace nella gestione delle metastasi sintomatiche per STS. Questo studio controllato non randomizzato di fase 1 suggerisce che la combinazione di GLA-SE con radioterapia per tumori STS superficiali sintomatici è fattibile ed efficace.La terapia è stata ben tollerata e, sebbene lo studio non fosse stato progettato per confrontare le dosi, non è stata riscontrata alcuna differenza evidente tra le coorti da 5 e 10 μg. Tutti i pazienti hanno avuto un controllo locale con una regressione profonda e duratura osservata in un terzo dei pazienti, con 1 paziente che ha avuto una riduzione delle dimensioni dell’80% e un altro che ha avuto una risposta completa nel sito di iniezione. Sebbene i tassi di controllo locale pubblicati dell’STS metastatico dopo radioterapia siano elevati (>80%), la maggior parte degli studi riguarda metastasi viscerali (ad esempio polmonari) e potrebbe non essere direttamente applicabile. Nei pazienti con lesioni valutabili concomitanti, l’IT GLA-SE con radioterapia può causare una risposta più duratura rispetto alla sola radioterapia, sebbene questo studio non sia stato progettato per effettuare un confronto diretto.
“Stiamo cercando di espandere questo studio in uno studio clinico più ampio e penso che sia anche molto importante pensare a come potremmo essere in grado, di migliorare ulteriormente questi risultati con diverse terapie combinate, in particolare terapie con citochine che potrebbero aiutare anche rafforzare ulteriormente questa risposta“, ha affermato il ricercatore.
Fonte:JAMA Oncology