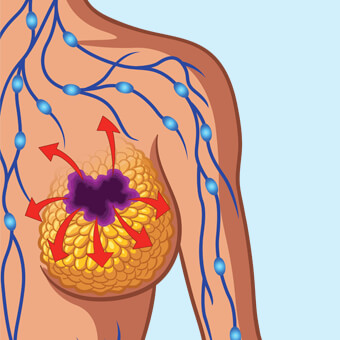
La FDA ha approvato venerdì, il primo farmaco per il trattamento del cancro al seno metastatico legato alla mutazione del gene BRCA.
Questi geni mutati, chiamati BRCA1 e BRCA2, sono diventati famosi nel 2013 quando l’attrice e regista Angelina Jolie ha annunciato di essere stata sottoposta a una mastectomia preventiva doppia. Jolie era portatrice della mutazione del gene BRCA1 che aumenta di molto le probabilità di una donna di sviluppare tumori al seno e alle ovaie.
Ora, la FDA ha approvato il farmaco Lynparza (olaparib) per l’uso nei tumori BRCA-linked che si sono diffusi oltre il seno.
“Lynparza fa parte di un gruppo di potenti nuovi farmaci antitumorali noti come inibitori di PARP ed è il primo farmaco ad essere approvato contro il cancro al seno”, ha osservato la FDA. Lynparza è già stato approvato per il trattamento di alcuni tumori ovarici.
( Vedi anche:L’ estratto di melograno altera le proprietà delle cellule staminali del cancro al seno).
Gli inibitori di PARP sono già stati “usati per il trattamento del carcinoma ovarico avanzato, BRCA-mutato e hanno ora dimostrato l’efficacia nel trattamento di alcuni tipi di carcinoma mammario con BRCA mutato”, ha spiegato il Dr. Richard Pazdur che Dirige il Centro di eccellenza Oncologia della FDA.
Secondo la FDA, le mutazioni BRCA sono coinvolte in un tumore mammario su quattro che si ritiene abbia una componente ereditaria. Questi geni aberranti sono anche implicati nel 5/10 per cento dei tumori al seno non ereditari.
Quando funziona correttamente, BRCA aiuta a riparare il DNA cellulare danneggiato e previene i tumori, ma quando BRCA1 e BRCA2 mutano, incoraggiano lo sviluppo di tumori al seno.
“Farmaci inibitori di PARP come Lynparza sembrano interferire con la funzione di BRCA mutato nelle cellule del seno, causandone la morte piuttosto che la crescita del tumore che rallenta la replica”, ha spiegato la FDA.
La sicurezza e l’efficacia di Lynparza per le donne con carcinomi mammari BRCA-avanzati sono state verificate in uno studio che ha coinvolto oltre 300 pazienti.
“La sperimentazione ha misurato il periodo di tempo in cui i tumori non hanno avuto una crescita significativa dopo il trattamento [sopravvivenza libera da progressione]”, ha spiegato l’agenzia. “La sopravvivenza mediana libera da progressione per i pazienti che assumevano Lynparza era di 7 mesi rispetto ai 4,2 mesi dei pazienti trattati con la sola chemioterapia”.
Lynparza causa effetti collaterali che possono includere anemia, basso numero di globuli bianchi, nausea, affaticamento, vomito, mal di testa, dolori articolari, aumento della suscettibilità al raffreddore e altre infezioni del tratto respiratorio e altri effetti. Poiché Lynparza può danneggiare un feto in via di sviluppo, si consiglia alle donne di usare la contraccezione mentre si trovano in trattamento con il farmaco. Inoltre, le donne non dovrebbero allattare al seno durante l’utilizzo di Lynparza.
Il farmaco è prodotto da AstraZeneca.
Insieme all’approvazione ampliata di Lynparza, la FDA ha affermato di aver “ampliato anche l’approvazione del BRACAnalysis CDx, una diagnostica associata a Lynparza che include il rilevamento delle mutazioni BRCA nei campioni di sangue da pazienti con cancro al seno”.
Una notizia correlata, uno studio pubblicato l’11 gennaio su The Lancet Oncology, ha rilevato che le giovani pazienti con carcinoma mammario trattate con il farmaco lynparza e che presentano una mutazione BRCA non hanno una sopravvivenza più breve rispetto alle pazienti senza la mutazione.
Lo studio, che ha seguito più di 2.700 pazienti per 10 anni, è stato condotto da Diana Eccles dell’Università di Southampton, in Inghilterra.
Fonte:Medicalxpress