Nonostante le cure mediche all’avanguardia, il 22% dei pazienti con STEMI trattati con PPCI sviluppa sintomi di insufficienza cardiaca entro 1 anno. La progressione dannosa è sostanzialmente determinata dalla dimensione dell’infarto originale e dal tempo alla riperfusione. Una risposta proinfiammatoria acuta ed esuberante può ulteriormente aumentare il danno cardiaco locale. Nel tempo, ciò può portare a un rimodellamento ventricolare avverso e a una graduale perdita della funzione cardiaca che può provocare insufficienza cardiaca. Per i pazienti con STEMI, in particolare quelli con infarti di grandi dimensioni, è necessario un ulteriore intervento nella fase acuta per ridurre il danno da ischemia-riperfusione e proteggere il tessuto miocardico, riducendo così il rischio di progressione verso l’insufficienza cardiaca.
Pertanto, attenuare la risposta proinfiammatoria immediata dopo l’ischemia-riperfusione ha il potenziale di proteggere il miocardio sopravvissuto da ulteriori lesioni.
La ricerca sugli effetti protettivi di due molecole antinfiammatorie a seguito di un attacco cardiaco ha scoperto che due proteine riducono la risposta infiammatoria e le cicatrici all’interno del cuore ferito.
Lo studio è pubblicato sull’American Journal of Pathology.
Il fattore di crescita trasformante beta1 (TGFβ1) e l’Heligmosomoidespolygyrus TGM (HpTGM) sono due molecole antinfiammatorie che si sono rivelate benefiche in terapia. I pazienti con attacchi cardiaci acuti (infarto miocardico con sopraslivellamento del tratto ST o STEMI) hanno molte probabilità di sopravvivere se si sottopongono tempestivamente alla riapertura dell’arteria coronaria occlusa (riperfusione coronarica) in centri clinici specializzati.
Tuttavia, nonostante i notevoli miglioramenti nel trattamento, la progressione verso l’insufficienza cardiaca rappresenta ancora un grave problema clinico.
Riduzione delle dimensioni dell’attacco cardiaco dopo tre mesi
La Prof.ssa Helen Arthur, docente di biologia cardiovascolare all’Università di Newcastle, spiega: “La riperfusione coronarica dopo STEMI è la terapia standard per salvare il muscolo cardiaco ischemico. Tuttavia, le prove suggeriscono che la successiva risposta infiammatoria che l’organismo avvia per riparare il tessuto cardiaco danneggiato può anche causare ulteriore perdita di muscolo cardiaco vitale e maggiore è la quantità di muscolo perso maggiore è il rischio di successiva progressione verso l’insufficienza cardiaca.
“Il motivo di questo studio era quello di indagare i potenziali effetti protettivi del TGFβ1 come possibile intervento per ridurre al minimo questo danno aggiuntivo al cuore oltre il danno ischemico causato dall’infarto stesso“.
Il gruppo di ricerca ha scoperto che i livelli di un’importante proteina antinfiammatoria TGFβ1 nel sangue dei pazienti con STEMI 24 ore dopo la riperfusione erano correlati con una riduzione delle dimensioni dell’infarto dopo tre mesi. Per indagare ulteriormente, i ricercatori hanno utilizzato un modello murino consolidato di attacco cardiaco per testare gli effetti protettivi del TGFβ1, una proteina nota per essere rilasciata nel corpo in risposta a un danno tissutale e la sua imitazione dell’HpTGM.
Si tratta di una proteina prodotta da un verme parassita per aiutare a eludere la risposta immunitaria e quindi consentire al verme di vivere all’interno del tessuto che riveste l’intestino. Il rilascio intravascolare di una di queste proteine antinfiammatorie naturali ha ridotto la risposta infiammatoria dannosa all’interno del cuore e, cosa ancora più importante, l’entità del danno cardiaco, come evidenziato dalla ridotta dimensione della cicatrice matura.
I ricercatori sono stati sorpresi di trovare effetti benefici quasi identici del trattamento con TGFβ1 e HpTGM. Sebbene non siano correlate dal punto di vista evolutivo, entrambe queste molecole interagiscono con le cellule in modo simile attivando la stessa via di segnalazione. La dose di terapia antinfiammatoria è stata somministrata al momento della riperfusione, che corrisponde ad un tempo clinicamente utile per un intervento terapeutico nell’uomo.
I ricercatori potrebbero attribuire i risultati benefici all’effetto protettivo di queste molecole sulle cellule endoteliali (le cellule che rivestono i vasi sanguigni che aiutano a regolare l’uscita dei globuli bianchi proinfiammatori dalla circolazione e entrano nel tessuto danneggiato).
TGFβ1 ha proprietà antinfiammatorie ben consolidate, mentre HpTGM è un parassitomimetico con un grande potenziale clinico. Un recente lavoro nel laboratorio Maizels dell’Università di Glasgow ha anche dimostrato che la somministrazione di HpTGM ha un importante effetto antinfiammatorio in modelli murini di colite o infiammazione delle vie aeree, sfruttando il prodotto sviluppato da un parassita per sedare la risposta immunitaria.
Leggi anche:Attacco cardiaco: esame del sangue potrebbe salvarti la vita
Spiegano gli autori:
“La riperfusione coronarica dopo un attacco cardiaco, infarto miocardico acuto con sopraslivellamento del tratto ST (STEMI) è la terapia standard per salvare il muscolo cardiaco ischemico. Tuttavia, le successive risposte infiammatorie all’infarto portano ad un’ulteriore perdita di miocardio vitale. Il fattore di crescita trasformante (TGF)-β1 è una potente citochina antinfiammatoria rilasciata in risposta al danno tissutale. Lo scopo di questo studio era di indagare gli effetti protettivi del TGF-β1 dopo IM. Nei pazienti con STEMI, è stata riscontrata una correlazione significativa ( P = 0,003) tra livelli più elevati di TGF-β1 circolante a 24 ore dopo l’infarto e una riduzione delle dimensioni dell’infarto dopo 3 mesi, suggerendo un ruolo protettivo dell’aumento precoce di TGF-β1 circolante. Un modello murino di riperfusione di ischemia cardiaca è stato utilizzato per dimostrare i molteplici benefici del TGF-β1 esogeno somministrato nella fase acuta. Ciò ha portato ad una dimensione dell’infarto significativamente più piccola (riduzione del 30%, P = 0,025), una riduzione dell’infiltrato infiammatorio (riduzione del 28%, P = 0,015), una minore espressione intracardiaca delle citochine infiammatorie IL-1β e della chemochina (motivo CC) ligando 2 (> riduzione del 50%, P = 0,038 e 0,0004, rispettivamente) a 24 ore e riduzione delle dimensioni della cicatrice a 4 settimane (riduzione del 21%, P = 0,015) dopo la riperfusione. Inoltre, un mimo a basso contenuto fibrogenico di TGF-β1, secreto dal parassita elmintico Heligmosomoides polygyrus, ha avuto un effetto protettivo quasi identico sui cuori di topo feriti. Infine, studi genetici hanno indicato che questo beneficio era mediato dalla segnalazione del TGF-β nell’endotelio vascolare”.
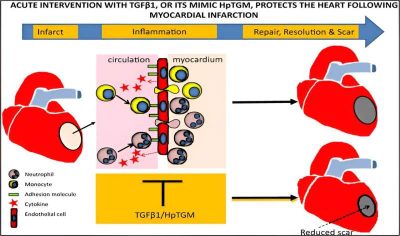
astratto grafico

Immagine Credito American Journal of Pathology
Il Professor Arthur ha concluso: “L’attuale studio dimostra che la somministrazione esogena di HpTGM al momento della riperfusione dell’arteria coronaria smorza la risposta proinfiammatoria delle cellule endoteliali coronariche e riduce il danno cardiaco, portando ad un aumento del salvataggio del miocardio e a una riduzione delle dimensioni della cicatrice, con il corollario di migliori prospettive per la funzione cardiaca a lungo termine. L’uso di HpTGM come terapia antinfiammatoria nel trattamento dei pazienti con infarto è chiaramente una prospettiva entusiasmante che richiede ulteriori studi traslazionali”.