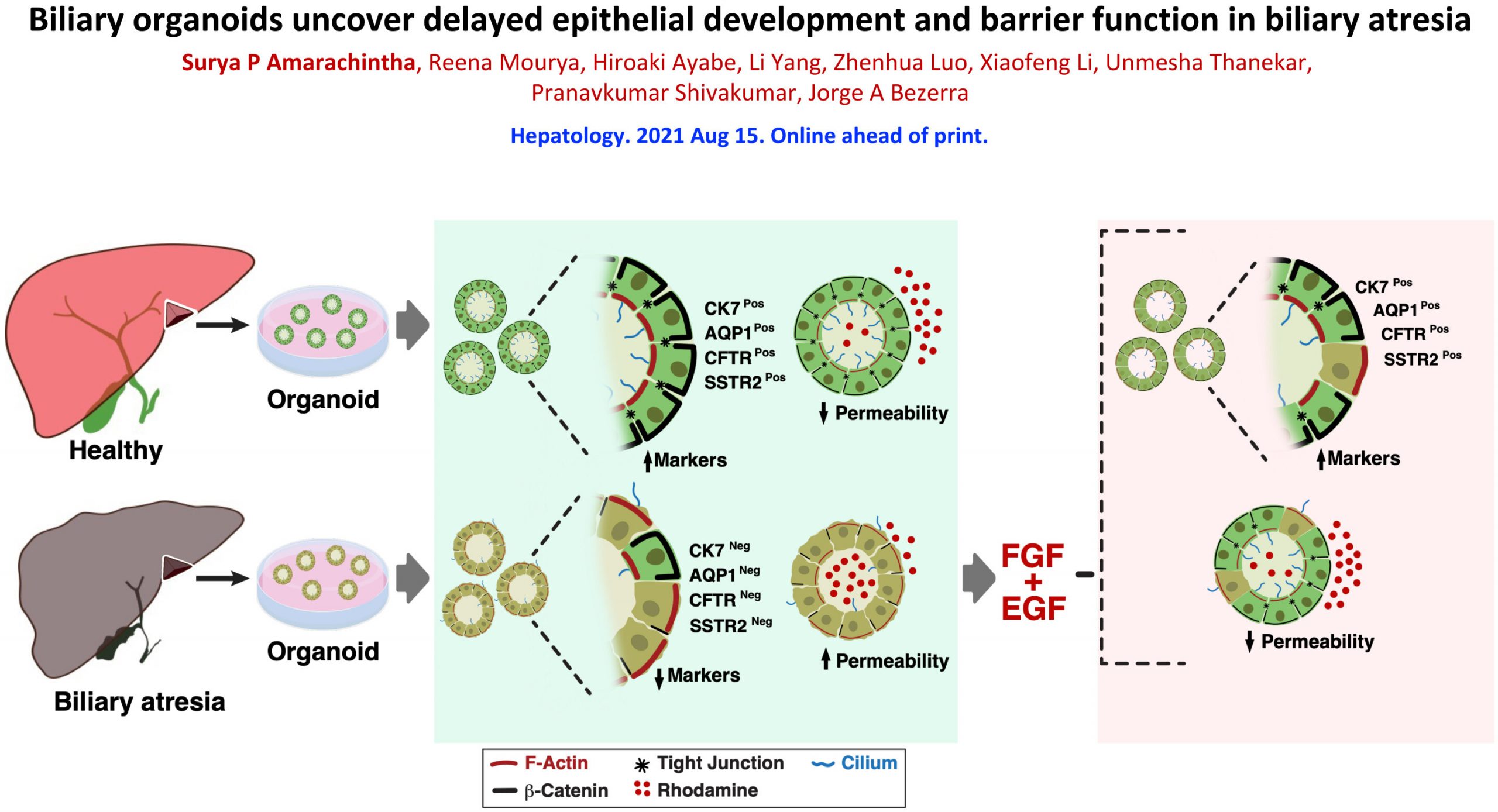
(Atresia biliare-Immagine: dopo aver osservato gli errori di polarità cellulare e permeabilità negli organoidi malati, i ricercatori hanno attivato FGF2 ed EGF per invertire la maggior parte dei difetti. Credito: Cincinnati Children’s).
L’atresia biliare è la principale causa di fibrosi epatica allo stadio terminale nei bambini e la ragione principale per cui i bambini hanno bisogno di trapianti di fegato. Nonostante molti anni di ricerca in tutto il mondo, gli scienziati non hanno ancora trovato un modo per prevenire la condizione.
Ora, uno studio condotto da esperti di fegato presso il Cincinnati Children’s rivela nuovi dettagli sulla malattia che indicano un approccio completamente nuovo per il trattamento. Le scoperte, pubblicate online il 15 agosto 2021 sulla rivista Hepatology, sono state rese possibili dalla capacità del team di far crescere organoidi biliari funzionali da tessuto malato.
“Abbiamo sviluppato questi organoidi senza alcuna manipolazione genetica delle cellule, con cellule che crescono da biopsie epatiche”, affermano Pranav Shivakumar, Ph.D., e Jorge Bezerra, MD, della Divisione di Gastroenterologia, Epatologia e Nutrizione al Cincinnati Children’s e autori senior dello studio. “Questo è importante perché siamo stati in grado di studiare il tessuto umano funzionante derivato da bambini piccoli, piuttosto che fare affidamento su campioni cellulari fissi o modelli murini che non imitano completamente la malattia umana”.
Atresia biliare: osservare un processo patologico in una Piastra di Petri
Confrontando gli organoidi malati con altri cresciuti da campioni di fegato sano, i ricercatori hanno rilevato diversi difetti strutturali che si verificano nelle cellule che formano i minuscoli tubi che trasportano gli acidi biliari lontano dal fegato, un aspetto critico del processo di digestione.
Gli organoidi biliari sani formano sfere di cellule strettamente legate che assumono una forma molto simile alle caramelle. Questa forma aiuta le cellule ad orientarsi per sviluppare superfici interne ed esterne con funzioni distinte. L’estremità superiore delle cellule punta verso l’interno, con ogni cellula che estende un ciglio simile a un capello nel centro della sfera. Le estremità inferiori più larghe delle cellule formano uno strato esterno protettivo. Tuttavia, le cellule negli organoidi malati formavano rivestimenti disorganizzati. Alcune cellule sono state capovolte in modo che le loro ciglia fossero rivolte verso l’esterno. Nel frattempo, invece di stretti legami a prova di perdite tra le cellule, il rivestimento mostrava spazi irregolari tra le cellule che consentivano ai materiali esterni di entrare all’interno.
“Il rivestimento di queste cellule epiteliali forma il dotto biliare che consente il normale flusso della bile dal fegato all’intestino e impedisce che le pareti del dotto biliare vengano danneggiate dagli acidi biliari che trasportano”, afferma Bezerra. “Se il rivestimento non è stretto, consente agli acidi biliari e ad altri substrati di fuoriuscire nella parete del dotto irritando le cellule e portando a un’infiammazione che distrugge il sistema biliare. Quando ciò accade, il fegato sviluppa fibrosi e può progredire fino all’insufficienza epatica“.
Vedi anche:Fibrosi epatica: candidato farmaco tra i pesticidi
Il salvataggio dei condotti difettosi sembra possibile
Mostrare il problema della permeabilità è stato di per sé un passo avanti, reso possibile solo attraverso lo studio degli organoidi funzionanti. Negli esseri umani, questo malfunzionamento comincerebbe presto nello sviluppo fetale, ben prima che qualsiasi campione di tessuto possa essere raccolto per rilevare la scarsa formazione del dotto. Studiando gli organoidi, i ricercatori hanno rilevato differenze di segnalazione cellulare tra organoidi sani e malati che potrebbero essere la causa di anomalie nella formazione di organoidi biliari. Questi segnali erano correlati al fattore di crescita dei fibroblasti-2 (FGF2) e al fattore di crescita epidermico (EGF).
“Quando abbiamo riattivato questi percorsi, abbiamo visto che molte più cellule negli organoidi malati si sono sviluppate correttamente. Gli organoidi trattati non erano perfetti, ma erano molto più vicini alla normalità, il che suggerisce che potrebbero essere in grado di supportare un’adeguata funzione epatica”, Shivakumar dice.
“Quando trattati con EGF e FGF2, gli organoidi dell’atresia biliare hanno mostrato una migliore polarità, una diminuzione della permeabilità e hanno espresso biomarcatori che indicano una funzione quasi normale”, riporta lo studio.
Il team di ricerca che ha ottenuto questo successo include il primo autore Surya Amarachintha, Ph.D. e l’autore corrispondente Pranavkumar Shivakumar, MPharm, Ph.D., entrambi del Cincinnati Children’s. Il team ha anche collaborato con i colleghi del primo Ospedale affiliato e del terzo Ospedale affiliato della Sun Yat-Sen University, Guangzhou, Cina. “Sono necessari molti altri passaggi per trasferire questa scoperta del piatto di laboratorio al trattamento”, afferma Bezerra.
Prossimi passi
- I ricercatori hanno iniziato a lavorare per confermare che i bambini con atresia biliare mostrano anche percorsi FGF2 ed EGF down-regolati.
- Il team deve anche determinare se esistono farmaci esistenti che attivano FGF2 ed EGF, in particolare nei dotti biliari, che sarebbero sicuri anche per i bambini. In caso contrario, forse potrebbe essere sviluppato un nuovo farmaco.
- In definitiva, qualsiasi potenziale trattamento richiederebbe una sperimentazione clinica per determinare se il trattamento modifica i risultati, come la soppressione drammatica della fibrosi progressiva con l’obiettivo di evitare un trapianto di fegato.