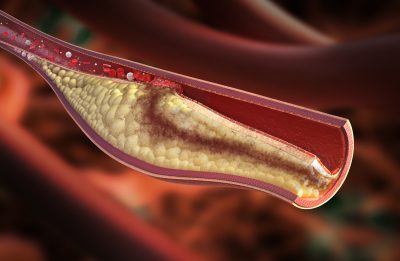
(Aterosclerosi-Immagine Credit Public Domain).
È noto da tempo che una dieta ricca di grassi può portare ad arterosclerosi, ma solo di recente abbiamo iniziato a capire in dettaglio come funziona il processo. Un nuovo studio su topi potrebbe essere molto utile per trovare nuovi trattamenti per mantenere le arterie aperte e fluenti.
Lo studio è stato pubblicato questo mese su JACC Basic To Translational Science.
I ricercatori della Tokyo Medical and Dental University (TMDU) hanno continuato la loro ricerca su come una dieta ricca di grassi provoca l’aterosclerosi, l’accumulo di placche di grasso sulle pareti dei vasi sanguigni che possono portare ad attacchi di cuore e altre malattie vascolari. L’aterosclerosi non è semplicemente una malattia causata dai grassi che rimangono bloccati nelle arterie: in realtà è una malattia infiammatoria guidata dalla risposta immunitaria del corpo, in particolare i neutrofili, i globuli bianchi che attaccano le infezioni e rispondono alle lesioni.
Normalmente, i neutrofili agiscono per regolare la risposta immunitaria, in modo che l’infiammazione possa risolvere il problema permettendo al corpo di tornare al suo stato normale. Ma quando uno stimolo è persistente, la risposta immunitaria può cambiare le sue strategie, diventando una condizione cronica a lungo termine. “Abbiamo applicato questa teoria a ciò che accade nell’aterosclerosi: in questo caso, lo stimolo persistente è la dislipidemia (livelli non salutari di grassi e colesterolo nel sangue). Quindi, dettagliare il ruolo dei neutrofili nell’infiammazione acuta può aiutarci a capire come diventa un’infiammazione cronica“, dice Mizuko Osaka, autrice principale dello studio
Il team ha confrontato un gruppo di topi normali di tipo selvatico con topi allevati appositamente per essere geneticamente privi di recettori per le lipoproteine a bassa densità (LDL) sulle loro membrane cellulari. Questo perché i topi trasportano la maggior parte del colesterolo plasmatico nelle lipoproteine ad alta densità e nel complesso hanno livelli di colesterolo molto più bassi; la mancanza di questi recettori significa che questi topi di laboratorio metabolizzano l’LDL (il colesterolo “cattivo”) più come fanno gli umani. Quando nutriti con una dieta ricca di grassi “umanizzata”, questi topi hanno sviluppato alti livelli di trigliceridi e colesterolo, hanno mostrato livelli significativamente aumentati di adesione dei neutrofili alle pareti dei loro vasi sanguigni e hanno sperimentato molta più infiammazione.
Vedi anche:Aterosclerosi: una proteina la causa dell’infiammazione
“Sulla base di alcuni biomarcatori nei topi LDLR nulli, sospettavamo che le trappole extracellulari dei neutrofili (NET, che aiutano a intrappolare ed eliminare i patogeni dal corpo) potessero essere coinvolte nell’attivazione dei neutrofili“, spiega Masayuki Yoshida, autore senior dello studio . “E infatti, abbiamo trovato una citrullinazione potenziata dell’istone H3, un noto marcatore di NET, in questi topi. (La citrullinazione è una modifica post-traduzionale delle proteine, con la trasformazione dei residui di arginina nell’aminoacido atipico citrullina). Andando oltre, abbiamo identificato specificamente i livelli plasmatici di CXCL1 (un peptide che agisce per attirare le cellule immunitarie nel sito di una lesione o infezione) essere significativamente aumentato nei topi LDLR-null dopo 7 giorni e 28 giorni di dieta ricca di grassi”.
Astratto:
Ciò suggerisce che CXCL1 è il legame tra la dieta ricca di grassi e la citrullinazione, parte del processo di produzione dei NET, e che porta alla formazione di placche di neutrofili sulle pareti dei vasi sanguigni quando sovrastimolati a lungo termine. In effetti, il blocco del processo di citrullinazione ha portato a un’inversione dell’aumentata adesione dei neutrofili.
Spiegano gli autori:
“L’eccessiva assunzione di grassi e la conseguente dislipidemia sono fattori di rischio per l’aterosclerosi. Diversi studi hanno dimostrato che l’infiammazione vascolare, il principale meccanismo che causa l’aterosclerosi, è collegata a una dieta ricca di grassi (HFD) o dislipidemia. In uno studio precedente, abbiamo riportato che l’HFD induce l’ adesione dei neutrofili all’endotelio vascolare arterioso nei topi wild-type (wt). L’adesione dei neutrofili osservata è stata indotta dall’aumento del fattore del complemento C5a, un modulatore chiave nel sistema del complemento. Il nostro risultato ha scoperto un nuovo meccanismo di transizione che collega l’infiammazione acuta all’infiammazione cronica nel contesto dell’infiammazione vascolare indotta da HFD e fa luce sui neutrofili come attori dominanti in questo processo. Tuttavia, non siamo stati in grado di dimostrare il coinvolgimento dei neutrofili nell’infiammazione vascolare associata alla formazione di lesioni aterosclerotiche perché i topi wt sono resistenti alla formazione di lesioni dopo l’alimentazione con HFD. Inoltre, i ruoli dei neutrofili, che sono attori chiave nell’infiammazione acuta nell’aterosclerosi, non sono stati studiati a fondo. Pertanto, questo studio ha esaminato il coinvolgimento dei neutrofili nell’infiammazione vascolare associata all’aterosclerosi. Inoltre, abbiamo ipotizzato che le differenze nell’attivazione dei neutrofili indotta da HFD tra topi wt e aterosclerotici possano influenzare l’infiammazione vascolare correlata all’aterosclerosi. Questo studio ha cercato di indagare il meccanismo dettagliato alla base del modo in cui i neutrofili contribuiscono all’infiammazione vascolare indotta da HFD in modelli di aterosclerosi come i topi con recettore nullo delle lipoproteine a bassa densità (LDLR-/-). Rapporti recenti evidenziano un ruolo emergente delle trappole extracellulari dei neutrofili (NET) in vari processi di attivazione dei neutrofili come la protezione contro l’infezione e l’adesione delle piastrine per indurre la trombosi venosa profonda. È stato dimostrato che i NET vengono avviati da un’interruzione della struttura della cromatina nel nucleo attraverso la citrullinazione dell’istone. La citrullinazione dell’istone è mediata dalla peptidilarginina deiminasi 4 (PAD4), un membro della famiglia di enzimi PAD. PAD4 attivato converte i residui di arginina nei residui di citrullina dell’istone, che innesca il cambiamento conformazionale del complesso istonico. Studi più recenti hanno identificato il coinvolgimento della citrullinazione in vari fenomeni fisiopatologici, come la trascrizione genica e la proliferazione cellulare. La citrullinazione o NET sono indotti da stress ossidativo , lipopolisaccaridi e N -formil-metionil-leucil-fenilalanina. Tuttavia, il coinvolgimento dei componenti lipidici nella citrullinazione degli istoni nei neutrofili non è ben noto. La dislipidemia, come l’ipertrigliceridemia e l’ipercolesterolemia, provoca infiammazione vascolare e aterosclerosi. Recentemente, è stato dimostrato che un nuovo modulatore selettivo del recettore attivato dal proliferatore dei perossisomi (PPAR) ha l’effetto di abbassare il livello di trigliceridi (TG) nel sangue di esseri umani e roditori attraverso la regolazione del trasporto degli acidi grassi e della ossidazione. Pertanto, abbiamo dimostrato l’induzione della citrullinazione dell’istone nei neutrofili mediante dislipidemia utilizzandotopi LDLR -/-come modello animale. In questo studio, riportiamo che l’infiammazione vascolare indotta da HFD comporta il miglioramento della citrullinazione nei topi LDLR -/- ma non nei topi wt. Il meccanismo sottostante sembra essere un’attivazione dei neutrofili mediata dal segnale CXCL1-CXCR2 attraverso la citrullinazione PAD4-dipendente dell’istone H3. I nostri risultati suggeriscono un nuovo meccanismo che può facilitare la transizione dall’infiammazione acuta a quella cronica nell’infiammazione vascolare aterosclerotica“.
Una volta compreso appieno come si manifesta una malattia, è più facile sviluppare strategie per prevenirla. Infatti, sebbene i topi siano metabolicamente diversi dalle persone, è possibile che alcuni farmaci già utilizzati per controllare il colesterolo possano essere utilizzati per ridurre l’adesione dei neutrofili influenzando i percorsi identificati in questo studio.