La proteina β-arrestin-2 aumenta l’accumulo di grovigli di tau neurotossici, una causa di diverse forme di demenza come la demenza frontotemporale e Alzheimer, interferendo con la rimozione dell’eccesso di tau dal cervello, secondo un nuovo studio dell’Università della South Florida Health (USF Health) Morsani College of Medicina.
I ricercatori della USF Health hanno scoperto che una forma della proteina composta da più molecole β-arrestin-2, nota come β-arrestin-2 oligomerizzato, interrompe il processo di clearance protettiva che normalmente libera da proteine malformate come la tau che causa la malattia. β-arrestin-2 monomerico, la forma a singola molecola della proteina, non compromette questo processo di smaltimento dei rifiuti tossici cellulari noto come autofagia.
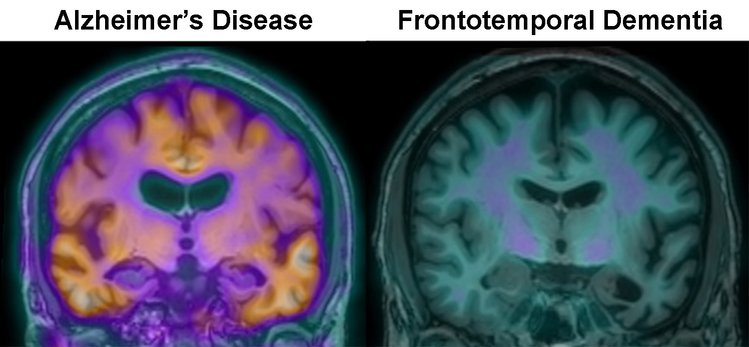
I risultati dello studio sono stati pubblicati oggi negli Atti della National Academy of Sciences (PNAS). Lo studio si è concentrato sulla degenerazione del lobo frontotemporale (FTLD), chiamata anche demenza frontotemporale, seconda solo alla malattia di Alzheimer come principale causa di demenza. Questa demenza aggressiva, tipicamente precoce (età 45-65 anni) è caratterizzata da atrofia delle regioni frontali o laterali del cervello o di entrambi. Come la malattia di Alzheimer, FTLD mostra un accumulo di tau e non ha trattamenti o cure specifici.
“La nostra ricerca potrebbe portare a una nuova strategia per bloccare la patologia tau nella FTLD, nella malattia di Alzheimer e in altre forme di demenza correlate, che alla fine distruggono le capacità cognitive come ragionamento, comportamento, linguaggio e memoria“, dice JungA (Alexa) Woo, PhD, autore principale del documento, assistente Professore di farmacologia e fisiologia molecolare e ricercatore presso l’USF Health Byrd Alzheimer’s Center. “È sempre stato un mistero il motivo per cui il cervello non è in grado di eliminare l’accumulo di tau”, ha dichiarato Stephen B. Liggett, MD, autore senior e Professore di medicina e ingegneria medica presso l’USF Health Morsani College of Medicine. “Sembra che si verifichi una “interazione accidentale” tra β-arrestin-2 e il meccanismo di eliminazione di tau, portando a queste demenze. β-arrestin-2 stessa non è dannosa, ma questa interazione imprevista sembra essere la base di questo mistero“.
“Questo studio identifica beta-arrestin-2 come un responsabile chiave nell’accumulo progressivo di tau nel cervello dei pazienti affetti da demenza“, ha dichiarato il coautore David Kang, PhD, Professore di medicina molecolare e Direttore della ricerca di base per il Byrd Alzheimer’s Center. “Illustra inoltre chiaramente una strategia innovativa per ridurre terapeuticamente la tau patologica mirando specificamente all’oligomerizzazione beta-arrestina”.
I due tratti distintivi principali del morbo di Alzheimer sono gruppi di frammenti di proteina appiccicosa di beta-amiloide (Aβ) noti come placche di amiloide e grovigli di soffocamento dei neuroni di una proteina chiamata tau. Accumuli anomali di entrambe le proteine sono necessari per guidare la morte delle cellule cerebrali o dei neuroni nell’Alzheimer, anche se gli accumuli di tau ora sembrano correlarsi meglio con la disfunzione cognitiva rispetto agli accumuli delle Aβ e i farmaci che agiscono su Aβ sono stati deludenti come trattamento. L’aggregazione di Aβ è assente nel cervello di pazienti con FTLD, dove la caratteristica chiave della neurodegenerazione sembra essere un eccessivo accumulo di tau, noto come tauopatia. I grovigli neurofibrillari risultanti – fibre intrecciate cariche di tau – distruggono la comunicazione sinaptica tra i neuroni, uccidendo infine le cellule cerebrali.
“Studiare la FTLD ci ha fornito quella finestra per studiare una caratteristica chiave di entrambi i tipi di demenza, senza la confusione di alcun componente Aβ”, ha detto il Dr. Woo. β-arrestin-2 monomerico è principalmente noto per la sua capacità di regolare i recettori, le molecole sulla cellula che sono responsabili della segnalazione di ormoni e neurotrasmettitori. β-arrestin-2 può anche formare più unità di interconnessione, chiamate oligomeri. La funzione degli oligomeri β-arrestin-2 non è ancora ben compresa. La forma monomerica è stata la base per gli studi iniziali del laboratorio che hanno esaminato la tau e la sua relazione con la neurotrasmissione e i recettori, “ma presto siamo stati trafitti da questi oligomeri di β-arrestin-2“, ha detto il Dott. Woo.
Vedi anche:Scarse prestazioni cognitive possono predire la progressione verso l’Alzheimer
Tra i risultati dei ricercatori riportati in PNAS:
-Sia nelle cellule che nei topi con elevati livelli di tau, i livelli di β-arrestin-2 sono aumentati. Inoltre, quando β-arrestin-2 è sovraespresso, i livelli di tau aumentano, suggerendo un ciclo di feedback disadattivo che aggrava la tau che causa la malattia,
-La riduzione genetica di β-arrestin-2 riduce la tauopatia, la disfunzione sinaptica e la perdita di cellule nervose e le loro connessioni nel cervello. Per questo esperimento i ricercatori hanno incrociato un modello murino di tauopatia precoce con topi geneticamente modificati in cui il gene β-arrestin-2 è stato inattivato o eliminato.
–β-arrestin-2 oligomerizzato – ma non la forma monomerica della proteina – aumenta la tau. I ricercatori hanno bloccato le molecole β-arrestin-2 dal legame per creare forme oligeromizzate della proteina. Hanno dimostrato che la tau patogena è diminuita significativamente quando era presente solo β-arrestin-2 oligomerico, che si lega ai recettori.
–β-arrestin-2 oligomerizzato aumenta la tau impedendo la capacità della proteina cargo p62 di aiutare a degradare selettivamente la tau in eccesso nel cervello. In sostanza, ciò riduce l’efficienza del processo autofagico necessario per eliminare la tau tossica, quindi tau “intasa” i neuroni.
–Il blocco dell’oligomerizzazione β-arrestin-2 sopprime la tau patogena in un modello murino che sviluppa tauopatia umana con segni di demenza.
“Abbiamo anche notato che la riduzione di β-arrestin-2 con la terapia genica non ha avuto effetti collaterali apparenti, ma una tale riduzione è stata sufficiente per aprire il meccanismo di eliminazione tau a tutto gas, cancellando i grovigli di tau come cancella una gomma”, ha detto il Dott. Liggett. “Questo è qualcosa che la ricerca ha sempre cercato: un intervento che non danneggia e inverte la malattia”.
“In base ai nostri risultati, ci aspettiamo che gli effetti dell’inibizione dell’oligomerizzazione β-arrestin-2 non solo inibiscano lo sviluppo di nuovi grovigli di tau, ma possano anche eliminare gli accumuli di tau esistenti a causa del meccanismo di miglioramento della clearance di tau“, hanno scritto gli autori per concludere.
Il lavoro è coerente con una nuova strategia di trattamento che potrebbe essere preventiva per le persone a rischio o con lieve deficit cognitivo e anche per le persone con demenza palese causata dalla tau, diminuendo i grovigli di tau esistenti.
Fonte: News Medical