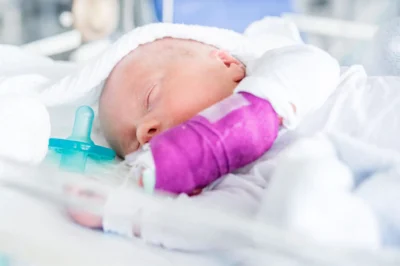
Aciduria metilmalonica-Immagine:nell’aciduria metilmalonica, un metabolita specifico si accumula nel corpo. Questo porta spesso a pazienti che richiedono cure mediche intensive. Crediti: Ospedale pediatrico universitario di Zurigo / Valérie Jaquet-
L’aciduria metilmalonica (MMA) è una rara malattia metabolica che colpisce circa un neonato su 90.000. Entrambi i genitori devono portare la predisposizione genetica perché si verifichi la malattia. Anche le conseguenze sono gravi: un enzima di cui questi giovani pazienti hanno bisogno per il metabolismo energetico rimane difettoso.
A causa dell’enzima difettoso, uno specifico metabolita si accumula nel corpo causando danni invece di essere scomposto per produrre energia. La MMA è attualmente considerata incurabile.
I pazienti possono sperimentare ritardo della crescita, insufficienza renale e grave compromissione neurologica. I bambini e gli adolescenti affetti usano spesso sedie a rotelle e non sempre sopravvivono per raggiungere l’età adulta.
La rete porta il successo
L’Ospedale pediatrico universitario di Zurigo è uno dei principali centri mondiali per la diagnosi e il trattamento di questa malattia. Campioni di pazienti provenienti da tutto il mondo vengono inviati a Zurigo per la diagnosi. In un grande progetto interdisciplinare, scienziati di vari Istituti di ricerca svizzeri hanno studiato in dettaglio 210 biopsie. Hanno esaminato non solo tutti i geni (DNA) nelle cellule del paziente, ma anche le trascrizioni dell’RNA di questi geni e molte delle proteine.
Questa è la prima volta che l’MMA viene studiata utilizzando un approccio multi-omico (genomica, trascrittomica, proteomica, metabolomica). Il lavoro è stato avviato e finanziato dall’area di interesse strategico del dominio dell’ETH per la salute personalizzata e le tecnologie correlate (PHRT) e ha coinvolto ricercatori dell’Ospedale pediatrico universitario di Zurigo, ETH di Zurigo, EPFL, dell’Università di Zurigo e dell’Health 2030 Genome Center di Ginevra. L’analisi molecolare è stata effettuata presso lo Swiss Multi-Omics Center (SMOC) di PHRT a Zurigo.
Vedi anche:Malattia genetica rara e mortale trattata con successo in utero per la prima volta
Maggiore accuratezza della diagnosi
Fino ad ora, i medici si sono affidati principalmente al sequenziamento del DNA per la diagnosi genetica dell’Aciduria metilmalonica. “Tuttavia, questo approccio ha portato a ripetuti casi in cui la diagnosi corretta è stata trascurata”, riferisce Sean Froese, leader del gruppo di ricerca presso l’Ospedale pediatrico universitario di Zurigo e co-autore senior dello studio. Sforzi precedenti hanno riportato che solo da un terzo alla metà di tutti i casi possono essere diagnosticati correttamente in questo modo. “Il motivo è che tutti, anche gli individui sani, hanno molte mutazioni genetiche naturali che non hanno alcun impatto apparente sulla salute umana, quindi è difficile trovare quella o due che effettivamente causano la malattia“, afferma Bernd Wollscheid, Professore presso il Dipartimento di Scienze e tecnologia della salute presso l’ETH di Zurigo, capo del comitato esecutivo di PHRT e coautore dello studio.
Scegliendo di ampliare in modo significativo la loro indagine molecolare, i ricercatori hanno considerato non solo la causa genetica della malattia, ma anche le sue conseguenze in termini di RNA, proteine e funzione delle proteine. Ciò ha consentito al consorzio, nell’ambito di questo studio, di sviluppare una strategia diagnostica che ha diagnosticato correttamente l’84% dei pazienti esaminati. “Andando avanti, il nostro nuovo metodo aumenterà drasticamente le possibilità per i pazienti di ricevere una diagnosi corretta“, afferma Patrick Forny, medico senior presso l’Ospedale pediatrico universitario di Zurigo e co-autore principale dello studio. “Ciò consentirà di fornire il trattamento corretto in una fase molto precoce”.
Un nuovo approccio alla terapia
I dati multi-omici hanno anche mostrato che i pazienti affetti da aciduria metilmalonica utilizzano una fonte di energia alternativa per far fronte al fatto che un enzima vitale è difettoso. Tuttavia, nei pazienti, questa fonte di energia alternativa di solito non è in grado di compensare sufficientemente la produzione di energia persa. In esperimenti in vitro con cellule di pazienti, i ricercatori sono riusciti a portare la produzione di energia a livelli quasi normali fornendo una tale fonte di energia alternativa.
Indagini future mostreranno se un tale approccio avrà lo stesso effetto nei modelli animali e può tradursi in una terapia fattibile per i pazienti. Inoltre, i ricercatori hanno lanciato un nuovo progetto nazionale interdisciplinare e interistituzionale chiamato SwissPedHealth, cofinanziato da PHRT e dalla Rete svizzera di salute personalizzata (SPHN), per aumentare ulteriormente l’efficacia diagnostica ed estendere l’approccio multi-omico ad altre malattie genetiche.
Fonte:Nature Metabolism