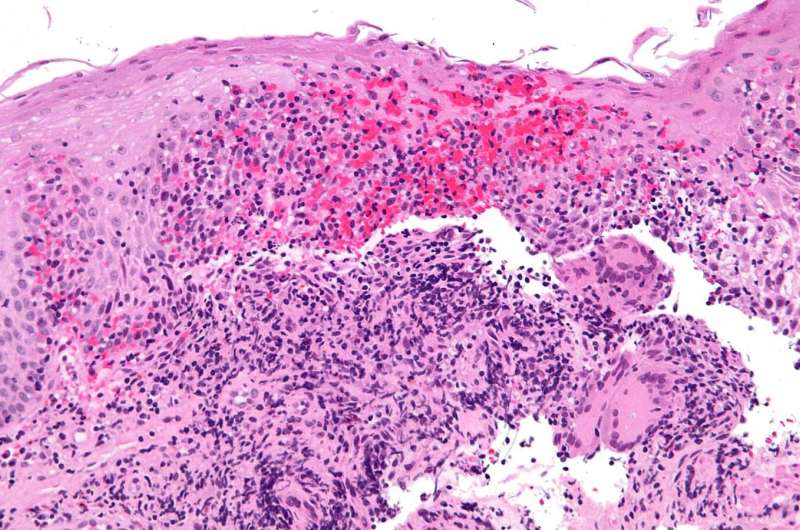
Micrografia ad alto ingrandimento del morbo di Crohn. Biopsia dell’esofago. Colorazione H&E. Credito:Nephron/Wikipedia.
I risultati di uno studio di fase III condotto da un team internazionale di ricercatori tra i quali il Prof. Marc Ferrante, Dipartimento di Gastroenterologia ed Epatologia, Ospedali Universitari di Lovanio in Belgio, rivela che il farmaco Mirikizumab è più efficace e ha un profilo di sicurezza favorevole, con meno eventi avversi gravi rispetto al placebo, nei soggetti affetti da morbo di Crohn in fase attiva da moderata a grave.
Il morbo di Crohn è una malattia infiammatoria intestinale cronica e progressiva caratterizzata da infiammazione che colpisce tutti gli strati della parete intestinale, portando potenzialmente a danni intestinali irreversibili e disabilità.
Gli attuali trattamenti spesso non riescono a raggiungere un controllo duraturo dei sintomi e la guarigione della mucosa. Studi precedenti hanno identificato l’Interleuchina-23 come una citochina critica nella patogenesi della malattia, rendendola un potenziale bersaglio per nuovi interventi terapeutici.
Nello studio, “Efficacia e sicurezza del Mirikizumab nei pazienti con malattia di Crohn moderatamente-severamente attiva: uno studio di fase 3, multicentrico, randomizzato, in doppio cieco, controllato con placebo e con controllo attivo, treat-through”, pubblicato online su The Lancet, i ricercatori hanno arruolato 1.150 pazienti adulti in 324 siti in 33 paesi che avevano mostrato intolleranza o risposta inadeguata ad almeno una terapia biologica o convenzionale approvata. I partecipanti sono stati assegnati in modo casuale a ricevere Mirikizumab, Ustekinumab o un placebo.
Il Mirikizumab è un anticorpo monoclonale ingegnerizzato già approvato per il trattamento della colite ulcerosa. Il Mirikizumab colpisce e inibisce la subunità p19 dell’interleuchina-23 con un effetto a valle che i ricercatori sperano possa silenziare il percorso dell’infiammazione associato al morbo di Crohn.
Gli endpoint coprimari hanno valutato la superiorità del Mirikizumab rispetto al placebo valutando la risposta clinica riferita dal paziente alla settimana 12, combinata con la risposta endoscopica o la remissione clinica mediante l’indice di attività della malattia di Crohn (CDAI) alla settimana 52.
I risultati hanno rivelato che il 38,0% dei pazienti trattati con Mirikizumab ha raggiunto l’endpoint combinato di risposta clinica alla settimana 12 e risposta endoscopica alla settimana 52, rispetto al 9,0% nel gruppo placebo. Inoltre, il 45,4% del gruppo Mirikizumab ha raggiunto la remissione clinica alla settimana 52 rispetto al 19,6% del placebo.
Rispetto a Ustekinumab nel raggiungimento della remissione clinica alla settimana 52, il 54,1% dei pazienti trattati con Mirikizumab ha raggiunto la remissione rispetto al 48,4% di Ustekinumab. Nella risposta endoscopica alla settimana 52, il 48,4% dei pazienti trattati con Mirikizumab rispetto al 46,3% dei pazienti trattati con Ustekinumab ha raggiunto questo endpoint.
L‘incidenza di eventi avversi e interruzioni è stata inferiore nel gruppo Mirikizumab rispetto al placebo. Eventi avversi gravi si sono verificati nel 10,3% dei pazienti trattati con Mirikizumab, nel 10,7% con Ustekinumab e nel 17,1% con placebo. Il profilo di sicurezza di Mirikizumab era coerente con i risultati precedenti, indicando un rapporto beneficio-rischio favorevole per il suo utilizzo nel trattamento del morbo di Crohn attivo.
Leggi anche:Morbo di crohn: scoperto possibile fattore scatenante
I risultati della sperimentazione indicano che il Mirikizumab può rispondere a esigenze mediche insoddisfatte offrendo opzioni di trattamento più durature ed efficaci. La capacità del Mirikizumab di mantenere la remissione clinica e ridurre l’infiammazione per 52 settimane è altamente incoraggiante per il suo potenziale ruolo nel migliorare la qualità della vita delle persone che combattono il morbo di Crohn.
Fonte:The Lancet
