Uno studio condotto dal Ludwig Cancer Research ha scoperto che i tumori ricorrenti del glioblastoma multiforme (GBM), un tumore cerebrale aggressivo, crescono dalle cicatrici fibrose dei predecessori maligni distrutti da interventi quali radioterapia, chirurgia e immunoterapia.
Guidato da Johanna Joyce, Spencer Watson e dall’ex studente Anoek Zomer di Ludwig Lausanne e pubblicato nell’attuale numero di Cancer Cell, dove è stato pubblicato in copertina, lo studio descrive come queste cicatrici consentano la ricrescita dei tumori e identifica i bersagli farmacologici per sabotare il loro supporto maligno. Dimostra inoltre l’efficacia di tali terapie combinate in studi preclinici utilizzando modelli murini di GBM.
“Abbiamo identificato la cicatrizzazione fibrotica come una fonte chiave di recrudescenza del GBM dopo la terapia, mostrando come crea una nicchia protettiva per la ricrescita del tumore”, ha affermato Joyce. “I nostri risultati suggeriscono che bloccare il processo di cicatrizzazione nel cervello aggiungendo agenti anti-fibrosi alle attuali strategie di trattamento potrebbe aiutare a prevenire la recidiva del glioblastoma e migliorare i risultati della terapia”.
C’è un grande bisogno di tali interventi. Il glioblastoma multiforme è la forma più comune e aggressiva di cancro al cervello negli adulti. Nonostante i notevoli sforzi per sviluppare terapie efficaci per questo cancro, l’aspettativa di vita media dei pazienti rimane di circa 14 mesi dopo la diagnosi.
Le origini dello studio attuale risalgono al 2016, quando il laboratorio Joyce ha riportato sulla rivista Science il suo esame nei modelli murini di strategie per superare la resistenza a una promettente immunoterapia per il trattamento del GBM. Quella terapia sperimentale, che inibisce la segnalazione del recettore del fattore stimolante le colonie-1 (CSF-1R) ed è in fase di valutazione in studi clinici oggi, ha come bersaglio le cellule immunitarie note come macrofagi e le loro versioni residenti nel cervello, la microglia, entrambe manipolate dalle cellule GBM per supportare la crescita e la sopravvivenza del tumore.
Il laboratorio Joyce ha dimostrato che l’inibizione del CSF-1R riprogramma queste cellule immunitarie in uno stato antitumorale e quindi induce una significativa regressione del tumore. Tuttavia, come ha dimostrato lo studio di Science, circa metà dei topi mostra una ricaduta dopo una risposta iniziale alla terapia. “La cosa più notevole di questa osservazione è che ogni volta che un tumore al cervello si ripresentava dopo l’immunoterapia, ricresceva proprio accanto a una cicatrice che si era formata nel sito originale di un tumore“, ha affermato Joyce.
Nello studio attuale, Joyce, Watson, Zomer e i loro colleghi hanno esaminato campioni tumorali ottenuti da pazienti sottoposti a terapia GBM e hanno dimostrato che la cicatrizzazione fibrotica si verifica anche negli esseri umani a seguito della terapia, e che è associata in modo simile alla recidiva del tumore. Hanno anche dimostrato che la cicatrizzazione fibrotica si verifica in risposta non solo all’immunoterapia, ma anche a seguito della rimozione chirurgica e radiologica dei tumori.
Per esplorare il modo in cui la fibrosi contribuisce alla recidiva, i ricercatori hanno utilizzato una serie integrata di tecnologie avanzate per analizzare la geografia cellulare e molecolare delle cicatrici e il microambiente dei tumori in recrudescenza.
Queste tecnologie includono l’analisi dell’espressione genica globale nelle singole cellule, l’analisi completa delle proteine nei tessuti, nonché un flusso di lavoro e una suite di metodi analitici basati sull’intelligenza artificiale per l’analisi spaziale dei tessuti denominata imaging a immunofluorescenza iperplessa (HIFI). Sviluppato di recente da Watson e colleghi nel laboratorio Joyce, HIFI consente la visualizzazione simultanea di più marcatori molecolari nelle cellule e attorno ad esse attraverso ampie sezioni trasversali dei tessuti, consentendo la generazione di mappe granulari del microambiente tumorale.
“Applicati insieme, questi metodi avanzati ci hanno permesso di vedere esattamente come si formano le cicatrici fibrotiche“, ha detto Watson. “Hanno rivelato che la fibrosi funge da una specie di bozzolo protettivo per le cellule tumorali residue e le spinge in uno stato dormiente in cui sono ampiamente resistenti alla terapia. Abbiamo scoperto che le protegge anche dalla sorveglianza e dall’eliminazione da parte del sistema immunitario“.
“Analisi integrate del microambiente tissutale dopo la terapia hanno rivelato che i discendenti delle cellule associate ai vasi sanguigni che alimentano il tumore vengono alterati funzionalmente fino a somigliare ai fibroblasti, cellule produttrici di fibre comunemente coinvolte nella guarigione delle ferite”, spiegano gli autori.
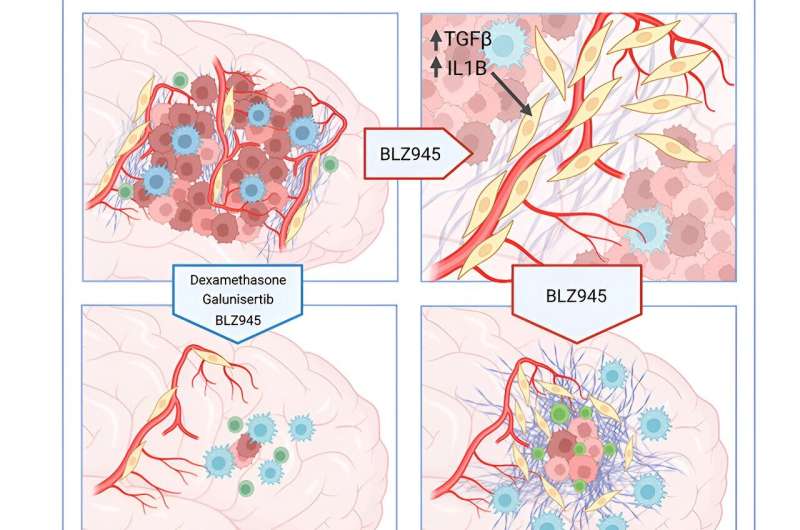
Queste cellule simili ai fibroblasti di derivazione perivascolare (PDFL) si diffondono nella regione precedentemente occupata dal tumore in regressione, dove mediano la generazione di cicatrici fibrotiche. I ricercatori hanno scoperto che queste cellule sono attivate in modo particolare dalla neuroinfiammazione e da fattori immunitari noti come citochine, in particolare uno chiamato fattore di crescita trasformante-β (TGF-β).
“Per verificare se colpire le cicatrici fibrotiche potesse migliorare i risultati terapeutici del GBM, abbiamo ideato un regime di trattamento utilizzando farmaci esistenti per bloccare la segnalazione del TGF-β e sopprimere la neuroinfiammazione in combinazione con l’inibizione del CSF-1R e lo abbiamo valutato in studi preclinici utilizzando modelli murini di GBM“, ha affermato Joyce.
“Abbiamo anche programmato questi trattamenti aggiuntivi in modo che coincidessero con il periodo di massima attivazione del PDFL identificato dai nostri studi. I nostri risultati mostrano che la combinazione di farmaci ha inibito la cicatrizzazione fibrotica, ridotto il numero di cellule tumorali sopravvissute e prolungato la sopravvivenza dei topi trattati rispetto ai controlli“.
Leggi anche:Glioblastoma: sviluppato nuovo dispositivo per la diagnosi
I ricercatori suggeriscono che gli approcci per limitare le cicatrici fibrotiche potrebbero migliorare significativamente i risultati per i pazienti GBM sottoposti a terapie chirurgiche, radioterapiche o mirate ai macrofagi. “Ulteriori ricerche”, notano gli autori, “probabilmente produrranno bersagli farmacologici ancora migliori per tali terapie combinate”.
Fonte:Cancer Cell
