Degenerazione retinica ereditaria-Immagine: Jason Comander, MD, Ph.D., Direttore del Servizio per i disturbi retinici ereditari presso Mass Eye and Ear, esamina la medicina basata su CRISPR prima di eseguire un intervento chirurgico con il nuovo trattamento nel settembre 2020, presso Mass Eye and Ear di Boston. Credito Mass Eye and Ear.
I risultati di uno studio clinico sull’editing genetico CRISPR in 14 individui con una forma di degenerazione retinica ereditaria mostrano che il trattamento è sicuro e ha portato a miglioramenti misurabili in 11 dei partecipanti trattati. Lo studio di Fase I/II denominato BRILLIANCE, è stato condotto dal ricercatore principale Eric Pierce, MD, Ph.D., di Mass Eye and Ear, un membro del sistema sanitario Mass General Brigham.
La degenerazione retinica ereditaria associata a CEP290 provoca una grave perdita della vista a esordio precoce a causa di varianti patogene in CEP290. EDIT-101 è un complesso di modifica genetica della proteina 9 (Cas9) associata a brevi ripetizioni palindromiche regolarmente interspaziate (CRISPR) – per trattare la degenerazione retinica ereditaria causata da una specifica variante dannosa nell’introne 26 di CEP290 (variante IVS26).
I risultati dello studio sono stati riportati il 6 maggio sul New England Journal of Medicine.
“Questa ricerca dimostra che la terapia genica CRISPR per la perdita ereditaria della vista merita di essere proseguita nella ricerca e negli studi clinici“, ha affermato Pierce, Direttore dell’Ocular Genomics Institute e del Berman-Gund Laboratory for the Study of Retinal Degenerations presso Mass Eye and Ear e Harvard Medical Scuola.
“Sebbene siano necessarie ulteriori ricerche per determinare chi potrebbe trarne maggiori benefici, consideriamo i primi risultati promettenti. Sentire da diversi partecipanti quanto fossero entusiasti di poter finalmente vedere il cibo nei loro piatti, è un enorme risultato. Erano individui che non riuscivano a leggere alcuna riga su una mappa oculistica e non avevano opzioni terapeutiche, il che è la sfortunata realtà per la maggior parte delle persone con disturbi retinici ereditari“.
Tutti i 14 partecipanti allo studio, inclusi 12 adulti (di età compresa tra 17 e 63 anni) e due bambini (di età compresa tra 10 e 14 anni), sono nati con una forma di amaurosi congenita di Leber (LCA) causata da mutazioni nel gene della proteina centrosomale 290 (CEP290). Sono stati sottoposti a una singola iniezione di un medicinale per l’editing del genoma CRISPR/Cas9, EDIT-101 in un occhio, tramite una procedura chirurgica specializzata. Questo studio, che ha incluso il primo paziente a ricevere un medicinale sperimentale basato su CRISPR direttamente nel corpo, si è concentrato principalmente sulla sicurezza con un’analisi secondaria dell’efficacia.
Non sono stati segnalati eventi avversi gravi correlati al trattamento o alla procedura, né sono state riscontrate tossicità dose-limitanti. Per l’efficacia, i ricercatori hanno esaminato quattro misure: acuità visiva meglio corretta (BCVA); test di stimolo a campo intero adattato al buio (FST), navigazione della funzione visiva (VNC, misurata da un labirinto completato dai partecipanti) e qualità della vita correlata alla vista.
Undici partecipanti hanno dimostrato miglioramenti in almeno uno di questi risultati, mentre sei hanno dimostrato un miglioramento in due o più. Quattro partecipanti hanno avuto un miglioramento clinicamente significativo della acuità visiva. Sei partecipanti hanno sperimentato miglioramenti significativi nella visione mediata dal cono come indicato dalle FST, cinque dei quali hanno avuto miglioramenti in almeno uno degli altri tre risultati. I fotorecettori a cono vengono utilizzati per la visione diurna e centrale.
“I risultati dello studio BRILLIANCE forniscono prove di concetto e importanti insegnamenti per lo sviluppo di farmaci nuovi e innovativi per le malattie ereditarie della retina. Abbiamo dimostrato che possiamo somministrare in modo sicuro alla retina una terapia di editing genetico basata su CRISPR e avere risultati clinicamente significativi”, ha affermato Baisong Mei, MD, Ph.D., Chief Medical Officer, Editas Medicine.
Studi come questo mostrano la promessa della terapia genica per il trattamento di malattie incurabili. Il Gene and Cell Therapy Institute del Mass General Brigham sta aiutando a tradurre queste scoperte fatte dai ricercatori in primi studi clinici condotti sull’uomo e, in definitiva, in trattamenti che cambieranno la vita dei pazienti.
Esplorazione di CRISPR come trattamento dei disturbi retinici ereditari
Le mutazioni nel gene CEP290 sono la principale causa di cecità ereditaria che si verifica durante la prima decade di vita. Le mutazioni causano un funzionamento improprio dei fotocettori dei bastoncelli e dei coni nella retina dell’occhio, che dopo un po’ di tempo porterà alla perdita irreversibile della vista. Pierce lo paragona al guasto di una piccola parte di un motore, che alla fine porta l’intero motore a vacillare.
CRISPR-Cas9 è un kit di strumenti per l’editing genetico che agisce come una forbice guidata dal GPS per tagliare una porzione del genoma mutato per lasciare un gene funzionale. Per la cecità ereditaria, l’obiettivo era iniettare CRISPR per raggiungere la retina dell’occhio per ripristinare la capacità di produrre il gene e la proteina responsabili delle cellule sensibili alla luce.
La società di editing genomico Editas Medicine ha iniziato a esplorare come affrontare la mutazione CEP290 nel 2014, conducendo studi preclinici per determinare se un approccio di editing genetico come CRISPR-Cas9 potrebbe essere fattibile per colpire queste grandi mutazioni genetiche. Questo lavoro ha portato allo studio BRILLIANCE, iniziato a metà del 2019.
Il primo trattamento CRISPR (in vivo) ha avuto luogo presso il Casey Eye Institute dell’Oregon Health & Science University (OHSU), sotto la guida di Mark Pennesi, MD, Ph.D.
“Questo studio dimostra che l’editing genetico CRISPR ha un potenziale entusiasmante per il trattamento della Amaurosi congenita di Leber, degenerazione retinica ereditaria“, ha affermato Pennesi.
“Non c’è niente di più gratificante per un medico che ascoltare un paziente descrivere come la sua vista è migliorata dopo un trattamento. Uno dei partecipanti al nostro studio ha condiviso diversi esempi, tra cui quello di essere riuscito a ritrovare il telefono dopo averlo smarrito e di sapere che la sua macchina per il caffè era rotta. Sebbene questi tipi di compiti possano sembrare banali per coloro che sono normalmente vedenti, tali miglioramenti possono avere un enorme impatto sulla qualità della vita delle persone con problemi di vista“, ha aggiunto
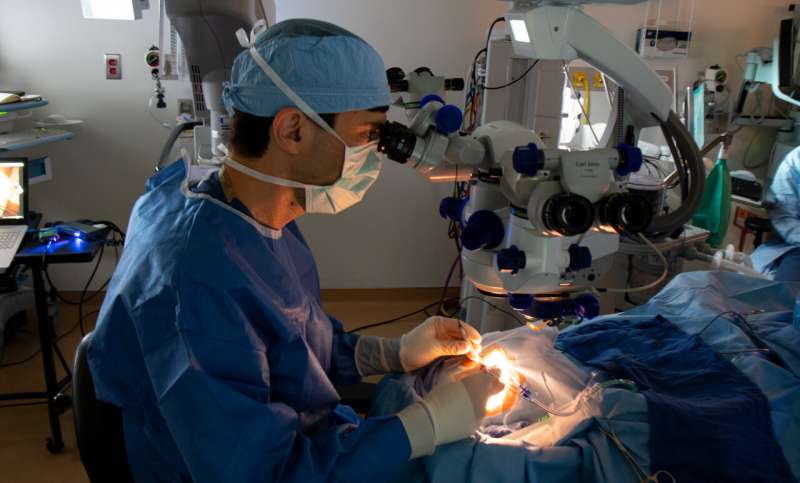
Il secondo paziente è stato curato al Mass Eye and Ear nel settembre 2020, a seguito dei ritardi causati dalla pandemia COVID-19. Ulteriori partecipanti sono stati trattati in altri tre centri di sperimentazione: Bascom Palmer Eye Institute, WK Kellogg Eye Center e Scheie Eye Institute presso il Children’s Hospital di Philadelphia (CHOP) e l’Ospedale dell’Università della Pennsylvania.
Due adulti hanno ricevuto una terapia a basso dosaggio, cinque hanno ricevuto una dose media e altri cinque hanno ricevuto un trattamento ad alto dosaggio. Due bambini, trattati al CHOP sotto la guida del medico Tomas S. Aleman, hanno ricevuto un trattamento a dose media.
“I nostri primi pazienti sono i bambini congenitamente ciechi ad essere trattati con l’editing genetico, che ha migliorato significativamente la loro visione diurna. La nostra speranza è che lo studio possa aprire la strada ai trattamenti dei bambini più piccoli con condizioni simili e portare a ulteriori miglioramenti nella vista”, ha affermato Aleman, Irene Heinz-Given e John LaPorte Research Professor in Oftalmologia presso Penn Medicine presso lo Scheie Eye Institute e un oftalmologo pediatrico presso il CHOP che è stato ricercatore principale del sito e coautore dello studio.
“Questo studio rappresenta una pietra miliare nel trattamento delle malattie genetiche, in particolare della cecità genetica, offrendo un importante trattamento alternativo, quando le forme tradizionali di terapia genica, come l’aumento genetico, non sono un’opzione“. ha agginto il ricercatore.
Leggi anche:Degenerazione retinica: farmaco già approvato migliora la vista
I partecipanti sono stati monitorati ogni tre mesi per un anno, quindi seguiti meno frequentemente per altri due anni. Durante le visite, sarebbero stati sottoposti a una serie di test sul siero e sulla vista per esaminare le misure di sicurezza ed efficacia dei risultati.
Nel novembre 2022, Editas ha sospeso l’iscrizione allo studio BRILLIANCE. Pierce e colleghi stanno valutando la possibilità di collaborare con altri partner commerciali per condurre ulteriori sperimentazioni, in collaborazione con Editas.
I ricercatori sperano che studi futuri possano esaminare il dosaggio ideale, se l’effetto del trattamento sia più pronunciato in determinati gruppi di età come i pazienti più giovani, e includere endpoint perfezionati per misurare gli effetti del miglioramento della funzione del cono sulle attività della vita quotidiana.