Batteri intestinali-Immagine astratto grafico Credito UTSW.
Uno studio dell’UTSW mostra che i batteri esposti agli antibiotici hanno sviluppato la capacità di morire più lentamente, nascondendosi all’interno delle cellule intestinali.
“Una sottopopolazione di batteri intestinali a cui è stato somministrato un antibiotico comunemente usato è diventata “persistente” e in grado di sopravvivere senza sviluppare una vera resistenza”, hanno scoperto gli scienziati dell’UT Southwestern Medical Center. I loro risultati, pubblicati su Cell Host & Microbe, potrebbero portare a modi migliori per combattere le infezioni batteriche.
“I ricercatori avevano ipotizzato l’esistenza di questi batteri persistenti sulla base di esperimenti con piastre di Petri, ma non è mai stato possibile osservarli svilupparsi in un ospite vivente“, ha affermato Andrew Koh, MD, Professore associato di pediatria e microbiologia. Il Dottor Koh ha co-condotto lo studio con Erdal Toprak, Ph.D., Professore Associato di Farmacologia e presso il Dipartimento di Bioinformatica di Lyda Hill. Entrambi sono membri dell’Harold C. Simmons Comprehensive Cancer Center.
“La resistenza agli antibiotici è una delle crisi più urgenti della medicina moderna”, ha spiegato il Dottor Koh, “con circa 2,8 milioni di infezioni resistenti agli antibiotici che provocano più di 35.000 morti all’anno negli Stati Uniti“. Ma come si sviluppa la resistenza agli antibiotici, in particolare negli ospiti animali vivi, non è chiaro. Uno dei motivi è che i topi, il modello di laboratorio per eccellenza, eliminano in modo efficiente diversi antibiotici somministrati in periodi di tempo prestabiliti, nel modo in cui la maggior parte dei pazienti umani riceve questi farmaci, causando una discrepanza tra le concentrazioni di antibiotici nei topi e negli esseri umani.
Nella speranza di osservare la formazione di resistenza agli antibiotici nei topi vivi, i ricercatori hanno sviluppato un modello murino in cui gli antibiotici venivano somministrati continuamente attraverso una pompa sottocutanea programmabile, consentendo alle concentrazioni sieriche di antibiotico di rimanere stabili finché la pompa rimaneva accesa.
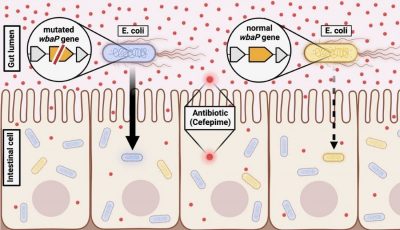
Lavorando con l’Escherichia coli – una specie comune di batteri intestinali – introdotto in topi “privi di germi” che non avevano un microbioma naturale, i ricercatori hanno scoperto che la maggior parte dei batteri veniva uccisa dall’antibiotico Cefepime. Ma alcuni di questi microbi sono sopravvissuti all’interno delle cellule intestinali e hanno impiegato più tempo a morire se trattati con antibiotici aggiuntivi in piastre di Petri rispetto all’E. coli isolato da topi non trattati.
L’analisi genetica ha mostrato che questi batteri persistenti avevano perso la funzione di un gene chiamato wbaP , che svolge un ruolo importante nella creazione di un rivestimento protettivo sulla superficie di E. coli e di alcune altre specie di batteri. Questa perdita sembrava essere fondamentale nel consentire ai batteri persistenti di invadere le cellule intestinali, dove la concentrazione di antibiotici era quasi 20 volte inferiore all’interno che all’esterno, e nel rallentare la morte dei batteri in seguito all’esposizione ad elevate concentrazioni di antibiotici.
Tali persistenza potrebbero essere la ragione per cui gli antibiotici a volte non eliminano completamente le infezioni, consentendo lo sviluppo di una pericolosa resistenza agli antibiotici – uno scenario che il Dott. Toprak e Koh e i loro colleghi intendono indagare in studi futuri. Il modello innovativo sviluppato potrebbe essere utilizzato per esaminare una serie di domande relative alla resistenza agli antibiotici negli animali vivi, incluso se determinati alimenti, batteri commensali, altri farmaci o condizioni autoimmuni possano influenzare la sopravvivenza e la resistenza batterica in seguito all’esposizione agli antibiotici.
Il Dottor Koh, un medico-scienziato e il Dottor Toprak, un biofisico sperimentale, hanno notato che la loro collaborazione è una testimonianza dell’ambiente collegiale dell’UTSW, che incoraggia i partenariati interdisciplinari.
Leggi anche:Cancro dell intestino: la chiave nei batteri intestinali?
“Questa iniziativa esemplifica come le complesse sfide globali possano essere affrontate in modo più efficace unendo diversi campi scientifici“, ha affermato il Dottor Toprak, studioso di ricerca biomedica della Southwestern Medical Foundation.
Fonte:Newswise