Colesterolo-Immagine Credit Public Domain.
Gli scienziati guidati da un team della Duke-NUS Medical School hanno fatto un passo avanti nella comprensione dei meccanismi che influenzano la crescita e lo sviluppo delle cellule tumorali. Nell articolo pubblicato sul Journal of Clinical Investigation, i ricercatori mettono in luce il ruolo precedentemente nascosto di un nuovo enzima, chiamato dominio contenente idrossilasi degli acidi grassi 2 (FAXDC2), rivelando il suo ruolo fondamentale nella sintesi del colesterolo e nella progressione del cancro.
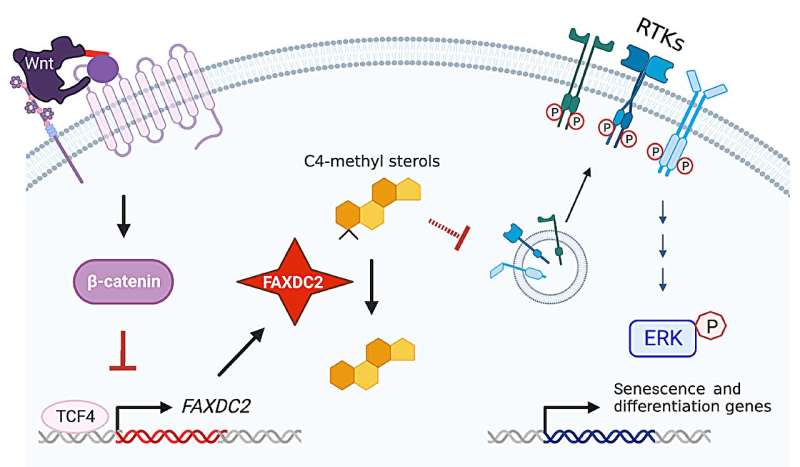
Lo studio descrive in dettaglio la cascata di eventi molecolari che vanno dalla soppressione di FAXDC2 all’interruzione della normale sintesi del colesterolo fino all’alterazione del destino del cancro, evidenziando una potenziale vulnerabilità nelle cellule tumorali che potrebbe essere presa di mira per un intervento terapeutico.
“Il nostro viaggio nei fattori cellulari del cancro è iniziato con l’esplorazione della via di segnalazione Wnt, un attore cruciale nella crescita e nello sviluppo delle cellule“, ha spiegato la Prof.ssa assistente Babita Madan, prima autrice dello studio del Cancer & Stem Cell Biology della Duke-NUS. (CSCB). “È stato durante questi studi che ci siamo imbattuti nell’enzima FAXDC2, che è emerso come figura centrale nel controllo del cancro e delle cellule staminali. La nostra scoperta suggerisce che l’attività di FAXDC2, o la sua soppressione, ha profonde implicazioni per la crescita e la differenziazione cellulare, dipingendo un complesso quadro della relazione tra la biologia del cancro e la sintesi del colesterolo”.
La ricerca è iniziata con un’analisi approfondita della via di segnalazione Wnt, nota per il suo ruolo fondamentale nella regolazione della crescita delle cellule normali e tumorali. La segnalazione Wnt è una via di segnalazione chiave che regola la crescita, lo sviluppo e il mantenimento delle cellule del cervello, della pelle, dei capelli e dell’intestino.
“Tuttavia, la segnalazione Wnt iperattiva, presente nei modelli di cancro impiegati nello studio, compromette la differenziazione cellulare e mantiene i tumori in uno stato simile alle cellule staminali. Queste cellule staminali tumorali indifferenziate proliferano rapidamente e in modo incontrollabile, promuovendo una progressione più rapida del tumore e sono resistenti alle terapie antitumorali.
Uno studio condotto da scienziati della Duke-NUS Medical School ha identificato il ruolo fondamentale, ma precedentemente sconosciuto di un enzima, chiamato FAXDC2, che viene soppresso nei tumori con segnalazione Wnt iperattiva. FAXDC2 regola la produzione di colesterolo e di molecole di segnalazione cellulare e la sua soppressione provoca una crescita cellulare anormale. Il ripristino della funzione FAXDC2 potrebbe potenzialmente normalizzare il comportamento cellulare in questi tumori.
Utilizzando tecnologie genomiche all’avanguardia per svelare questo complesso processo biologico, l’attenzione degli scienziati è stata attirata dall’enzima FAXDC2 quando hanno scoperto che aumentava notevolmente dopo che modelli di cancro al pancreas erano stati trattati con un inibitore Wnt prodotto a Singapore, ETC-159.
Analisi approfondite di campioni di tessuto tumorale del colon-retto hanno confermato questa scoperta, mostrando un modello coerente di soppressione di FAXDC2 e successivo accumulo di precursori del colesterolo, incluso un elemento costitutivo del colesterolo chiamato lofenolo. Più bassa è l’espressione di FAXDC2, maggiore è il livello di lofenolo.
“FAXDC2 è un enzima precedentemente sconosciuto che aiuta a produrre colesterolo dal precursore lofenolo. È importante sottolineare che la quantità di FAXDC2 presente nelle cellule modifica la quantità di lofenolo presente”, ha spiegato il Professor David Virshup, Direttore del programma CSCB e autore senior dello studio. “Il Lophenol sembra modulare l’attività del percorso di differenziazione e, pertanto, riteniamo che aiuti a mantenere le cellule tumorali in uno stato più simile alle cellule staminali“.
Il Professor Virshup ha sottolineato le implicazioni più ampie di queste intuizioni, affermando: “Questo studio fornisce uno sguardo affascinante sul meccanismo molecolare delle cellule tumorali. Il ruolo di FAXDC2 nella regolazione della sintesi del colesterolo apre nuove strade per terapie future. La comprensione di questi complessi meccanismi apre la strada a approcci innovativi per combattere il cancro, sottolineando l’importanza degli intermedi della biosintesi del colesterolo come importanti molecole di segnalazione e potenziali farmaci”.
La scoperta del ruolo di FAXDC2 nella biologia del cancro segna solo l’inizio di un viaggio scientifico più lungo. Sono necessarie ulteriori ricerche per comprendere appieno come la soppressione di FAXDC2 e i conseguenti cambiamenti nel metabolismo del colesterolo possano essere sfruttati per sviluppare nuove terapie antitumorali.
Il gruppo di ricerca è interessato a esplorare il potenziale terapeutico del target FAXDC2 nel trattamento del cancro, considerandolo come una possibile strada per lo sviluppo di farmaci che potrebbero inibire la crescita del cancro modulando le vie di sintesi del colesterolo.
Inoltre, i risultati stimolano l’interesse verso strategie preventive che potrebbero mitigare il rischio di sviluppo del cancro mantenendo l’equilibrio dei precursori del colesterolo nel corpo. Comprendere i fattori scatenanti che portano alla soppressione di FAXDC2 nelle cellule tumorali potrebbe aprire la strada a nuove metodologie di prevenzione, offrendo potenzialmente una nuova speranza nella lotta contro il cancro.
Leggi anche:Cancro al pancreas: colesterolo come bersaglio emergente del cancro
“Questi risultati rispecchiano il nostro costante impegno nel migliorare la cura dei pazienti attraverso scoperte cruciali“, ha commentato il Professor Patrick Tan, vicePresidente senior per la ricerca presso Duke-NUS. “La strada da percorrere prevede una ricerca rigorosa e una collaborazione tra varie discipline, tutte mirate a tradurre queste intuizioni fondamentali in scoperte mediche tangibili che un giorno potrebbero trasformare le strategie di trattamento e prevenzione del cancro“.