Le cellule nervose del cervello richiedono un’enorme quantità di energia per sopravvivere e mantenere le loro connessioni per comunicare con altre cellule nervose. Nella malattia di Alzheimer, la capacità di produrre energia è compromessa e le connessioni tra le cellule nervose (chiamate sinapsi) alla fine si disgregano e appassiscono, causando la sbiadimento e il venir meno dei nuovi ricordi.
Un gruppo di ricerca della Scripps Research Institute, in un articolo pubblicato sulla rivista Advanced Science, ha ora identificato le reazioni energetiche nelle cellule cerebrali che malfunzionano e portano alla neurodegenerazione. Utilizzando una piccola molecola per risolvere il malfunzionamento che si è verificato nei mitocondri, i principali produttori di energia della cellula, i ricercatori hanno dimostrato che molte connessioni neurali sono state ripristinate con successo in modelli di cellule nervose derivati da cellule staminali umane di pazienti affetti da Alzheimer. Questi risultati evidenziano che il miglioramento del metabolismo mitocondriale potrebbe essere un obiettivo terapeutico promettente per l’Alzheimer e i disturbi correlati.
“Abbiamo pensato che se fossimo riusciti a riparare l’attività metabolica nei mitocondri, forse avremmo potuto salvare la produzione di energia“, afferma l’autore senior dello studio, Stuart Lipton, MD, Ph.D., Professore della Step Family Foundation e co-Direttore del Neurodegeneration New Medicines. Center presso lo Scripps Research e neurologo clinico a La Jolla, in California. “Nell’utilizzo di neuroni umani derivati da persone affette da Alzheimer, la protezione dei livelli energetici è stata sufficiente per salvare un gran numero di connessioni neuronali“.
Nel nuovo studio, Lipton e il suo team hanno trovato un blocco negli enzimi che producono energia a causa di un’etichetta anomala di atomi di azoto (N) e ossigeno (O) su un atomo di zolfo (S), che insieme formano un “SNO” disfunzionale. Questa reazione è chiamata S-nitrosilazione e il team ha dimostrato che una virtuale “SNO-Storm” di queste reazioni si è verificata nei neuroni del cervello di pazienti con Alzheimer.
Lipton e i suoi colleghi hanno inizialmente scoperto il “tag SNO” sugli enzimi energetici confrontando i cervelli umani (ottenuti durante l’autopsia di persone affette da malattia di Alzheimer) con quelli senza malattie cerebrali. I ricercatori hanno successivamente generato cellule nervose da cellule staminali derivate da biopsie cutanee di persone con e senza una mutazione genetica che causa la malattia di Alzheimer. Quindi, utilizzando una serie di etichette metaboliche e un apparecchio per la misurazione dell’ossigeno, hanno calcolato la produzione di energia cellulare e identificato deficit unici nelle cellule nervose dell’Alzheimer rispetto ai controlli.
I ricercatori hanno scoperto che i neuroni avevano un ciclo di Krebs interrotto, il processo cellulare nei mitocondri che produce la maggior parte della fonte di energia molecolare cruciale del corpo, l’ATP. Il team ha individuato un blocco nella fase in cui si forma una molecola chiave: il succinato, che guida gran parte della successiva produzione di ATP. Nello studio, il blocco ha inibito la capacità dei mitocondri di produrre l’energia necessaria per sostenere i neuroni e le loro numerose connessioni.
I ricercatori hanno ipotizzato che se fossero riusciti a fornire alcune delle molecole di succinato mancanti, avrebbero potuto ripristinare la produzione di energia, essenzialmente riavviando il ciclo di Krebs mitocondriale in stallo. Poiché il succinato non viaggia facilmente dentro o fuori dalle cellule, I ricercatori hanno utilizzato un analogo che potesse passare meglio attraverso le membrane delle cellule nervose. La strategia ha funzionato, riparando fino a tre quarti delle sinapsi che erano andate perse, prevenendo al contempo un ulteriore declino.
“Il succinato non è un composto che le persone possono ora assumere come trattamento, ma è la prova di principio che è possibile riattivare il ciclo di Krebs“, afferma Lipton. “La bellezza dello studio è che siamo stati in grado di dimostrarlo nelle cellule nervose viventi derivate da pazienti affetti da Alzheimer, ma dobbiamo ancora trovare un composto molto migliore per sviluppare un farmaco efficace che possa essere assunto dagli esseri umani“.
Leggi anche:Alzheimer: cellule immunitarie esauste possono essere responsabili
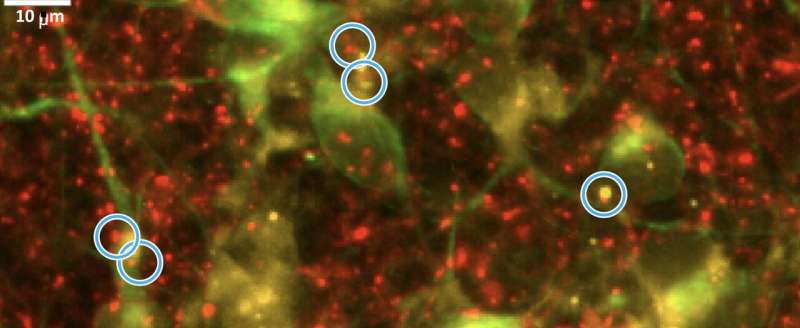
Immagine: le cellule nervose dell’Alzheimer manifestano una diminuzione delle connessioni tra le cellule nervose, chiamate sinapsi, mostrate qui all’interno dei cerchi blu. Metà della sinapsi è contrassegnata da una macchia fluorescente rossa e l’altra metà da una macchia gialla. Credito: Scripps Research.
Lipton ha una storia di sviluppo di farmaci approvati dalla FDA per il morbo di Alzheimer, come Namenda, e riconosce che qui è necessario molto più lavoro per produrre un ulteriore farmaco che preservi energia che sia sicuro ed efficace negli esseri umani. Il suo laboratorio continuerà a perseguire il ciclo mitocondriale di Krebs come promettente bersaglio terapeutico nella speranza di poter ripristinare la connettività neuronale nei pazienti con Alzheimer, arrestando così la progressione della malattia e migliorando la funzione cognitiva.
Oltre a Lipton, gli autori dello studio includono Alexander Andreyev, Nima Dolatabadi, Xu Zhang, Melissa Luevanos, Mayra Blanco, Christine Baal, Ivan Putra e Tomohiro Nakamura di Scripps Research; Hongmei Yang e Steven Tannenbaum del MIT; e Paschalis-Thomas Doulias e Harry Ischiropoulos della Perelman School of Medicine dell’Università della Pennsylvania.
Immagine Credit Public Domain.
Fonte: Advanced Science