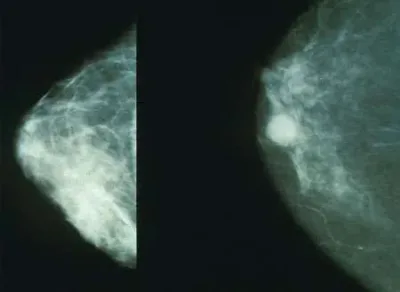
Cancro al seno triplo negativo-Immagine: mammografie che mostrano un seno normale (a sinistra) e un seno con cancro (a destra). Credito: dominio pubblico-
I ricercatori dell’Università di Liverpool hanno creato un composto biomedico che ha il potenziale per fermare la diffusione del cancro al seno triplo negativo.
Il documento, “Targeted Destruction of S100A4 Inhibits Metastasis of Triple Negative Breast Cancer Cells”, è pubblicato su Biomolecules.
Scienziati dei dipartimenti di Chimica e Biochimica dell’Università di Liverpool e della Nanjing Medical School in Cina hanno scoperto un possibile modo per bloccare le proteine prodotte nel corpo quando un paziente ha il cancro e che ne provoca la diffusione ad altre parti del corpo. Questo processo, chiamato metastasi, è in gran parte responsabile della morte dei pazienti.
Il problema principale che ostacola il successo del trattamento dei tumori che si verificano comunemente non è il tumore primario che di solito può essere rimosso chirurgicamente, ma la sua diffusione ad altri organi del corpo.
Il Professor Philip Rudland, Professore emerito presso il Dipartimento di biochimica dell’Università di Liverpool, ha dichiarato: “Come regola generale, il cancro che si è diffuso viene trattato con la chemioterapia, ma questo trattamento raramente può essere somministrato senza danneggiare gravemente o diventare tossico per il paziente. L’importanza del nostro lavoro è stata quella di identificare un obiettivo specifico e importante da attaccare, senza effetti collaterali tossici”.
Il team di ricerca ha scoperto in passato che specifiche proteine sono coinvolte nel processo metastatico; queste proteine sono diverse da quelle coinvolte nella produzione del tumore primario. Uno di questi esempi è una proteina chiamata “S100A4”, ed è la proteina scelta dal gruppo di ricerca come bersaglio per l’identificazione di inibitori chimici della metastasi, utilizzando sistemi modello di cellule del carcinoma mammario senza recettore ormonale altamente metastatico e incurabile.
Usando questi sistemi modello, i ricercatori hanno scoperto un nuovo composto che può bloccare specificamente l’interazione di questa proteina S100A4 che induce metastasi con il suo bersaglio all’interno della cellula. I ricercatori del Dipartimento di Chimica hanno quindi sintetizzato una sostanza chimica più semplice e l’hanno collegata a una testata che stimola il normale meccanismo di degradazione delle proteine di una cellula.
Questo composto ora funziona a dosi molto basse per inibire le proprietà associate alla metastasi, un miglioramento di oltre 20.000 volte rispetto all’inibitore originale ora disarmato e praticamente senza effetti collaterali tossici. Inoltre, in collaborazione con ricercatori cinesi della Nanjing Medical School, i ricercatori hanno dimostrato che questo composto inibisce la metastasi in simili tumori metastatici nei topi, suggerendo un potenziale ruolo terapeutico.
Spiegano gli autori:
“Il cancro al seno rappresenta circa un quarto dei casi di cancro nelle donne (in tutto il mondo 2,2 milioni nel 2020) e quasi un terzo di queste donne sono morte (685.000) a causa della malattia. Il tipo più mortale di cancro al seno è quello senza recettori ormonali, il cancro al seno triplo negativo (TNBC) che rappresenta il 10-15% di tutti i tumori al seno, con tre volte il rischio di morte dei pazienti entro 5 anni. Questo aumento della mortalità è dovuto a una mancanza di specificità degli agenti chemioterapici impiegati, poiché agenti antiormonali specifici sono inefficaci nel TNBC privo di recettori. Pertanto, i nuovi trattamenti per TNBC sono di alta priorità per soddisfare questa esigenza clinica. La maggior parte delle pazienti, tuttavia, che soffrono di carcinoma mammario e altri carcinomi, non muoiono a causa del tumore primario, ma per disseminazione o metastasi. Alcune cellule tumorali possiedono la capacità di migrare e invadere il tessuto vicino e alla fine metastatizzare mentre altre no. Questi risultati suggeriscono che specifici geni/proteine coinvolti nel processo metastatico, sono diversi da quelli coinvolti nella produzione del tumore primario. Queste proteine sono state chiamate proteine che inducono metastasi, un esempio è S100A4, un membro della famiglia S100 che lega il calcio. S100A4 è espresso nella maggior parte dei tumori metastatici umani ed è associato alla morte prematura di pazienti con diversi tipi di carcinomi, compresi quelli della mammella, della mucosa orale, della vescica, del pancreas, della prostata, del colon-retto, dell’esofago, del polmone, dello stomaco e delle ghiandole tiroidee. Sebbene S100A4 non possa stimolare la proliferazione cellulare o indurre la formazione di tumori da solo, può stimolare la cascata metastatica come dimostrato nei sistemi di mosche modello e roditori mediante l’interazione con oncogeni come ras Val12. Pertanto, il grande vantaggio di S100A4 rispetto agli oncogeni standard come bersaglio per la terapia antitumorale è che induce e mantiene direttamente le metastasi e la sua soppressione non provoca effetti dannosi negli animali. Questi fatti sono in contrasto con quelli degli oncogeni standard che non possono indurre metastasi direttamente la cui soppressione come proto-oncogeni causa gravi effetti deleteri negli animali.
Leggi anche:Cancro al seno triplo negativo: combinazione di farmaci blocca la progressione
La Dott.ssa Gemma Nixon, docente senior di chimica farmaceutica presso l’Università di Liverpool, ha dichiarato: “Questo è un entusiasmante passo avanti nella nostra ricerca. Ora speriamo di compiere i prossimi passi e ripetere questo studio in un ampio gruppo di animali con tumori metastatici simili in modo che l’efficacia e la stabilità dei composti possano essere studiate a fondo e, se necessario, migliorate mediante ulteriori progetti e sintesi, prima di qualsiasi sperimentazione clinica. Significativamente, questa particolare proteina che stiamo studiando è coinvolta in molti tumori diversi, il che potrebbe significare che questo approccio potrebbe essere valido per molti altri tumori umani comuni”.
Fonte:Biomolecules