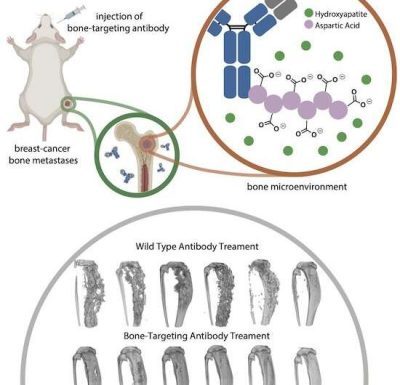
(Cancro al seno-Immagine: gli scienziati della Rice hanno aggiunto un peptide mirato all’osso a un anticorpo usato per combattere il cancro al seno per ridurre le metastasi ossee. Credito: Xiao Research Group).
Una quantità moderata di un farmaco antitumorale biologico potenziato dai peptidi fa molto nel trattamento dei tumori al seno che metastatizzano alle ossa.
Uno studio condotto da scienziati della Rice University e del Baylor College of Medicine ha dimostrato l’efficacia del trattamento di tali tumori nei modelli di roditori, facendo sperare in nuove terapie per il trattamento delle metastasi ossee.
Lo studio, che apparirà sulla copertina della rivista ACS Central Science dell’American Chemical Society, fa avanzare le tecniche sperimentate dal chimico della Rice Han Xiao e dal suo coautore alla Baylor, il biologo Xiang Zhang.
I ricercatori hanno scoperto attraverso test approfonditi che l’ingegnerizzazione dei peptidi “bone-homing” e il loro collegamento a un comune farmaco contro il cancro al seno, l’anticorpo Trastuzumab, mira e attacca efficacemente le metastasi ossee.
I ricercatori hanno riportato con sorpresa che l’aumento della dose del composto farmacologico non lo rende migliore. Il farmaco contiene un peptide ingegnerizzato che trova e si lega all’osso, ma ha funzionato meglio quando è stata somministrata una quantità moderata.
“La carica negativa del peptide ha un’affinità per la nicchia del cancro alle ossa caricata positivamente”, ha detto Xiao, il cui laboratorio ha creato una libreria di anticorpi modificati per i test. “Abbiamo scoperto che l’efficacia terapeutica è migliore con l’anticorpo che ha un’affinità mediocre. Questa è davvero una grande scoperta”.

Ben il 40% delle sopravvissute al cancro al seno alla fine presenta metastasi a organi distanti, il più delle volte all’osso. Xiao ha notato che i tumori ossei sono notoriamente difficili da trattare, data la natura dura del materiale e la rete vascolare limitata. La somministrazione di una bassa quantità di farmaco, può anche aiutare i tumori a sviluppare resistenza.
Lo studio ha dimostrato che gli anticorpi potenziati dai peptidi prevengono anche le metastasi secondarie dall’osso ad altri organi.
Vedi anche:Cancro al seno: riduzione livelli di rame blocca le metastasi
Spiegano gli autori:
“Nonostante la rapida evoluzione degli anticorpi terapeutici, la loro efficacia clinica nel trattamento dei tumori ossei è ostacolata dalla farmacocinetica inadeguata e dalla scarsa accessibilità al tessuto osseo di queste grandi macromolecole. Qui, mostriamo che l’ingegneria degli anticorpi terapeutici con sequenze peptidiche homing dell’osso migliora notevolmente le loro concentrazioni nella nicchia metastatica ossea, con conseguente riduzione significativa della sopravvivenza e della progressione delle metastasi ossee del cancro al seno. Per migliorare la capacità di mirare al tumore osseo degli anticorpi ingegnerizzati, abbiamo introdotto un numero variabile di peptidi di localizzazione ossea nei siti permissivi dell’anticorpo anti-HER2, Trastuzumab. Rispetto all’anticorpo non modificato, gli anticorpi ingegnerizzati hanno una farmacocinetica simile e in vitro attività citotossica, ma mostrano una migliore distribuzione nel tumore osseo in vivo. Di conseguenza, nei modelli di xenotrapianto di metastasi del cancro al seno in siti ossei, gli anticorpi ingegnerizzati con una maggiore specificità ossea mostrano una maggiore inibizione sia delle metastasi ossee iniziali che delle metastasi multiorgano secondarie. Inoltre, questa strategia ingegneristica viene applicata anche per preparare coniugati anticorpo-farmaco mirati all’osso con una maggiore efficacia terapeutica. Questi risultati dimostrano che l’aggiunta di un target specifico per l’osso alla terapia con anticorpi si traduce in una solida efficacia nel rilascio nel tumore osseo. Ciò fornisce una potente strategia per superare la scarsa accessibilità degli anticorpi ai tumori ossei e la conseguente resistenza alla terapia”.
Astratto grafico:

I ricercatori sperano di trovare collaboratori per spostare la strategia verso le sperimentazioni umane.
Il borsista post-dottorato di Rice Zeru Tian e lo studente laureato Chanfei Yu sono co-autori principali del documento. I coautori sono i borsisti post-dottorato di Baylor Weijie Zhang e Zhan Xu e l’associato post-dottorato Ling Wu; gli studenti laureati della Rice Kuan-Lin Wu, Chenhang Wang e Yuda Chen e l’allieva della Rice Ruchi Gupta, ora una studentessa laureata alla Yale School of Medicine.
Xiao è un giovane investigatore del The Norman Hackerman-Welch e Assistente Professore di chimica, bioscienze e bioingegneria. Zhang è professore associato di biologia molecolare e cellulare presso il McNair Scholar del Lester and Sue Smith Breast Center di Baylor.
Fonte: ACS Central Science